
 习题精选系列答案
习题精选系列答案科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
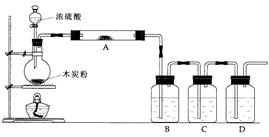
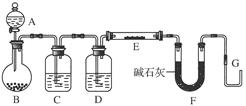
 ;
; 中可以燃烧。
中可以燃烧。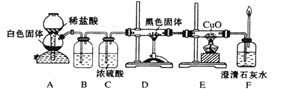
 置C吸收气体中水蒸气的理由是_
置C吸收气体中水蒸气的理由是_ ______。
______。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.鉴别集气瓶中的甲烷和乙烯:分别点燃,观察火焰的颜色及是否有黑烟 |
| B.检验酒精中的少量水:向酒精中加入足量生石灰 |
| C.制备氯乙烷(C2H5Cl):将乙烷和氯气的混合气放在光照条件下反应 |
| D.除去乙烷中的乙烯气体:将实验室制得的乙烯气体通入NaOH 溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在溴乙烷中滴加硝酸银溶液,检验溴乙烷分子中含有溴原子 |
| B.在两支分别盛有少量苯和四氯化碳的试管中加碘水后振荡,区分苯和四氯化碳 |
| C.酒精与碘水混合并振荡,萃取碘水中的碘 |
| D.在苯中加铁粉后再加溴水并振荡,制取溴苯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.量筒 | B.容量瓶 | C.滴定管 | D.烧杯 |
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
| 实验步骤 | 实验操作 | 实验操作目的 |
| 步骤1 | | |
| 步骤2 | | |
| 步骤3 | | |
| 步骤4 | 洗涤沉淀 | |
| 步骤5 | | 得到FeSO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液。完成以下实验探究过程:
mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液。完成以下实验探究过程: 作、预期现象和结论。
作、预期现象和结论。| 编号 | 实验操作 | 实验现象 | 结论 |
| ① | 用药匙取少许样品,加入试管A中,再用滴管取过量  ____ 溶液并滴加到试管A中,充分反应 ____ 溶液并滴加到试管A中,充分反应 | 有固体剩余,并有气泡产生 | 合金中除铝外还含有Fe、Cu 元素 |
| ② | 往试管A的剩余固体中加过量 ________ ,充分反应后,静置,取上层清液于试管B中 | 固体部分溶解,并有气体放出,溶液呈浅绿色 | |
| ③ | 往试管B中加入少量 _____,再滴加KSCN溶液 | _____ | |
| ④ | 往②剩余固体中加入稀硝酸;再滴加 ____________ 溶液. | 固体溶解,有无色刺激性气体产生并很快变成红棕色,溶液显蓝色;再加某溶液后有蓝色沉淀产生 |
查看答案和解析>>
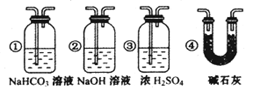
科目:高中化学 来源:不详 题型:实验题
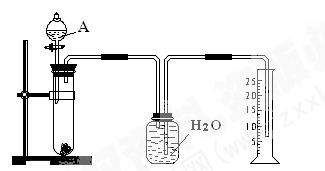
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
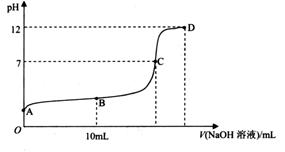
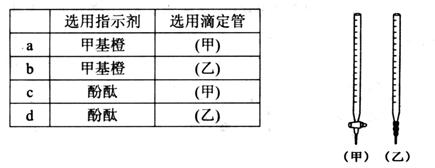
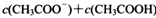 ________
________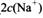 (选填“>”、“<”或“=”);
(选填“>”、“<”或“=”);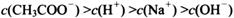
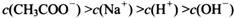
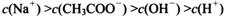
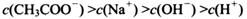
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com