


 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案科目:高中化学 来源: 题型:
 室温下,将1.00mol?L-1盐酸滴入20.00mL1.00mol?L-1氨水中,溶液pH随加入盐
室温下,将1.00mol?L-1盐酸滴入20.00mL1.00mol?L-1氨水中,溶液pH随加入盐查看答案和解析>>
科目:高中化学 来源: 题型:
 (2012?河西区一模)室温下,将1.00mol?Lˉ1盐酸滴入20.00mL 1.00mol?Lˉ1氨水中,溶液pH随加入盐酸体积变化的曲线如右图所示.下列说法正确的是( )
(2012?河西区一模)室温下,将1.00mol?Lˉ1盐酸滴入20.00mL 1.00mol?Lˉ1氨水中,溶液pH随加入盐酸体积变化的曲线如右图所示.下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
 室温下,将1.00mol/L盐酸滴入20.00mL 1.00mol/L氨水中,溶液pH和温度(℃)
室温下,将1.00mol/L盐酸滴入20.00mL 1.00mol/L氨水中,溶液pH和温度(℃)+ 4 |
| 离子浓度的关系 | 溶质 | 溶液的pH | 物料守恒关系 | |
| ① | C(NH4+)>C(Cl-)>C(OH-)>C(H+) | NH4Cl、NH3?H2O NH4Cl、NH3?H2O |
pH>7 | / |
| ② | NH4Cl | / | c(NH4+)+c(NH3?H2O)=c(Cl-) c(NH4+)+c(NH3?H2O)=c(Cl-) | |
| ③ | C(Cl-)>C(H+)>C(NH4+)>C(OH-) | NH4Cl、HCl NH4Cl、HCl |
pH<7 | / |
查看答案和解析>>
科目:高中化学 来源: 题型:
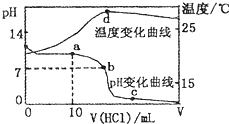 室温下,将1.00mol?L-1盐酸滴入20.00 mL 1.00mol?L-1的氨水中,溶液pH和温度随加入盐酸体积的变化曲线如图所示.下列有关说法中不正确的是( )
室温下,将1.00mol?L-1盐酸滴入20.00 mL 1.00mol?L-1的氨水中,溶液pH和温度随加入盐酸体积的变化曲线如图所示.下列有关说法中不正确的是( )A、a点溶液中离子浓度大小的关系:c(NH
| ||
B、b点溶液中离子浓度大小的关系:c(NH
| ||
C、c点溶液中离子浓度大小的关系:c(NH
| ||
| D、d点时溶液温度达到最高,之后温度略有下降,原因是NH3?H2O电离吸热 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省莱芜市高三上学期期末检测化学试卷 题型:选择题
.室温下,将1.00mol· 盐酸滴人20.00mL1.00
盐酸滴人20.00mL1.00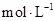 氨水中,溶液pH随加人盐酸体积变化曲线如图所示。下列有关说法正确的是
氨水中,溶液pH随加人盐酸体积变化曲线如图所示。下列有关说法正确的是

D.a点:pH=14
B.b点:
C.c点,水电离出的
D.c点后,溶液中离子浓度大小关系一定为: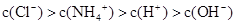
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com