
【题目】下列解释事实的化学用语正确的是
A.用饱和 Na2CO3 溶液浸泡锅炉水垢除去其中的 CaSO4:CO![]() + CaSO4
+ CaSO4![]() CaCO3 + SO
CaCO3 + SO![]()
B.用白醋和淀粉 KI 试纸检验加碘盐中的 KIO3:5I + IO![]() + 3H2O = 3I2 + 6OH-
+ 3H2O = 3I2 + 6OH-
C.碱性条件下,用 KClO 溶液与 Fe(OH)3 反应制备新型净水剂 K2FeO4: 3ClO + 2Fe(OH)3 = 2FeO![]() + 3Cl + 4H+ + H2O
+ 3Cl + 4H+ + H2O
D.氯碱工业制备氯气:2Cl + 2H+ ![]() Cl2↑+ H2↑
Cl2↑+ H2↑
【答案】A
【解析】
A. 用饱和Na2CO3溶液浸泡锅炉水垢,可以发生沉淀的转化,其离子方程式为CO![]() + CaSO4
+ CaSO4![]() CaCO3+ SO
CaCO3+ SO![]() ,A正确;
,A正确;
B. 用白醋和淀粉 KI 试纸可以检验加碘盐中的KIO3,因为在酸性条件下KI 和KIO3可以发生归中反应,其离子方程式为5I + IO![]() + 6CH3COOH = 3I2+ 3H2O+6CH3COO-,B不正确;
+ 6CH3COOH = 3I2+ 3H2O+6CH3COO-,B不正确;
C. 碱性条件下,用 KClO 溶液与Fe(OH)3反应制备新型净水剂K2FeO4,该反应的离子方程式为3ClO+ 2Fe(OH)3+4OH- = 2FeO![]() + 3Cl+ 5 H2O,C不正确;
+ 3Cl+ 5 H2O,C不正确;
D. 氯碱工业电解饱和食盐水制备氯气,该反应的离子方程式为2Cl+ 2 H2O![]() Cl2↑+ H2↑+2OH-,D不正确。
Cl2↑+ H2↑+2OH-,D不正确。
故选A。


科目:高中化学 来源: 题型:
【题目】将0.1 mol/L CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起( )
A. 溶液的pH增大
B. CH3COOH电离度增大
C. 溶液的导电能力减弱
D. 溶液中c(OH-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌锰干电池的负极是作为电池壳体的金属锌,正极是被二氧化锰和碳粉包围的石墨电极,电解质是氯化锌和氯化铵的糊状物,该电池放电过程中产生MnOOH。废旧电池中的Zn、Mn元素的回收,对环境保护有重要的意义。
Ⅰ.回收锌元素,制备ZnCl2
步骤一:向除去壳体及石墨电极的黑色糊状物中加水,搅拌,充分溶解,经过滤分离得固体和滤液。
步骤二:处理滤液,得到ZnCl2·xH2O晶体。
步骤三:将SOCl2与ZnCl2·xH2O晶体混合制取无水ZnCl2。
制取无水ZnCl2,回收剩余的SOCl2并验证生成物中含有SO2(夹持及加热装置略)的装置如图:

(已知:SOCl2是一种常用的脱水剂,熔点-105℃,沸点79℃,140℃以上时易分解,与水剧烈反应生成两种气体。)
(1)写出SOCl2与水反应的化学方程式:__。
(2)接口的连接顺序为a→__→__→h→i→__→__→__→e。
Ⅱ.回收锰元素,制备MnO2
(3)洗涤步骤一得到的固体,判断固体洗涤干净的方法:__。
(4)洗涤后的固体经初步蒸干后进行灼烧,灼烧的目的:__。
Ⅲ.二氧化锰纯度的测定
称取1.40g灼烧后的产品,加入2.68g草酸钠(Na2C2O4)固体,再加入足量的稀硫酸并加热(杂质不参与反应),充分反应后冷却,将所得溶液转移到100mL容量瓶中用蒸馏水稀释至刻线,从中取出20.00mL,用0.0200mol/L高锰酸钾溶液进行滴定,滴定三次,消耗高锰酸钾溶液体积的平均值为17.30mL。
(5)写出MnO2溶解反应的离子方程式__。
(6)产品的纯度为__。
(7)若灼烧不充分,滴定时消耗高锰酸钾溶液体积__(填“偏大”“偏小”“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,体积为5L的密闭容器中,0.5molX和0.5molY进行反应:
2X(g)+Y(g)![]() 2Z(g),经60s达到平衡,生成0.2molZ。下列说法正确的是:
2Z(g),经60s达到平衡,生成0.2molZ。下列说法正确的是:
A. 将容器体积变为10L,Z的平衡浓度变为原来的![]()
B. 在该温度下,该反应的平衡常数K=0.011
C. 达到平衡时,容器内气体的压强是原来的90%
D. 若降低温度,X的体积分数增大,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚丙烯腈纤维商品名叫腈纶,性质极像羊毛,故被称为“人造羊毛”。聚丙烯腈的单体是丙烯腈(CH2=CHCN),其合成方法很多,如以乙炔为原料,其合成过程的化学方程式如下:
①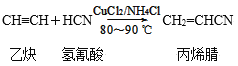
②nCH2=CHCN![]()
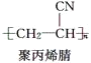
阅读以上材料,回答问题:
(1)制备丙烯腈的反应类型是__。
(2)聚丙烯腈中氮的质量分数为__。
(3)如何检验某品牌的羊毛衫是羊毛还是“人造羊毛”?__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g)![]() 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
A. m=2
B. 两次平衡的平衡常数相同
C. X与Y的平衡转化率之比为1:1
D. 第二次平衡时,Z的浓度为0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,H2(g)与I2(g)反应生成HI(g),反应的能量变化如下图所示。下列说法不正确的是

A.H2(g)+I2(g)=2HI(g) ΔH=-13kJ·mol1
B.反应物的总能量比生成物的总能量高
C.H2(g)和I2(g)的总能量比HI(g)的能量高13kJ
D.断裂反应物中化学键吸收的总能量比形成生成物中化学键放出的总能量低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物 Y 能用于高性能光学树脂的合成,可由化合物 X 与 2-甲基丙烯酰氯在一定条件下反应制得:

下列有关化合物 X、Y 的说法正确的是
A.X 分子中所有原子一定共平面B.Y 分子存在顺反异构
C.可以用酸性 KMnO4 溶液鉴别 X 和 YD.X→Y 的反应为取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化合物X的叙述正确的是( )

A.X分子能发生氧化、取代、消去反应B.X分子只存在2个手性碳原子
C.X分子中含有五种官能团D.1 mol X与足量NaOH溶液反应,最多消耗3 mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com