
【题目】2009年7月27日,位于莫斯科郊外的杜布纳国际联合核研究所的专家们合成第117号新元素。下列有关117号元素叙述正确的是( )
A. 该合成过程是化学变化 B. 该元素位于第7周期ⅦA族
C. 该元素是非金属元素 D. 该元素的单质易溶于水
科目:高中化学 来源: 题型:
【题目】标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为cmol/L,则下列关系中不正确的是( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图实验装置制取乙酸乙酯。回答以下问题;

(1)在A试管中加入乙醇、乙酸和浓硫酸的顺序是_______________________________。
(2)写出A试管中发生反应的化学方程式___________________________________________
(3)B试管中所装液体应为___________,乙酸乙酯生成后,将在该溶液的______(填“上”或“下”)层,分离出该产品所需的主要仪器是_________________________________________
(4)该装置用球形干燥管代替长导管,并将干燥管的末端插入B中液面以下,在此处球形干燥管的作用有①_________________________________________________________
②_________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上曾经通过反应“3Fe + 4NaOH![]() Fe3O4+ 2H2↑+4Na↑” 生产金属钠。下列有关说法正确的是
Fe3O4+ 2H2↑+4Na↑” 生产金属钠。下列有关说法正确的是
A. 用磁铁可以将Fe与Fe3O4分离 B. 将生成的气体在空气中冷却可获得钠
C. 该反应条件下铁的氧化性比钠强 D. 每生成lmolH2,转移的电子数约为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. CaO与水反应过程中,有共价键的断裂和形成
B. H2O的热稳定性比H2S强,是由于H2O的分子间作用力较大
C. KCl、HCl、KOH的水溶液都能导电,所以它们都属于离子化合物
D. 葡萄糖、二氧化碳和足球烯(C60)都是共价化合物,它们的晶体都属于分子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中,不正确的是
A. 焰火的五彩缤纷是某些金属元素的性质的展现
B. SiO2可用于制造光导纤维,其性质稳定,不溶于强酸、强碱
C. “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化物有关
D. 根据分散质微粒直径大小可以将分散系分为溶液、胶体和浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式己配平): Cu+2H2SO4(浓)![]() CuSO4+A↑+2H2O试通过计算和推理完成下面的问题:
CuSO4+A↑+2H2O试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成,则A应该属于______(填序号)
a.电解质 b.非电解质 c.硫化物 d.酸性氧化物 e.碱性氧化物
(2)A物质可以使酸性KMnO4溶液褪色,此反应中______(填写化学式,下同)失去电子,还原产物是______。
(3)一定量的铜片与100mL18mol/L的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的CuSO4的质量为______g,发生还原反应的硫酸的物质的量为___________mol。
(4)将反应后所得到的溶液与足量Ba(OH)2溶液充分反应。请写出此过程发生的反应的离子方程式:______、_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有某铁碳合金(铁和碳两种单质的混合物),某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究。
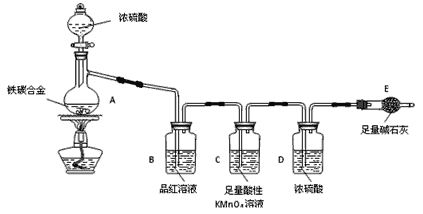
I.测定铁的质量分数:
(1)检查上述装置气密性的一种方法是:关闭分液漏斗的活塞,在E装置后面连上一根导管,然后___________________________________________________________________,则证明装置的气密性良好。
(2)称量E的质量,并将a g铁碳合金样品放入装置A中,再加入足量的浓硫酸,待A中不再逸出气体时,停止加热,拆下E并称重,E增重b g。铁碳合金中铁的质量分数为______________________(写表达式)。
(3)装置C的作用______________________________________________。s5
(4)甲同学认为,依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,原因是空气中CO2、水蒸气进入E管使b增大。你认为改进的方法是________________________________________。
(5)乙同学认为,即使甲同学认为的偏差得到改进,依据此实验测得合金中铁的质量分数也可能会偏高。你认为其中的原因是________________________________________________________。
Ⅱ.探究浓硫酸的某些性质:
(6)往A中滴加足量的浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:_______________________________________。
(7)A中铁与浓硫酸发生反应的化学方程式是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:

(1)第②步操作的目的是除去粗盐中的________________(填化学式,下同),第⑥步操作的目的是除去滤液中_______________________________。
(2)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、CaCO3、________(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com