
【题目】已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式己配平): Cu+2H2SO4(浓)![]() CuSO4+A↑+2H2O试通过计算和推理完成下面的问题:
CuSO4+A↑+2H2O试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成,则A应该属于______(填序号)
a.电解质 b.非电解质 c.硫化物 d.酸性氧化物 e.碱性氧化物
(2)A物质可以使酸性KMnO4溶液褪色,此反应中______(填写化学式,下同)失去电子,还原产物是______。
(3)一定量的铜片与100mL18mol/L的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的CuSO4的质量为______g,发生还原反应的硫酸的物质的量为___________mol。
(4)将反应后所得到的溶液与足量Ba(OH)2溶液充分反应。请写出此过程发生的反应的离子方程式:______、_____________________。
【答案】 bd SO2 MnSO4 16 0.1 SO42+Cu2++2OH-+Ba2+=BaSO4↓ +Cu(OH)2 SO42- +2H++2OH-+Ba2+=BaSO4↓ +2H2O
【解析】(1)A物质可以导致酸雨的形成,则A是二氧化硫,应该属于酸性氧化物,且SO2为非电解质,不是硫化物,故答案为bd;
(2)SO2使酸性KMnO4溶液褪色,此反应中SO2 失去电子,发生氧化反应,氧化剂是KMnO4;还原产物为MnSO4 ;
(3)一定量的铜片与100mL 18mol/L 的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,由定量关系得:Cu+2H2SO4(浓)![]() CuSO4+SO2 ↑+2H2O,电子转移2mol,就会生成1molSO2 气体和1molCuSO4,则该反应过程中转移了0.2mol电子,生成的0.1molSO2 气体,则被还原的硫酸的物质的量为0.1mol,生成的CuSO4的质量为0.1mol×160g/mol=16g;
CuSO4+SO2 ↑+2H2O,电子转移2mol,就会生成1molSO2 气体和1molCuSO4,则该反应过程中转移了0.2mol电子,生成的0.1molSO2 气体,则被还原的硫酸的物质的量为0.1mol,生成的CuSO4的质量为0.1mol×160g/mol=16g;
(4)将反应后所得到的溶液与足量Ba(OH)2溶液充分反应,此过程发生的反应的离子方程式:Ba2++SO42-+2OH-+2H+=2H2O+BaSO4↓、Ba2++SO42-+2OH-+Cu2+=Cu(OH)2↓+BaSO4↓。


科目:高中化学 来源: 题型:
【题目】在0.2L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,对于该溶液成分。下列说法不正确的是( )

A. NaCl的物质的量为0.2mol
B. 溶质MgCl2的质量为9g
C. 该混合液中BaCl2的物质的量为0.1mol
D. 将该混合液加水稀释至体积为1L,稀释后溶液中Ba2+的物质的量浓度为0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(有毒性,市场上很易与食盐混淆)是一种常见的工业用盐,广泛用于物质合成、金属表面处理等,它的用途、物理性质与NaCl极为相似。相关化学性质如图所示,下列说法不正确的是

A. NaNO2稳定性大于NH4NO2
B. NaNO2与N2H4反应中,NaNO2是氧化剂
C. 可用KI-淀粉和食醋鉴别NaNO2 和NaCl
D. 分解NaN3盐每产生1molN2转移6mole-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2009年7月27日,位于莫斯科郊外的杜布纳国际联合核研究所的专家们合成第117号新元素。下列有关117号元素叙述正确的是( )
A. 该合成过程是化学变化 B. 该元素位于第7周期ⅦA族
C. 该元素是非金属元素 D. 该元素的单质易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是 ( )
A. NaHSO4溶液中滴加Ba(OH)2溶液至SO![]() 恰好沉淀:2H++2OH-+SO
恰好沉淀:2H++2OH-+SO![]() +Ba2+===BaSO4↓+2H2O
+Ba2+===BaSO4↓+2H2O
B. NaHSO4溶液中滴加Ba(OH)2溶液至溶液呈中性:H++OH-+SO![]() +Ba2+===BaSO4↓+H2O
+Ba2+===BaSO4↓+H2O
C. 将Na投入到CuSO4溶液中: 2Na+Cu2+===2Na++Cu
D. KAl(SO4)2溶液与少量Ba(OH)2溶液反应3Ba2++6OH-+3SO![]() +2Al3+===2Al(OH)3↓+3BaSO4↓
+2Al3+===2Al(OH)3↓+3BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A—B键的键能。下表列出了一些化学键的键能E:
化学键 | H—H | Cl—Cl | O===O | C—Cl | C—H | O—H | H—Cl |
E/kJ·mol-1 | 436 | 247 | x | 330 | 413 | 463 | 431 |
请回答下列问题:
(1)如图表示某反应的能量变化关系,则此反应为 (填“吸热”或“放热”)反应,其中ΔH=
(用含有a、b的关系式表示)。
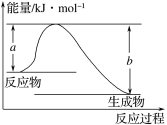
(2)若图示中表示反应H2(g)+![]() O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,则b= kJ·mol-1,x= 。
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,则b= kJ·mol-1,x= 。
(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃利用空气中的氧气跟氯化氢反应制氯气。反应的化学方程式为 。若忽略温度和压强对反应热的影响,根据上题中的有关数据,计算当反应中有1 mol电子转移时,反应的热量变化为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色透明的酸性溶液中,能大量共存的离子组是( )
A. Na+、K+、HCO3-、NO3- B. NH4+、A13+、SO42-、NO3-
C. K+、SO32-、NH4+、NO3- D. NH4+、Na+、NO3-、SiO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请完成下列问题
(1)写出由甲苯制备三硝基甲苯的化学方程式:________。
(2)某有机物分子式是C3H2O2,它的水溶液显酸性且能使溴水褪色,该有机物的结构简式为________。
(3)![]() 分子结构中最多有________个原子共面。
分子结构中最多有________个原子共面。
(4)有下列几种反应类型:①消去②取代③氧化④加成⑤还原⑥水解,用丙醛制取1,2-丙二醇,正确的合成路线依次发生的反应所属类型不可能是________。
A.⑤①④⑥B.④①④②C.⑤①④②D.⑤③⑥①
(5)化合物A分子式为C5H8,它是合成天然橡胶的单体,则由A合成的天然橡胶的顺式结构简式为________。
(6)聚碳酸酯 的透光率良好,可制作车、船、飞机的挡风玻璃,以及眼镜镜片、光盘、唱片等。合成聚碳酸酯是用绿色化学原料碳酸二甲酯(
的透光率良好,可制作车、船、飞机的挡风玻璃,以及眼镜镜片、光盘、唱片等。合成聚碳酸酯是用绿色化学原料碳酸二甲酯( )与________(写出该有机物的结构简式)缩合聚合而成。
)与________(写出该有机物的结构简式)缩合聚合而成。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】长期食用增塑剂超标的食品会对人体健康产生较大影响。邻苯二甲酸二丁酯(C16H22O4)是一种常见的增塑剂,它属于( )
A. 单质 B. 氧化物 C. 有机物 D. 无机物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com