
【题目】在无色透明的酸性溶液中,能大量共存的离子组是( )
A. Na+、K+、HCO3-、NO3- B. NH4+、A13+、SO42-、NO3-
C. K+、SO32-、NH4+、NO3- D. NH4+、Na+、NO3-、SiO32-
科目:高中化学 来源: 题型:
【题目】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。已知:p(Ba2+) = -lgc(Ba2+ ),p(SO42-)=-lgc(SO42-).下列说法正确的是( )

A. 该温度下,Ksp( BaS04) =1.0xl0-24
B. a 点的 Ksp(BaS04)小于 b 点的 Ksp(BaSO4)
C. d点表示的是该温度下BaS04的不饱和溶液
D. 加入BaCl2可以使溶液由c点变到a点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. CaO与水反应过程中,有共价键的断裂和形成
B. H2O的热稳定性比H2S强,是由于H2O的分子间作用力较大
C. KCl、HCl、KOH的水溶液都能导电,所以它们都属于离子化合物
D. 葡萄糖、二氧化碳和足球烯(C60)都是共价化合物,它们的晶体都属于分子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式己配平): Cu+2H2SO4(浓)![]() CuSO4+A↑+2H2O试通过计算和推理完成下面的问题:
CuSO4+A↑+2H2O试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成,则A应该属于______(填序号)
a.电解质 b.非电解质 c.硫化物 d.酸性氧化物 e.碱性氧化物
(2)A物质可以使酸性KMnO4溶液褪色,此反应中______(填写化学式,下同)失去电子,还原产物是______。
(3)一定量的铜片与100mL18mol/L的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的CuSO4的质量为______g,发生还原反应的硫酸的物质的量为___________mol。
(4)将反应后所得到的溶液与足量Ba(OH)2溶液充分反应。请写出此过程发生的反应的离子方程式:______、_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表代表周期表中的几种短周期元素,下列说法中错误的是( )

A. ED4分子中各原子均达8电子结构
B. AD3和ED4两分子的中心原子均为sp3杂化
C. A、B、C第一电离能的大小顺序为C>B>A
D. C、D气态氢化物稳定性强弱和沸点高低均为C>D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有某铁碳合金(铁和碳两种单质的混合物),某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究。
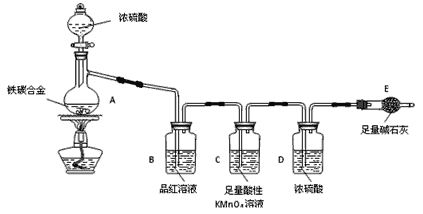
I.测定铁的质量分数:
(1)检查上述装置气密性的一种方法是:关闭分液漏斗的活塞,在E装置后面连上一根导管,然后___________________________________________________________________,则证明装置的气密性良好。
(2)称量E的质量,并将a g铁碳合金样品放入装置A中,再加入足量的浓硫酸,待A中不再逸出气体时,停止加热,拆下E并称重,E增重b g。铁碳合金中铁的质量分数为______________________(写表达式)。
(3)装置C的作用______________________________________________。s5
(4)甲同学认为,依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,原因是空气中CO2、水蒸气进入E管使b增大。你认为改进的方法是________________________________________。
(5)乙同学认为,即使甲同学认为的偏差得到改进,依据此实验测得合金中铁的质量分数也可能会偏高。你认为其中的原因是________________________________________________________。
Ⅱ.探究浓硫酸的某些性质:
(6)往A中滴加足量的浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:_______________________________________。
(7)A中铁与浓硫酸发生反应的化学方程式是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡椒酚是植物挥发油中的一种成分。关于胡椒酚的下列说法,其中正确的是

①该化合物属于芳香烃;
②分子中至少有7个碳原子处于同一平面;
③它的部分同分异构体能发生银镜反应;
④1mol该化合物最多可与2molBr2发生反应。
A. ①③ B. ①②④ C. ②③ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数值,下列说法正确的是
A. 室温下,21.0g 乙烯与丙烯的混合气体中含有的碳原子数为1.5NA
B. 常温常压下,0.1molC8H18所含有的共价键数目为2.0 NA
C. 0.1mol乙醇与氧气完全反应生成二氧化碳时转移电子数为0.1NA
D. 标准状况下,2.24L乙酸乙酯中所含氧原子数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com