
【题目】电子工业常用30%的FeCl3溶液腐蚀镀在绝缘板上的铜箔,制造印刷电路板。
(1)写出FeCl3溶液与金属铜发生反应的离子方程式:_________________________。
(2)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备用如图所示步骤:
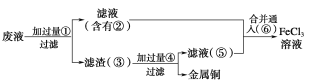
A.写出上述实验中加入或生成的有关物质的化学式:
①________;②________;③________;④________;⑤________;⑥________。
B.写出下列过程中的离子方程式:
①→②___________________________________;
⑤+⑥_______________________________________________________。
【答案】2Fe3++Cu=2Fe2++Cu2+ Fe FeCl2 Fe、Cu HCl FeCl2 Cl2 Cu2++Fe=Fe2++Cu、Fe+2Fe3+=3Fe2+ 2Fe2++Cl2=2Fe3++2Cl-
【解析】
由工艺流程可知,滤渣③中含有金属铜,目的是制取氯化铁,废液应该与过量的Fe反应,故①Fe;滤液②中含有FeCl2,通入⑥氯气可以得到氯化铁;滤渣③中含有金属Cu、未反应的Fe,加入④盐酸,过滤,回收铜,滤液⑤中含有FeCl2,据此解答。
(1)铜与氯化铁反应生成氯化铜、氯化亚铁,反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+;
(2)由工艺流程可知,滤渣③中含有金属铜,目的是制取氯化铁,废液应该与过量的Fe反应,故①Fe;滤液②中含有FeCl2,通入⑥氯气可以得到氯化铁;滤渣③中含有金属Cu、未反应的Fe,加入④盐酸,过滤,回收铜,滤液⑤中含有FeCl2,则
A.根据以上分析可知①~⑥分别是Fe、FeCl2、Fe和Cu、HCl、FeCl2、Cl2;
B.废液加入过量铁和铁离子反应生成亚铁离子,和铜离子反应生成铜,反应的离子方程式Cu2++Fe=Fe2++Cu、Fe+2Fe3+=3Fe2+;
滤液无语中含有FeCl2,通入氯气可以得到氯化铁,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-。


科目:高中化学 来源: 题型:
【题目】已知A是一种常见金属,F是一种红褐色沉淀。试根据图中转化关系,回答下列问题。

(1)写出A、C、F、G的化学式:A________;C________;F________;G________。
(2)保存C溶液时要加固体A的原因是______________________。
(3)写出下列转化的离子方程式。
①D→C:___________________________________________________;
②C→D:___________________________________________________;
③B→C+D__________________________________________________。
(4)写出E→F的化学方程式:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一个电化学过程的示意图,回答下列问题:

(1)甲池是___________(填“原电池”、“电解池”或“电镀池”)装置,乙装置中电极A的名称是_______(填“正极”、“负极”、“阴极”或“阳极”)。
(2)甲装置中通入CH4的电极反应式为__________________________________,乙装置中电极B(Ag)的电极反应式为________________________________,丙装置中D极的产物是____________(写化学式)。
(3)一段时间,当丙池中产生112 mL(标准状况)气体时,均匀搅拌丙池,所得溶液在25 ℃时的pH=________(已知:NaCl溶液足量,电解后溶液体积为500 mL)。若要使丙池恢复电解前的状态,应向丙池中通入________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种药物合成中间体的结构简式为 ,下列有关该物质的说法不正确的是( )
,下列有关该物质的说法不正确的是( )
A. 属于芳香族化合物
B. 能发生消去反应、还原反应和酯化反应,不能发生水解反应
C. 1 mol该有机物与足量Na2CO3溶液反应,消耗2.5 mol Na2CO3
D. 能分别与金属Na、NaOH溶液、NaHCO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有下列7种有机物:
①CH4 ②![]() ③
③ ④
④ ⑤
⑤ ⑥
⑥![]() ⑦
⑦
请回答:其中属于醇类的是________(填序号,下同),互为同系物的是_______,能与金属钠反应的有_________,互为同分异构体的是________。
(2)肉桂酸甲酯由C、H、O三种元素组成,已知其相对分子质量为162,核磁共振氢谱显示有6个峰,其面积之比为1︰2︰2︰1︰1︰3 ,利用红外光谱仪检测其中的某些基团,测得红外光谱如下图,则肉桂酸甲酯的结构简式是 ____________________(不考虑立体异构)。

(3)写出2-甲基-2-丁烯的结构简式:____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁铝合金投入400 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。
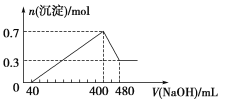
计算:
(1)合金中Mg的质量为________g;
(2)硫酸的物质的量浓度为________ mol·L1;
(3)NaOH溶液的物质的量浓度为________ mol·L1;
(4)生成H2在标准状况下的体积为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸锰可用于制造钠离子电池的负极材料。可用如下反应制得乙酸锰:4Mn(NO3)2·6H2O+26(CH3CO)2O =4(CH3COO)3Mn +8HNO2+ 3O2↑+40CH3COOH
(1)Mn3+基态核外电子排布式为______。
(2)NO中氮原子轨道的杂化类型是______。
(3)与HNO2互为等电子体的一种阴离子的化学式为______。
(4)配合物[Mn(CH3OH)6]2+中提供孤对电子的原子是______。
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有______。
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《化学与生活》
(1) 2017年10月22日,沪通长江大桥天生港航道桥主拱结构成功合龙。
①桥墩建造需要用到大量水泥。生产水泥的主要原料为黏土和____(填字母)。
a. 纯碱 b. 石灰石 c. 食盐

②氯丁橡胶作为桥梁支座,其作用是将桥跨结构上的荷载传递给墩台。氯丁橡胶属于____(填字母)。
a. 无机非金属材料
b. 金属材料
c. 有机高分子材料
③桥梁建造需要使用大量钢材,其中预埋钢板及上、下钢板均采用镀锌钢板,钢板镀锌的主要目的是____(填字母)。
a. 美化桥梁 b. 提高硬度 c. 提高耐腐蚀性
(2)洋蓟被人们冠以“蔬菜之皇”的美称,含有脂肪、蛋白质、糖类、维生素A、维生素C和丰富的钙、磷、铁等元素,其中:

①属于脂溶性维生素的是____。
②属于人体所需微量元素的是____。
③脂肪在人体内水解生成高级脂肪酸和____;糖类在人体中水解生成葡萄糖,写出葡萄糖在人体内氧化的化学方程式: ____。
(3)合理利用自然资源,防止环境污染和生态破坏。
①向燃煤中加入适量石灰石,可大大减少______的排放。煤的气化是实现能源清洁化的重要途径,水煤气的主要成分是CO和______。
②明矾是一种常用的混凝剂,其净水原理是___________(用离子方程式表示)。
③我国科学家证明了黄粉虫的幼虫可降解聚苯乙烯(![]() )这类难以自然降解的塑料。请写出由苯乙烯合成聚苯乙烯的化学方程式:________________。防治废塑料制品造成的白色污染,还可以采用的方法有:__________(任写一种)。
)这类难以自然降解的塑料。请写出由苯乙烯合成聚苯乙烯的化学方程式:________________。防治废塑料制品造成的白色污染,还可以采用的方法有:__________(任写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫的氧化物是形成酸雨的罪魁祸首,含硫烟气(主要成分为SO2)的处理备受关注,主要有以下两种方法。请回答下列问题:
Ⅰ.碱液吸收法
步骤1:用足量氨水吸收SO2。
步骤2:再加入熟石灰,发生反应2NH+Ca2++2OH-+SO![]() ===CaSO3↓+2NH3·H2O。
===CaSO3↓+2NH3·H2O。
(1)已知:25 ℃时,Kb(NH3·H2O)=a;Ksp(CaSO3)=b。该温度下,步骤2中反应的平衡常数K=__________(用含a、b的代数式表示)。
Ⅱ.水煤气还原法
已知:ⅰ.2CO(g)+SO2(g) ![]() S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1
S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1
ⅱ.2H2(g)+SO2(g) ![]() S(l)+2H2O(g) ΔH2=+45.4 kJ·mol-1
S(l)+2H2O(g) ΔH2=+45.4 kJ·mol-1
(2)写出CO(g)与H2O(g)反应生成CO2(g) 、H2(g)的热化学方程式为_______________。
若该反应在绝热、恒容体系中进行,达到平衡的标志___________。
A.氢氧键的断裂速率等于氢氢键的断裂速率
B.混合气体的平均摩尔质量保持不变
C.混合气体的总压强保持不变
D. H2O(g) 与H2(g)的体积比保持不变
(3)反应ⅱ的正反应的活化能E________(填“>”“<”或“=”)ΔH2。
(4)在一定压强下,发生反应ⅱ。平衡时,α(SO2) (二氧化硫的转化率)与原料气投料比[![]() ]和温度(T)的关系如图所示。
]和温度(T)的关系如图所示。

①α(H2):M________(填“>”“<”或“=”)N。
②逆反应速率:M________(填“>”“<”或“=”)Q。
(5)T ℃,向10 L恒容密闭容器中充入2 mol CO(g)、2 mol SO2(g)和2 mol H2(g),发生反应ⅰ和反应ⅱ。5 min达到平衡时,CO2(g)和H2O(g)的物质的量分别为1.6 mol、1.8 mol。
①该温度下,反应ⅱ的平衡常数K=________。
②其他条件不变,6 min时缩小容器容积。α(SO2)__________(填“增大”“减小”或“不变”),原因为_____________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com