
【题目】《化学与生活》
(1) 2017年10月22日,沪通长江大桥天生港航道桥主拱结构成功合龙。
①桥墩建造需要用到大量水泥。生产水泥的主要原料为黏土和____(填字母)。
a. 纯碱 b. 石灰石 c. 食盐

②氯丁橡胶作为桥梁支座,其作用是将桥跨结构上的荷载传递给墩台。氯丁橡胶属于____(填字母)。
a. 无机非金属材料
b. 金属材料
c. 有机高分子材料
③桥梁建造需要使用大量钢材,其中预埋钢板及上、下钢板均采用镀锌钢板,钢板镀锌的主要目的是____(填字母)。
a. 美化桥梁 b. 提高硬度 c. 提高耐腐蚀性
(2)洋蓟被人们冠以“蔬菜之皇”的美称,含有脂肪、蛋白质、糖类、维生素A、维生素C和丰富的钙、磷、铁等元素,其中:

①属于脂溶性维生素的是____。
②属于人体所需微量元素的是____。
③脂肪在人体内水解生成高级脂肪酸和____;糖类在人体中水解生成葡萄糖,写出葡萄糖在人体内氧化的化学方程式: ____。
(3)合理利用自然资源,防止环境污染和生态破坏。
①向燃煤中加入适量石灰石,可大大减少______的排放。煤的气化是实现能源清洁化的重要途径,水煤气的主要成分是CO和______。
②明矾是一种常用的混凝剂,其净水原理是___________(用离子方程式表示)。
③我国科学家证明了黄粉虫的幼虫可降解聚苯乙烯(![]() )这类难以自然降解的塑料。请写出由苯乙烯合成聚苯乙烯的化学方程式:________________。防治废塑料制品造成的白色污染,还可以采用的方法有:__________(任写一种)。
)这类难以自然降解的塑料。请写出由苯乙烯合成聚苯乙烯的化学方程式:________________。防治废塑料制品造成的白色污染,还可以采用的方法有:__________(任写一种)。
【答案】 b c c 维生素A Fe 甘油 C6H12O6+6O2![]() 6CO2+6H2O SO2 H2 Al3++3H2O
6CO2+6H2O SO2 H2 Al3++3H2O![]() Al(OH)3(胶体)+3H+ n
Al(OH)3(胶体)+3H+ n![]()
![]()
![]() 减少使用;循环利用;重复利用;寻找替代品(任写一种)
减少使用;循环利用;重复利用;寻找替代品(任写一种)
【解析】(1)①生产水泥的主要原料为黏土和石灰石,答案选b;②氯丁橡胶属于有机高分子材料,答案选c;③锌的金属性强于铁,钢板镀锌的主要目的是提高耐腐蚀性,答案选c;(2) ①属于脂溶性维生素的是维生素A;②属于人体所需微量元素的是Fe;③脂肪在人体内水解生成高级脂肪酸和甘油;葡萄糖在人体内氧化的化学方程式为: C6H12O6+6O2![]() 6CO2+6H2O;(3)①向燃煤中加入适量石灰石,可大大减少SO2的排放。煤的气化是实现能源清洁化的重要途径,水煤气的主要成分是CO和H2;②明矾是一种常用的混凝剂,其净水原理是Al3++3H2O
6CO2+6H2O;(3)①向燃煤中加入适量石灰石,可大大减少SO2的排放。煤的气化是实现能源清洁化的重要途径,水煤气的主要成分是CO和H2;②明矾是一种常用的混凝剂,其净水原理是Al3++3H2O![]() Al(OH)3(胶体)+3H+;③苯乙烯发生加聚反应生成聚苯乙烯,反应的化学方程式为: n
Al(OH)3(胶体)+3H+;③苯乙烯发生加聚反应生成聚苯乙烯,反应的化学方程式为: n![]()
![]()
![]() ;防治废塑料制品造成的白色污染,还可以采用的方法有: 减少使用;循环利用;重复利用;寻找替代品。
;防治废塑料制品造成的白色污染,还可以采用的方法有: 减少使用;循环利用;重复利用;寻找替代品。


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】硝酸是一种重要的化工原料,工业上采用氨的催化氧化法制备硝酸。
(1) 已知反应N2(g)+3H2(g) 2NH3(g)为放热反应,在恒容容器中能说明该反应达到平衡状态的是(_______)
A.容器内N2、H2、NH3的浓度之比为1:2:3
B. v正(N2)=v逆(H2)
C.容器内压强保持不变
D.混合气体的密度保持不变
(2)理论上,为了增大平衡时的转化率,可采取的措施是_____________(要求答出两点)
⑶合成氨技术的创立开辟了人工固氮的重要途径,合成氨反应的平衡常数K值和温度的关系如下表,则400℃时,测得某时刻氮气、氢气、氨气的物质的量浓度分别为1 mol·L-1、2 mol·L-1、3 mol·L-1时,此时刻该反应正反应速率_____ 逆反应速率(填“大于”、“小于”或“等于”)
温度/℃ | 200 | 300 | 400 |
K | 1.0 | 0.86 | 0.5 |
(4)消除硝酸工厂尾气的一种方法是用甲烷催化还原氮氧化物,已知:
① CH4 (g)+2O2(g)=CO2(g)+2H2O(g) △ H=-890.3 kJ·mol-1
② N2(g)+2O2(g)=2NO2(g) △ H=-67.0 kJ·mol-1
则CH4(g)将NO2(g)还原为N2(g)等的热化学方程式为___________________________________________
(5)在25 ℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成____沉淀(填化学式),当两种沉淀共存时,溶液中C(Mg2+)/C(Cu2+)=_________(已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业常用30%的FeCl3溶液腐蚀镀在绝缘板上的铜箔,制造印刷电路板。
(1)写出FeCl3溶液与金属铜发生反应的离子方程式:_________________________。
(2)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备用如图所示步骤:
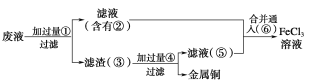
A.写出上述实验中加入或生成的有关物质的化学式:
①________;②________;③________;④________;⑤________;⑥________。
B.写出下列过程中的离子方程式:
①→②___________________________________;
⑤+⑥_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如何防止铁的锈蚀是工业上研究的重点内容。为研究铁的锈蚀,某同学做了探究实验,如下图所示,铁处于①②③三种不同的环境中

请回答:
(1)金属腐蚀主要分为__________腐蚀和_____________腐蚀两种。
(2)铁被腐蚀的速率由快到慢的顺序是_________________(填序号)。
(3)①中正极的电极反应式为_________________________________________________,②中负极的电极反应式为_________________________________________。
(4)据资料显示,全世界每年因腐蚀而报废的金属材料相当于其年产量的20%以上。为防护金属被腐蚀可采取的措施有__________(填序号)。
①健身器材刷油漆 ②自行车钢圈镀铬
③将钢管用导线与铜条连接 ④将钢管用导线与碳棒连接
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如下图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )

A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性:X>W>Z
C. 最简单气态氢化物的热稳定性:Y>X>W>Z
D. 元素X、Z、W的最高化合价分别与其主族序数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示。常温下,B、E呈气态,其中B呈黄绿色。D是最常见的无色液体,E常用作制冷剂,F是一种不溶于水的碱,G是厨房中的常见调味品,H由两种元素组成,其摩尔质量为32 g·mol-1。

(1) E的电子式为____。
(2) H的化学式为____。
(3) 写出反应①的离子方程式:_________________。
(4) 写出反应②的化学方程式:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法不正确的是( )
A. 除去乙酸乙酯中混有的乙酸,可以用饱和碳酸钠溶液
B. 顺-2-丁烯与反-2-丁烯与氢气加成的产物不相同
C. 聚合物![]() 可由单体CH3CH=CH2和CH2=CH2加聚制得
可由单体CH3CH=CH2和CH2=CH2加聚制得
D. C3H2Cl6有4种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、社会发展息息相关,下列有关说法正确的是
A. “冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”。 “薪柴之灰”与铵态氮肥混合施用可增强肥效。
B. 玻璃和压电陶瓷都属于新型无机非金属材料。
C. 侯德榜制碱法的原理是在饱和食盐水中先通二氧化碳后通氨气制得碳酸钠。
D. 高铁酸钾(K2FeO4)在水处理过程中涉及的变化过程有:蛋白质的变性、胶体吸附、盐类水解、氧化还原反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微型纽扣电池在现代生活中应用广泛。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,总反应是Zn+Ag2O=ZnO+2Ag。请回答下列问题。
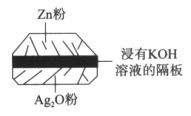
(1)该电池属于__________电池(填“一次”或“二次”)。
(2)负极是_________,电极反应式是____________。
(3)使用时,负极区的pH_______(填“增大”、“减小”或“不变”,下同),电解质溶液的pH__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com