
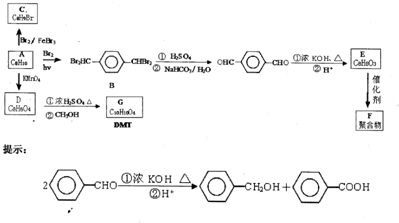
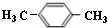
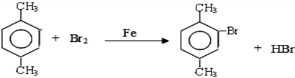
 ,A和溴发生取代反应生成C,根据C的分子式知,C的结构简式为
,A和溴发生取代反应生成C,根据C的分子式知,C的结构简式为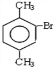 ,A被酸性高锰酸钾氧化生成D对二苯甲酸,其结构简式为
,A被酸性高锰酸钾氧化生成D对二苯甲酸,其结构简式为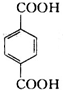 ,D和甲醇发生置换反应生成G,G的结构简式为
,D和甲醇发生置换反应生成G,G的结构简式为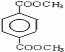 ,对二苯甲醛和浓KOH溶液然后酸化得到E,根据E的分子式知,E的结构简式为
,对二苯甲醛和浓KOH溶液然后酸化得到E,根据E的分子式知,E的结构简式为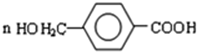 ,E发生缩聚反应生成F,F的结构简式为
,E发生缩聚反应生成F,F的结构简式为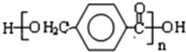 ,再结合题目分析解答.
,再结合题目分析解答. ,A和溴发生取代反应生成C,根据C的分子式知,C的结构简式为
,A和溴发生取代反应生成C,根据C的分子式知,C的结构简式为 ,A被酸性高锰酸钾氧化生成D对二苯甲酸,其结构简式为
,A被酸性高锰酸钾氧化生成D对二苯甲酸,其结构简式为 ,D和甲醇发生置换反应生成G,G的结构简式为
,D和甲醇发生置换反应生成G,G的结构简式为 ,对二苯甲醛和浓KOH溶液然后酸化得到E,根据E的分子式知,E的结构简式为
,对二苯甲醛和浓KOH溶液然后酸化得到E,根据E的分子式知,E的结构简式为 ,E发生缩聚反应生成F,F的结构简式为
,E发生缩聚反应生成F,F的结构简式为 ,
, ,故答案为:取代反应;
,故答案为:取代反应; ;
; ,
, ;
;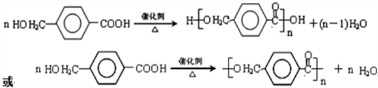 ,故答案为:
,故答案为: ;
; ,芳香化合物H是E的同分异构体,则H中含有苯环,H分子中含有酯基和醚键两种官能团,同时能发生银镜反应,说明为甲酯基,符合条件的H结构简式有
,芳香化合物H是E的同分异构体,则H中含有苯环,H分子中含有酯基和醚键两种官能团,同时能发生银镜反应,说明为甲酯基,符合条件的H结构简式有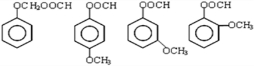 ,
, .
.


科目:高中化学 来源: 题型:
| A、钠和水反应 Na+H2O═Na++OH-+H2↑ |
| B、Cl2与KBr溶液反应 Cl2+2Br-═2Cl-+Br2 |
| C、氯气与NaOH溶液反应 Cl2+OH-═Cl-+ClO-+H2O |
| D、盐酸与石灰石反应 CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
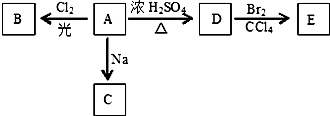
查看答案和解析>>
科目:高中化学 来源: 题型:

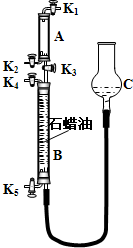
查看答案和解析>>
科目:高中化学 来源: 题型:
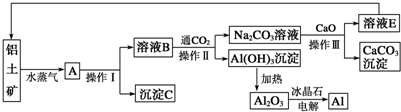
| ||
| 通电,Na3AlF6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+ |
| B、Al3+ |
| C、Fe2+ |
| D、Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
| 原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 | 0.089 |
| 主要化合价 | +1 | +2 | +1 | +3 | +5、-3 | +7、-1 | +5、-3 | -2 | +2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 X、Y、Z、W四种常见元素,且均为短周期元素.已知:①X的最高价氧化物对应的水化物为无机酸中最强酸 ②Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料 ③Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料 ④W被称为军事金属,可在CO2中燃烧.
X、Y、Z、W四种常见元素,且均为短周期元素.已知:①X的最高价氧化物对应的水化物为无机酸中最强酸 ②Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料 ③Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料 ④W被称为军事金属,可在CO2中燃烧.| 氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 成分 | 质量(g) | 摩尔质量(g?mol-1) |
| 蔗糖 | 68.4 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com