
请回答下列问题:
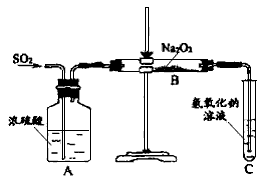
(1)第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是:_____________
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3。
_________________________________
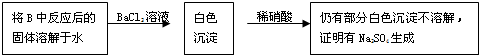
(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否有
Na2SO4生成,他们设计了如下方案:

科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:

| 碱石灰的 可能组成 |
NaOH、CaO | NaOH、CaO、 Ca (OH)2 |
NaOH、 Ca (OH)2 |
NaOH、 Ca (OH)2、H2O |
| n (Na+)、n (Ca2+) 的关系 |
40x+56y=4 | 40x+56y<4.0<40x+74y 40x+56y<4.0<40x+74y |
40x+74y=4.0 40x+74y=4.0 |
40x+74y<4.0 40x+74y<4.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
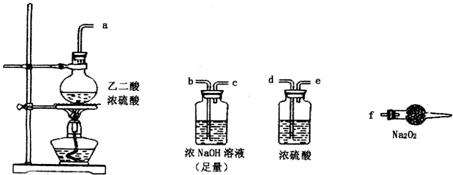
 有两个实验小组的同学探究一氧化碳、二氧化硫与过氧化钠的反应.请回答下列问题:
有两个实验小组的同学探究一氧化碳、二氧化硫与过氧化钠的反应.请回答下列问题:
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
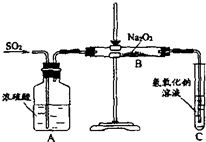
有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如下图所示的装置进行实验。通入SO2气体,将带余烬的木条插入试管C中,木条复燃。
请回答下列问题:
(1)第1小组同学认为Na2O2与SO2反应生成Na2SO3和O2,该反应的化学方程式是:___________________。
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3:__________。
(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否有Na2SO4生成,他们设计了如下方案: 0
0
上述方案是否合理?_________,请简要说明两点理由:①________________,②__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com