
����Ŀ��ij��ѧ��ȤС��ȡһ�����Ĺ���������Һ��ȷ�ⶨ�˹�������ĺ�������̽���˹�����������ʡ�����д���пհף�
�����ⶨ��������ĺ���
��1����ȡ10��00 mL�ܶ�Ϊ�� g/mL�Ĺ���������Һ��250 mL_______�����������ƣ��У���ˮϡ�����̶ȣ�ҡ�ȡ���ȡϡ�ͺ�Ĺ���������Һ25��00 mL����ƿ�У�����ϡ�����ữ��������ˮϡ�ͣ�������������
��2���ø�����ر���Һ�ζ������������䷴Ӧ�����ӷ���ʽΪ________��
��3���жϵζ������յ��������_________________________��
��4���ظ��ζ����Σ�ƽ������c mol/L KMnO4����ҺV mL����ԭ����������Һ�й����������������Ϊ____________��
��5�����ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ����ⶨ���_________������ƫ��������ƫ������������������
����̽���������������
�û�ѧ��ȤС��������ṩ��ʵ���������������ʵ�飬�ֱ�֤���˹�������������ԺͲ��ȶ��ԡ���ʵ���������Լ�ֻ�й���������Һ����ˮ���⻯�ص�����Һ������������Һ��ʵ����������Ʒ����ѡ����
�뽫���ǵ�ʵ�鷽����ʵ�����������±���
ʵ������ | ʵ�鷽�� | ʵ������ |
��֤������ | ____________ | ____________ |
��֤���ȶ��� | ____________ | ____________ |
���𰸡�250mL����ƿ 2MnO4-+ 5H2O2+ 6H+= 2Mn2++ 8H2O+ 5O2�� ����һ�θ��������Һ����Һ��dz��ɫ����30���ڲ���ɫ ![]() ƫ�� ȡ��������������Һ���Թ��У��������������Һ��ȡ�����⻯�ص�����Һ���Թ��У��������������Һ�� ��������ɫ��������Һ����ǣ���Һ����ɫ�� ȡ��������������Һ���Թ��У����ȣ��ô����ǵ�ľ�����飨ȡ��������������Һ���Թ��У����ȣ��õ����ܽ��õ�������ͨ�뵽װ�б���������Һ���Թ��У� �������ݣ�ľ����ȼ����Һ����ǻ���dz��ɫ����������
ƫ�� ȡ��������������Һ���Թ��У��������������Һ��ȡ�����⻯�ص�����Һ���Թ��У��������������Һ�� ��������ɫ��������Һ����ǣ���Һ����ɫ�� ȡ��������������Һ���Թ��У����ȣ��ô����ǵ�ľ�����飨ȡ��������������Һ���Թ��У����ȣ��õ����ܽ��õ�������ͨ�뵽װ�б���������Һ���Թ��У� �������ݣ�ľ����ȼ����Һ����ǻ���dz��ɫ����������
��������
������1������һ�����һ��Ũ�ȵ���ҺҪ������ƿ������Ҫʹ��250 mL��Һ������Ҫʹ��250 mL����ƿ��
��2�����������Һ��ǿ�������ԣ�˫��ˮ�л�ԭ�ԣ�����Ϸ���������ԭ��Ӧ�����ݵ����غ㼰ԭ���غ�ɵø÷�Ӧ�����ӷ���ʽΪ2MnO4-+ 5H2O2+ 6H+= 2Mn2++ 8H2O+ 5O2����
��3�����������Һ����ɫ�ģ����䷢����Ӧ�������Mn2+����ɫ�ģ���˵���������ǡ�÷�Ӧ��ȫʱ�ټ��������أ�����Һ������ɫ��Ϊdz��ɫ�������жϵζ������յ�������ǵ���һ�θ��������Һ����Һ��dz��ɫ����30���ڲ���ɫ��
��4��n(KMnO4)=cV��10-3mol����n(H2O2)=5/2n(KMnO4)=5cV��10-3/2mol����ԭ����������Һ�й����������������Ϊ10��(5cV��10-3/2��34g/mol)��(10��00 mL����g/mL)= ![]() ��
��
��5�����ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ������������Һ�����ƫ���մ����ݼ���Ĺ��������������ƫ�࣬ʹ�ⶨ���ƫ�ߣ�
������֤H2O2�����Եķ�����ȡ��������������Һ���Թ��У��������������Һ��ȡ�����⻯�ص�����Һ���Թ��У��������������Һ������������ɫ��������Һ����ǣ���Һ����ɫ������֤��H2O2�������ԣ���֤H2O2���ȶ��Եķ�����ȡ��������������Һ���Թ��У����ȣ��ô����ǵ�ľ�����飨ȡ��������������Һ���Թ��У����ȣ��õ����ܽ��õ�������ͨ�뵽װ�б���������Һ���Թ��У������������ݣ�ľ����ȼ����Һ����ǻ���dz��ɫ��������������֤����H2O2���ȶ��ԡ�


 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���й��ĸ����������ڹ������ȵ�λ��
�ٸ�������������о۰���������ĭ���۰�������____������ĸ����
a���������� b�����ǽ������� c���л��߷��Ӳ���
�ڸ�����Ϣ����ϵͳ��ʹ���˹��ά�����ά����Ҫ�ɷ���____������ĸ����
a��ͭ b��ʯī c����������
�۸�������������ô���ˮ�ࡣ����ˮ�����Ҫԭ��Ϊ�����____������ĸ����
a��ʯ��ʯ b������ c������
��2��Ӫ���������������彡����
���������ṩ��������ҪӪ������Ϊ____������͵����ʡ�������������ˮ������ղ�����____��
��ά������������Ҫ��Ӫ�����ʡ���ͼΪijƷ��ά����C����Ƭ˵����IJ������ݡ�������Ƭ�����ӵ���ɫ����____����ζ����___������Ƭ����ˮʱ������������Ч�������������ӵľ�ʯ���___��Ӧ�ͷų������塣

��3��ú̿���ҹ���Դ�ṹ��ռ����Ҫ��λ������ʹ�����������ɳ�����չ��
�ٿ���ȼú������SO2�ŷţ��ܹ�����____��������γɡ�ȼú�ŷŵ������л�����������Ⱦ����о�һ�֣�_____��
��ȼú������CO2��NH3�������������ֻ�����Ʒ���ð�ˮ����CO2���Ƶ�̼泥�NH4HCO3����д���÷�Ӧ�Ļ�ѧ����ʽ_____����Һ����CO2��Ӧ���Ʊ�����[CO(NH2)2]�����غ�̼������ֵ����У���Ԫ�ص����������ϸߵ���_____��
��ú��������Һ����ʵ����Դ������Ҫ;����ˮú����CO��H2�ڼ��ȡ���ѹ�ʹ������������¿��Ժϳ�Һ��ȼ�ϣ�CH3OH�����÷�Ӧ�Ļ�ѧ����ʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1.0mol��L -1NaOH��Һ�к�ijŨ��������Һʱ����pH������NaOH��Һ�����(V)��ϵ����ͼ��ʾ����ԭ������Һ�����ʵ���Ũ�Ⱥ�ǡ����ȫ��Ӧ����Һ��������ֱ���(�����Ϻ����Ϊ�������֮��)
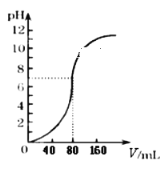
A. 0.5mol��L-1 80mLB. 0.5mol��L-1 160mL
C. 1.0mol��L-1 80mLD. 1.0mol��L-1 160mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(Ca3N2)��������һ����ɫ��ĩ���ڿ�������������ˮ�ᷢ��ˮ�⣬�����������Ʋ��ų�����ij��ѧ��ȤС������Ʊ������Ƶ�ʵ�����£�
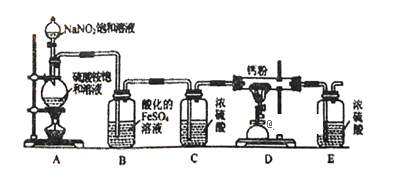
���������Ƶ��Ʊ�
��1������װ�ú������װ�������Եķ�����_______________________________________��
��2��װ��A��ÿ���ɱ�״����4.48LN2��ת�Ƶĵ�����Ϊ___________________��
��3��װ��B��������������������B�з�����Ӧ�����ӷ���ʽΪ______________________��װ��E��������______________________��
��4��ʵ�鲽�����£����װ�������Ժ�װ��ҩƷ��_____________________(�밴��ȷ��˳���������в���Ĵ���)��
����ȼD���ľƾ���ƣ� ����Һ©������; ����ȼA���ľƾ��ƣ� ��ͣ�ϵ�ȼA���ľƾ��ƣ���ֹͣ��ȼD���ľƾ����
��5�����û�ѧ����ȷ���������к���δ��Ӧ�ĸƣ�д��ʵ�����������_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��SO2 ͨ�� BaCl2 ��Һ�в���������������ͨ����һ���������Բ�����ɫ��������ͼ���Ҳ� Y �ι��з��õ�ҩƷ��Ϸ���Ҫ����ǣ� ��
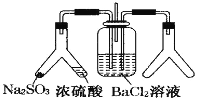
��Cu ��Ũ���� ��CaO ��Ũ��ˮ �۴���ʯ��ϡ����ܸ��������Һ��Ũ���� �ݹ������ƺ�ˮ ��������Ͷ�������
A. ȫ��B. �ۢ�C. �٢ڢݢ�D. �٢ڢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������͵������ﶼ�dz����Ĵ�����Ⱦ��ش�����������⡣
ij�¶��µ��������������ڴ����еĺ������������ʱ���漰���·�Ӧ��
i��2NO(g)��Cl2(g)2ClNO(g) ��H 1��0 ��ƽ�ⳣ��ΪK1
ii��2NO2(g)��NaCl(s) NaNO3(s)��ClNO(g) ��H2��0 ��ƽ�ⳣ��ΪK2
��1�����з�Ӧ4NO2(g)��2NaCl(s) 2NaNO3(s)��2NO(g)��Cl2(g)����˷�Ӧ��ƽ�ⳣ��K3��_______����K1��K2��ʾ������Ӧ����H3��__________������H1����H2��ʾ����
��2��Ϊ�о���ͬ�����Է�Ӧii��Ӱ�죬�ں��������£���2L�����ܱ������м���0.2mol NO2���㹻��NaCl(s)��10minʱ��Ӧii�ﵽƽ�⡣���ƽ��ʱNO2��ת������1(NO2) ��50%����
��10min����(ClNO)��_________ ��ƽ�ⳣ��K2��___________��
���������������䣬ʹ��Ӧ�ں�ѹ�����½��У�ƽ��ʱNO2ת����Ϊ��2(NO2)������1(NO2)______��2(NO2)������>����<������=������
��3������һ������NaOH��Һ����SO2�������������Һǡ�ó����ԣ������й�����Һ�����ӹ�ϵ��ȷ����______________��
a��c(Na��)��c(HSO3-)��2c(SO32-)
b��c(Na��) > c(HSO3-) ��c(SO32-) > c(H+) = c(OH��)
c��c(Na��) > c(HSO3��) + c(SO32��) +c(H2SO3)
d��c(OH-) ��c(SO32-)��c(H2SO3)��c(H+)
��4����ҵ��Ҳ������Na2SO3��Һ����SO2�����õ�ⷨ�������պ�������Һ��ʵ������Һ�Ļ��������ã�װ����ͼ��ʾ����
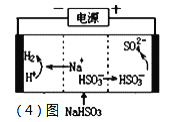
�ٹ���һ��ʱ�����������Һ��pH______����������������С����������������
��д�������ĵ缫��Ӧʽ_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ�С�H�ĺ����ʾ��ȷ����
A. H2SO4(aq)��Ba(OH)2(aq)=BaSO4(s)��2H2O(l) ��H(���)
B. NaOH(aq)��![]() H2SO4(Ũ)=
H2SO4(Ũ)=![]() Na2SO4(aq)��H2O(l) ��H(�к���)
Na2SO4(aq)��H2O(l) ��H(���)
C. CH4(g)��2O2(g)=CO2(g)��2H2O(l) ��H(ȼ����)
D. 2H2(g)��O2(g)=2H2O(g) ��H(ȼ����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ�������ж���ȷ����( )
A.��״���£�11.2 L H2O �к��е���ԭ����Ϊ0.5NA
B.5.6 g�����������ᷴӦת�Ƶĵ�����Ϊ0.3NA
C.16 g O2��16 g O3���е���ԭ����Ŀ���
D.���³�ѹ�£�11.2 L��������ԭ����ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״�����Ҫ�Ļ�ѧ��ҵ����ԭ�Ϻ�Һ��ȼ�ϡ���ҵ�Ͽ�����CO��CO2������ȼ�ϼ״�����֪�״��Ʊ����йػ�ѧ��Ӧ�Լ��ڲ�ͬ�¶��µĻ�ѧ��Ӧƽ�ⳣ�����±���ʾ��
��ѧ��Ӧ | ƽ�ⳣ�� | �¶ȣ��棩 | |
500 | 800 | ||
��2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
��H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
��3H2(g)+ CO2(g) | K3 | ||
��1����Ӧ����_________������ȡ����ȡ�����Ӧ��
��2��ij�¶��·�Ӧ����H2��ƽ��ת���ʣ�a������ϵ��ѹǿ(P)�Ĺ�ϵ����ͼ1��ʾ����ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K(A)_____K(B)�����������������������
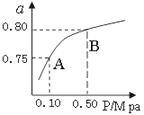
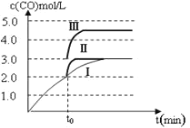
ͼ 1 ͼ2
��3���жϷ�Ӧ�ۡ�H____0�� ��S____0���>����=����<������500�桢2L���ܱ������У����з�Ӧ�ۣ����ijʱ��H2��CO2�� CH3OH��H2O�����ʵ����ֱ�Ϊ6mol��2 mol��10 mol��10 mol�� ��ʱv(��)___v(��)���>����=����<����
��4��һ���¶��£���3 L�ݻ��ɱ���ܱ������з�����Ӧ�ڣ���֪ c(CO)�뷴Ӧʱ��t�仯���ߢ�����ͼ2��ʾ������t0ʱ�̷ֱ�ı�һ�����������ߢ��Ϊ���ߢ�����ߢ����ߢ��Ϊ���ߢ�ʱ���ı��������________�������ߢ��Ϊ���ߢ�ʱ���ı��������_____________��
��5��һ�������¼״���һ����̼��Ӧ���Ժϳ����ᣮ���������£���amol/L��CH3COOH��bmol/LBa��OH��2��Һ�������ϣ���Ӧƽ��ʱ��2c��Ba2+��=c��CH3COO-�����ú�a��b�Ĵ���ʽ��ʾ�û����Һ�д���ĵ��볣��Ϊ________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com