
【题目】下图是第3周期11~17号元素某些性质变化趋势的柱形图。下列有关说法中正确的是( )
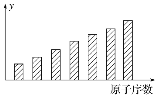
A.y轴表示的可能是电离能B.y轴表示的可能是电负性
C.y轴表示的可能是原子半径D.y轴表示的可能是形成基态离子转移的电子数
科目:高中化学 来源: 题型:
【题目】已知298K时,Ksp(NiS)=1.0×10-21,Ksp(NiCO3)=1.0×10-7 ;p(Ni)=-lg c(Ni2+),p(B)=-lg c(S2-)或-lg c(CO32-)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是( )

A. 对于曲线I,在b点加热,b点向c点移动
B. 常温下NiCO3的溶解度大于NiS的溶解度
C. 向d点对应的溶液中加入对应阴离子的钠盐,d点向b点移动
D. P为3.5且对应的阴离子是CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
(1)CH3COOH(l)+2O2(g) == 2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
(2)C(s)+ O2(g) == CO2(g) △H2=-393.5 kJmol-1
(3)H2(g) +![]() O2(g) == H2O(l) △H3=-285.8kJ·mol-1
O2(g) == H2O(l) △H3=-285.8kJ·mol-1
则反应2C(s)+2H2(g) +O2(g) == CH3COOH(l)的△H为( )
A. -488.3 kJ·mol-1 B. -244.15 kJ·mol-1 C. +488.3 kJ·mol-1 D. +244.15 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得浓度均为0.5 molL-1的Pb(CH3COO)2溶液的导电性明显弱于Pb(NO3)2溶液,又知PbS是不溶于水及稀酸的黑色沉淀,下列离子方程式书写错误的是
A.Pb(NO3)2溶液与 CH3COONa 溶液混合:Pb2++2CH3COO-= Pb(CH3COO)2
B.Pb(NO3)2 溶液与K2S溶液混合:Pb2++S2-=PbS↓
C.Pb(CH3COO)2 溶液与K2S溶液混合:Pb2++S2- =PbS↓
D.Pb(CH3COO)2 在水中电离: Pb(CH3COO)2![]() Pb2+ +2CH3COO-
Pb2+ +2CH3COO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】x mol的铁铝合金完全溶于1L某稀硝酸后,生成了y mol的NO(无其他还原产物).则关于该反应的下列说法中,不正确的是( )
A.在该反应中,硝酸既显氧化性,又显酸性
B.根据题中所给条件,无法计算出硝酸的物质的量浓度
C.参加反应的硝酸的物质的量为4y mol
D.若将生成的NO与O2混合溶于水被完全吸收,需标准状况下O2的体积是11.2y L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示,有关该有机物的叙述不正确的是

A. 在一定条件下,能发生取代、氧化、酯化和加聚反应
B. 该物质分子中最多可以有11个碳原子在同一平面上
C. 1mol该物质最多可与4molH2发生加成反应
D. 1mol该物质完全氧化最多可消耗14mol氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g),在一个可变容积的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g),在一个可变容积的密闭容器中进行,试回答:
(1)增加Fe的量,其反应速率的变化是___(填“增大”“不变”或“减小”)。
(2)增加H2O的量,其反应速率__(填“增大”“不变”或“减小”)。
(3)将容器的体积缩小一半,其反应速率__(填“增大”“不变”或“减小”)。
(4)保持体积不变,充入N2使体系压强增大,其反应速率___。(填“增大”“不变”或“减小”)。
(5)保持压强不变,充入N2使容器的体积增大,其反应速率___(填“增大”“不变”或“减小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.配置一定浓度的稀硫酸,用量筒量取浓硫酸后,未将蒸馏水洗涤量筒后的洗涤液转移至容量瓶中,会使配置的溶液浓度偏小
B.提纯混有少量硝酸铵的氯化钠,应采用在较高温度下制得浓溶液,再采取冷却结晶、过滤、干燥的方法
C.蒸发时将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热
D.石油的蒸馏实验中,忘记加沸石,可以先停止加热,待溶液冷却后加入沸石,在继续加热蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇(CH3OH)是一种重要的化工原料,可由H2与CO或CO2反应制备,主要用于制备羧基甲酯等。
(1)水杨酸甲酯是无色透明油状液体,密度为1.54g·cm-3,常作为医药制剂的赋香剂。制备及提纯水杨酸甲酯的实验步骤如下:
步骤1.在三口烧瓶中加入3.5g(0.025mol)水杨酸 、15mL(0.375mol)甲醇、1mL浓硫酸,几粒沸石,在85~95℃加热回流1.5h(装置如图所示)。
、15mL(0.375mol)甲醇、1mL浓硫酸,几粒沸石,在85~95℃加热回流1.5h(装置如图所示)。

步骤2.向回收甲醇后剩余液中加入10mL水,振荡、静置,分液出有机相。
步骤3.有机相依次用水、10%Na2CO3溶液、水洗涤。
步骤4.干燥,蒸馏并收集221~224℃馏分。
①图中仪器W的名称是___。
②步骤3,第一次水洗的主要目的是___;第二次水洗的目的是___。
③合成水杨酸甲酯的化学方程式为___;实验中加入过量甲醇的目的是___。
(2)工业上制备甲醇的主要反应有:
(Ⅰ)CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH1 平衡常数K1
CH3OH(g)+H2O(g) ΔH1 平衡常数K1
(Ⅱ)CO(g)+2H2(g)![]() CH3OH(g) ΔH2 平衡常数K2
CH3OH(g) ΔH2 平衡常数K2
(Ⅲ)CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH3 平衡常数K3
CO(g)+H2O(g) ΔH3 平衡常数K3
维持![]() =75:25,CO、CO2以及n(CO2):n(CO)=1:2,用不同催化剂时甲醇的产率随温度的变化如图所示:
=75:25,CO、CO2以及n(CO2):n(CO)=1:2,用不同催化剂时甲醇的产率随温度的变化如图所示:

①平衡常数K3=___(用K1、K2表示);△H1___0(填“>"或“<”)。
②下列叙述正确的是___ (填标号)。
A.催化剂Cu/ZnO不能催化反应(I)
B.催化剂Cu/ZnO在温度低于480K时活性很低
C.图中a点所示条件下,延长反应时间能提高甲醇的产率
D.图中b点所示条件下,若增加H2的浓度不能提高甲醇的产率
③400K时向某恒容密闭容器中充入CO和H2,使c(CO)=0.10mol·L-1,c(H2)=0.20mol·L-1,且只发生反应(II);平衡时c(CH3OH)=0.08mol·L-1。该温度下反应(II)的平衡常数为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com