
【题目】下列反应中,相关示意图错误的是
A | B | C | D |
将二氧化硫通入到一定量氯水中 | 将氨水滴入到一定量氯化铝溶液中 | 将铜粉加入到一定量浓硝酸中 | 将铁粉加入到一定量氯化铁溶液中 |
|
|
|
|
A. A B. B C. C D. D
【答案】B
【解析】A、将二氧化硫通入到一定量氯水中,会发生反应:Cl2+SO2+2H2O=H2SO4+2HCl,最终是盐酸和硫酸,所以溶液的pH不变,选项A正确;B、将氨水滴入到一定量氯化铝溶液中,会发生反应:AlCl3+3NH3·H2O== Al(OH)3↓+3NH4Cl,Al(OH)3只能被强碱溶解,而NH3·H2O是弱碱,不能溶解,因此图像不符合,选项B错误;C、将铜粉加入到一定量浓硝酸中,首先发生反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,当反应进行到一定程度后溶液变稀,这时发生反应:3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O,当硝酸反应完全后无论Cu还存在多少,都不再发生反应,因此符合题意,选项C正确;D、将铁粉加入到一定量氯化铁溶液中,2FeCl3+Fe==3FeCl2,Cl-的物质的量不变,但是由于溶液中Fe元素的质量增加,所以Cl元素的质量分数减少。当FeCl3完全反应后溶液的质量达到最大值,因此此时溶液中Cl元素的质量分数不变,选项D正确。答案选B。


科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.PCl3分子是平面三角形,中心原子磷原子是sp2杂化
B.乙炔分子中的C原子是sp2杂化
C.凡中心原子采取sp3杂化的分子,其VSEPR模型都是四面体形
D.NH4Cl中有4种化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员以Zn和尖晶石型锰酸锌(ZnMn2O4)为电极材料,研制出一种水系锌离子电池。该电池的总反应方程式:xZn + Zn1xMn2O4![]() ZnMn2O4(0 < x < 1)。下列说法正确的是
ZnMn2O4(0 < x < 1)。下列说法正确的是
A. 充电时,Zn2+向ZnMn2O4电极迁移
B. 充电时,阳极反应:ZnMn2O4 2xe—=Zn1-xMn2O4+xZn2+
C. 放电时,每转移1mol e-,ZnMn2O4电极质量增加65g
D. 充放电过程中,只有Zn元素的化合价发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CO2与NH3反应可制得重要的化工产品三聚氰胺:3NH3 + 3CO2![]()
 +3H2O。
+3H2O。
(1)基态N原子的价层电子排布图为____________,三聚氰胺的几种组成元素中电负性由大到小的顺序为____________(用元素符号表示)。
(2)三聚氰胺中氮原子的杂化轨道类型为____________。
(3)上述合成三聚氰胺的反应过程中存在多种类型化学键的断裂与形成,但这些化学键中不包括____________(填选项字母)。
a.α键 b.π键 c.非极性共价键 d.极性共价键
(4)三聚氰胺的熔点为250 ℃,则其晶体类型是____________,又知硝基苯的熔点为5.7 ℃,异致这两种物质熔点差异的原因是____________。
(5)随者科学技术的发展,科学家们已合成了由碳、氧两种元素形成的原子晶体.其晶胞结构如图(a) 所示:若晶胞参数为a pm,设NA表示阿伏加德罗常数的值,则该晶胞的密度是____________ g cm-3。
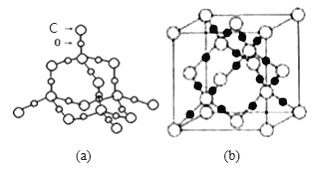
(6)SiO2晶体结构片断如图 (b)所示。通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。
化学键 | Si-O | Si-Si | O=O |
键能/ KJ·mol-1 | 460 | 176 | 498 |
Si(s)+O2(g)![]() SiO2(s),该反应的反应热△H = ___________
SiO2(s),该反应的反应热△H = ___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置进行实验,甲乙两池均为1 molL—1的AgNO3溶液,A、B均为Ag电极。实验开始先闭合K1,断开K2。一段时间后,断开K1,闭合K2,形成浓度差电池,电流计指针偏转(Ag+浓度越大氧化性越强)。下列说法不正确的是

A.闭合K1,断开K2后,A电极增重
B.闭合K1,断开K2后,乙池溶液浓度上升
C.断开K1,闭合K2后,NO3— 向B电极移动
D.断开K1,闭合K2后,A电极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E五种元素,其原子序数依次增大。C元素的单质是生活中最常见的助燃剂。A与C形成的一种化合物是引起温室效应的主要气体。D与C同主族。E是我国最早使用的合金的主要成分。根据上述信息回答下列问题:
(1)写出E元素外围电子排布式:_______________。
(2)A、B、C三种元素中电负性最大的是:___________,
第一电离能最大的是:_________(填元素符号)。
(3)D元素气态氢化物的分子构型是:__________,其键角______109°28′(填“大于”“小于”或“等于”)。D元素在其最高价氧化物分子中的杂化方式为:_________。
(4)E元素形成的单质晶体类型为:___________晶体,假设其原子半径为r pm,NA为阿伏加德罗常数,则其晶体密度的表达式为ρ=________________g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中对于相关物质的分类全部正确的是
选项 | 纯净物 | 混合物 | 非电解质 | 弱电解质 | 碱性氧化物 |
A. | 液氨 | 氢氧化铁胶体 | CO | 氢硫酸 | Al2O3 |
B. | 明矾 | 漂白粉 | 乙醇 | 硫酸钡 | Na2O |
C. | 碱石灰 | 碘酒 | Cl2 | HClO | K2O |
D. | 磁性氧化铁 | 水玻璃 | SO2 | 冰醋酸 | CaO |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. Na2O2遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色
B. Na2O2与CO2反应生成0.1 mol O2时转移电子0.4 mol
C. Na2O2投入到CuCl2溶液中有蓝色沉淀及气泡产生
D. 向饱和烧碱溶液中加入2 g Na2O2,充分反应完后,溶液中c(Na+)不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com