
����Ŀ�������������ʳƷ�ķ�������ʵ�����ñ���ͪ��ӵ��������ϳɱ����ᣬԭ����ͼ��ʾ��
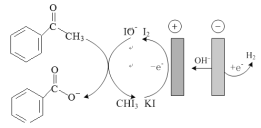
ʵ�鲽�����£�
����I���������ϳ�
�ڵ����м������� KI��20mL����ˮ��20 mL��1��4-������������������ȫ�ܽ⣬�ټ���23.30 mL����ͪ�����ӵ绯ѧװ�ã��㶨�������3h��
����II����ϴ����
��Ӧֹͣ����ӦҺת������ƿ�������ȥ��Ӧ�ܼ���������ˮ�Ͷ��ȼ���ϴ����ƿ����ϴ��Һת������Һ©�����ö��ȼ�����ȡ��ȥ���������ʣ������ˮ����л��ࣻ
����III���Ƶò�Ʒ
��Ũ�����ữˮ����pHΪ1~2�����ż��뱥��KHSO3��Һ�������ˡ�ϴ�ӡ���������õ���Ʒ12.2 g��
�й����ʵ��������±���ʾ��
���� | ����ʽ | �ܽ��� | �е�(��) | �ܶ�(g/cm3) | ��Է������� |
����ͪ | C8H8O | ������ˮ | 202.3 | 1.03 | 120 |
������ | C7H6O2 | ����ˮ | 249 | 1.27 | 122 |
���ȼ��� | CH2Cl2 | ������ˮ | 40 | 1.33 | 85 |
�ش��������⣺
(1)����I�У������ĵ缫��ӦʽΪ___������I-ʧȥ���Ӻ�IJ�����OH-��Ӧ�����ӷ���ʽΪ_��
(2)����II��������У���Ҫʹ�õ�����ͼ����������_______(����ĸ)������ͼ����������������IJ�������______(����������)��
(3)����II��Һ�����У�Ӧ��������÷ֲ��________(����ĸ)��
A�����ν��л��ࡢˮ��ӷ�Һ©�����Ͽڵ���
B�����ν��л��ࡢˮ��ӷ�Һ©�����¿ڷų�
C���Ƚ��л���ӷ�Һ©�����¿ڷų����ٽ�ˮ����¿ڷų�
D���Ƚ��л���ӷ�Һ©�����¿ڷų����ٽ�ˮ����Ͽڵ���
(4)����III�У�����Ũ�����Ŀ����_________��
(5)����III�У����뱥��NaHSO3��Һ��ˮ���е���ɫ���Ա�dz��˵��������I2����ԭΪI-�������ӷ���ʽΪ___________��
(6)��ʵ��IJ�����_________��
���𰸡�H2O��2e-=H2����2OH-����2H+��2e-=H2���� I2��2OH-= I-��IO-��H2O a��c��d��e��g ������ D ����������ת��Ϊ������ ![]() ��I2��H2O =
��I2��H2O =![]() ��3H����2I- 50.0%
��3H����2I- 50.0%
��������
����ͼʾ����������õ��ӷ�����ԭ��Ӧ������ʧ���ӷ���������Ӧд���缫��Ӧʽ������������OH-��Ӧ�����ӷ���ʽ����������װ���ж���ѡ��������ȱ���������ݷ�Һ�����涨�ȴ��¿ڷų��²�Һ�塢����Ͽڵ����ϲ�Һ�壻��ǿ��������ԭ�����ͼ��������Ŀ�ģ����ݷ�Ӧ�����жϷ�Ӧ���д�����ӷ���ʽ���������и����ı���ͪ�������������������۲�����������ʡ�
��1������װ��ͼ��֪���ұߵ缫Ϊ�����������ӵõ��ӷ�����ԭ��Ӧ����H2����H2O�õ��ӷ�����ԭ��Ӧ����H2��OH-���缫��Ӧ��2H++2e-�TH2����2H2O+2e-=H2+2OH-����ߵ缫Ϊ���ص�������I-ʧ���ӷ���������Ӧ���缫��Ӧʽ��2I--2e-�TI2������I-ʧȥ���Ӻ�IJ���I2��OH-��Ӧ�����ӷ���ʽΪI2+2OH-�TI-+IO-+H2O����Ϊ2H++2e-�TH2����2H2O+2e-=H2+2OH-��I2+2OH-�TI-+IO-+H2O��
��2����������װ�� ���µ��ϣ������ҷֱ���Ҫ�ƾ��ơ�������ƿ���¶ȼơ������ܡ�β�ӹܡ���ƿ�Ȳ���������������������ѡȡa��c��d��e��g������Ҫ�����ܣ���Ϊa��c��d��e��g�������ܡ�
���µ��ϣ������ҷֱ���Ҫ�ƾ��ơ�������ƿ���¶ȼơ������ܡ�β�ӹܡ���ƿ�Ȳ���������������������ѡȡa��c��d��e��g������Ҫ�����ܣ���Ϊa��c��d��e��g�������ܡ�
��3������II��Һ�����У�Ӧ��������ݱ������ݣ���ȡ�����ȼ�����ܶȴ���1����ˮ�أ����÷ֲ��ˮ�����ϲ㣬�л������²㣬��ҺʱΪ��ֹ���²�Һ������Ⱦ���ȴ��¿ڷų��²�Һ�塢����Ͽڵ����ϲ�Һ�壬D���ϣ���ΪD��
��4��ˮ���к��б������Σ�����Ũ���ᣬ�������κ�Ũ���ᷴӦ�������ᱽ���ᣬ���������У�����Ũ�����Ŀ���ǽ���������ת��Ϊ�������Ϊ����������ת��Ϊ�����ᡣ
��5��������У����뱥��NaHSO3��Һ��ˮ���е���ɫ���Ա�dz��˵��������I2����ԭΪI-��HSO3-��I2����ΪSO42-�������ӷ���ʽΪHSO3-+I2+H2O=SO42-+3H++2I-����ΪHSO3-+I2+H2O=SO42-+3H++2I-��
��6������ ��Ӧ��1mol����ͪ����1mol�����ᣬ23.3mL����ͪ��������m=23.3mL��1.03g/mL=24.0g������ͪ�����ʵ�����n=
��Ӧ��1mol����ͪ����1mol�����ᣬ23.3mL����ͪ��������m=23.3mL��1.03g/mL=24.0g������ͪ�����ʵ�����n=![]() =0.2mol�����������ɱ���������ʵ�����0.2mol��������0.2mol��122g/mol=24.4g������=
=0.2mol�����������ɱ���������ʵ�����0.2mol��������0.2mol��122g/mol=24.4g������=![]() =
=![]() ��100%=50.0%����Ϊ50.0%��
��100%=50.0%����Ϊ50.0%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�����ȷ����(����)
A.����ˮ��Ӧ�����ӷ���ʽ��Na��H2O=Na����OH����H2��
B.����ˮ������Ӧ�Ļ�ѧ����ʽ��3Fe��4H2O(g)![]() Fe3O4��4H2
Fe3O4��4H2
C.þ�������ˮ�����ܷ�Ӧ
D.�ƺ�����ͭ��Һ��Ӧ�����ӷ���ʽ��2Na��Cu2��=2Na����Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������H����ȡijҩ����м��壬ʵ�����ɷ����廯����A�Ʊ�H��һ�ֺϳ�·�����£�

��֪����.RCHO+CH2(COOH)2![]() RCH=CHCOOH
RCH=CHCOOH
��. ![]()
�ش��������⣺
(1)B�Ľṹ��ʽΪ____________��H�ķ���ʽΪ____________��
(2)C�к��������ŵ�������____________��B��C�ķ�Ӧ����Ϊ____________��
(3)д��F��G��H�Ļ�ѧ����ʽ��____________________________________��
(4)M��D��ͬ���칹�壬ͬʱ��������������M�Ľṹ��____________�֡�
������FeCl3��Һ������ɫ��Ӧ��
���ܷ���ˮ�ⷴӦ��
�۱�����ֻ������ȡ������
���к˴Ź���������ʾ��4��壬�ҷ����֮��Ϊ3��2��2��1��M�Ľṹ��ʽΪ_______��
(5)д����![]() ��CH2(COOH)2Ϊԭ�Ϻϳ�
��CH2(COOH)2Ϊԭ�Ϻϳ�![]() ������ͼ(���Լ���ѡ)��
������ͼ(���Լ���ѡ)��
_____________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���CO2ͨ��1L 0.01 mol��L-1 ��ijһԪ��MOH��Һ�У���Һ��ˮ�������OH-����Ũ��[cˮ(OH-)]��ͨ���CO2�����(V)�Ĺ�ϵ��ͼ��ʾ�����������������

A.MOHΪһԪǿ��
B.b����Һ�У�c(H+) = 1��10-7 mol��L-1
C.c����Һ�У�c(M+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)]
D.d����Һ�У�c(M+)=2c(CO32-)+c(HCO3-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�ܱ������з������·�Ӧ��X��g��+3Y��g��2Z��g������H��0����ͼ��ʾ�÷�Ӧ�����ʣ�v����ʱ��
��t���仯�Ĺ�ϵ��t2��t3��t5ʱ��������������ı䣬����û�иı�����ʵij�ʼ������������˵���в���ȷ���ǣ�������

A. ![]() ʱ�����˴���B.
ʱ�����˴���B. ![]() ʱ�������¶�
ʱ�������¶�
C. ![]() ʱ������ѹǿD.
ʱ������ѹǿD. ![]() ʱ����ת�������
ʱ����ת�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�ﵽ����ʵ��Ŀ�ģ���Ӧ��ʵ�鷽���Լ���ؽ��;���ȷ����
ѡ�� | ʵ��Ŀ�� | ʵ�鷽�� | ��ؽ��� |
A | ������ˮ��pH |
| pH��ֽ������ |
B | ̽��������C5H12���ѽ� |
| C5H12�ѽ�Ϊ���ӽ�С��������ϩ�� |
C | ʵ���¶ȶ�ƽ���ƶ���Ӱ�� |
| 2NO2 |
D | ��AlCl3��Һ�Ʊ�AlCl3���� |
| AlCl3�е�����ܼ�ˮ |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ij��Һ���Ƿ���![]() �����õķ�����( )
�����õķ�����( )
A.ȡ�����μ�BaCl2��Һ�����Ƿ��в�����ˮ�İ�ɫ��������
B.ȡ�����μ�ϡ�����ữ��BaCl2��Һ�����Ƿ��в�����ˮ�İ�ɫ��������
C.ȡ�����μ�ϡ���ᣬ�ٵμ�BaCl2��Һ�����Ƿ��в�����ˮ�İ�ɫ��������
D.ȡ�����μ�ϡ���ᣬ�����������ٵμ�BaCl2��Һ�����Ƿ��в�����ˮ�İ�ɫ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʱ���ķ�չ����ɫ��������Խ��Խ�ܵ���ҵ���ͬ�����Ϊ��������ÿһλ����Ӧ�����ɵ���ʶ��ijͬѧ�����÷Ͼɵ�������������Ϊԭ���ϡ����á���������������ȡ�������岢����һϵ�е�����̽����
��ȡ����������Ҫ�漰�������ĸ����裺
��һ��������Ʒ���ܽ⡣ȡһ��������Ʒ������250mL��ƿ�У�����һ��Ũ�Ⱥ������ǿ����Һ��ˮԡ����(Լ93��)������Ӧ��ȫ��(��������������)�����ȼ�ѹ���ˣ��ռ���Һ��250mL�ձ��У�
�ڶ����������������������ɡ�����Һ��������ˮԡ���У���3 mol/L H2SO4������ҺpH��8��9���õ�������ɫ����״Al(OH)3����ѹ���˵õ�������
����������������Һ�����ɡ�������ת����250mL�ձ��У����ȱߵ���һ��Ũ�Ⱥ������H2SO4��Һ��
���IJ�������������Һ���γɡ�������ȫ���ܽ�����һ�����Ĺ���K2SO4�����õ��ı��ͳ�����Һ��ȴ����ֱ������ȫ����������ѹ���ˡ�ϴ�ӡ���ɣ���ò�Ʒ��������[KAl(SO4)2��12H2O��M��474g/mol]��
�ش��������⣺
(1)��һ�������ܽ�������漰������Ҫ��Ӧ�����ӷ���ʽΪ__________________________
(2)Ϊ�˼ӿ�����Ʒ���ܽ⣬Ӧ�ö�����Ʒ����������Ԥ������________________________
(3)���IJ������У�Ϊ�˱�֤��Ʒ�Ĵ��ȣ�ͬʱ�ּ��ٲ�Ʒ����ʧ��Ӧѡ��������Һ�е�___(��ѡ����ĸ)����ϴ�ӣ�ʵ��Ч����ѡ�
A.�Ҵ� B.����K2SO4��Һ C.����ˮ D.1��1�Ҵ�ˮ��Һ
(4)Ϊ�˲ⶨ������������Ĵ��ȣ���������ʵ�������ȷ��ȡ������������4.0g���ձ��У�����50mL 1mol/L��������ܽ⣬��������Һת����100mL����ƿ�У�ϡ�����̶��ߣ�ҡ�ȣ���ȡ25.00 mL��Һ��250 mL��ƿ�У�����30 mL 0.10mol/L EDTA��2Na����Һ���ٵμӼ���2D���ӳȣ���ʱ��Һ�ʻ�ɫ����������һϵ�в�����������0.20 mol/Lп����Һ�ζ�����Һ�ɻ�ɫ��Ϊ�Ϻ�ɫ���ﵽ�ζ��յ�ʱ��������5.00 mLп����Һ���ζ�ԭ��ΪH2Y2����Al3����AlY����2H����H2Y2��(����)��Zn2����ZnY2����2H��(ע��H2Y2����ʾEDTA��2Na����Һ����)����������������Ĵ���Ϊ_________%��
(5)�������˿�������������Ϥ�ľ�ˮ��֮�⣬������������ʳƷ�����ɼ�����������(��)������������Ҫ����һ�������������������������ʳ�������������ɼ���ԭ����_______
(6)Ϊ��̽����������Ľᾧˮ��Ŀ���ֽ�����N2�����н����ȷֽ�ʵ�飬�õ�����������ȷֽ�������ͼ��ʾ(TG%�������Ƿֽ��ʣ���������ռ��Ʒԭʼ�����İٷ��ʣ�ʧ�ذٷ��ʣ�![]() ��100%)��
��100%)��
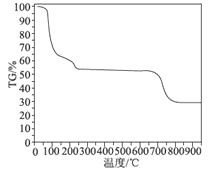
����TG���߳��ֵ�ƽ̨��ʧ�ذٷ��ʣ�30��270�淶Χ�ڣ�ʧ����ԼΪ45.57%��680��810�淶Χ�ڣ�ʧ�ذٷ���ԼΪ25.31%����ʧ����ԼΪ70.88%����ֱ�д�����漰��30��270�桢680��810���¶ȷ�Χ���������ε��ȷֽⷽ��ʽ��___________��_____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Һ��ȼ�ϵ�����������ȼ�ϵ�ؾ������С����������洢װ�õ��ŵ㡣һ������(N2H4)Ϊȼ�ϵĵ��װ����ͼ��ʾ���õ���ÿ����е�������Ϊ��������KOH��Ϊ����ʡ����й��ڸ�ȼ�ϵ�ص���������ȷ����

A. �������Ҳ�缫�������غ��������缫
B. ���������ĵ缫��ӦʽΪN2H4��4OH����4e��===N2��4H2O
C. ��ȼ�ϵ�صĵ缫����Ӧ���ö������ϣ�����ߵ缫��Ӧ�����ڵ缫���������������ʹ������������Һ��ֽӴ�
D. ��ȼ�ϵ�س����ŵ�ʱ����������������Ӧ��pH��С
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com