
【题目】下列金属活动性最强的( )
A.Mg
B.Ag
C.Cu
D.Zn
科目:高中化学 来源: 题型:
【题目】用足量的一氧化碳还原4.64 g某金属氧化物,把生成的二氧化碳全部通入到过量的澄清石灰水中,得到的沉淀干燥后质量为8.0 g,则此金属氧化物是下列中的( )
A. 氧化铜 B. 氧化铁 C. 四氧化三铁 D. 二氧化锰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHCO3的溶解度较小。在饱和的NH3和NaCl的混合溶液中通入CO2,可析出NaHCO3(固体):NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。据此,我国杰出的化学家侯德榜设计出了生产纯碱的方法:
饱和NaCl(溶液)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
这种方法被人们称为侯氏制碱法,打破了帝国主义对我国经济的一种封锁,大长了中国人的民族志气。
试回答下列问题:
(1)写出由NaHCO3固体制取Na2CO3的化学方程式:__________________。
(2)如果Na2CO3(固体)中混有NaHCO3(固体),应如何除去?_____________(写出方法);如果NaHCO3(溶液)中混有Na2CO3(溶液),应如何除去?________(写出化学方程式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,如图是海水综合利用的一个方面。
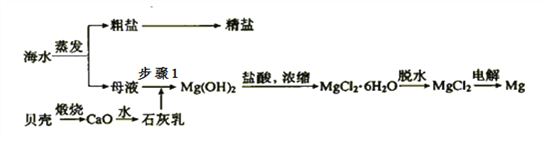
Ⅰ.(1)上述过程中没有涉及到的四大基本反应类型是 ______;
a.化合反应 b.分解反应 c.置换反应 d.复分解反应
(2)步骤1中分离操作的名称是___________;
(3)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Na2CO3溶液
加入试剂的顺序是_____________;
II.实验室利用精盐配制480mL 2.0mol·L1NaCl溶液。
(4)除容量瓶外,还需要的玻璃仪器有___________________;
(5)用托盘天平称取固体NaCl________g;
(6)配制时,按以下几个步骤进行:①计算 ②称量 ③溶解 ④冷却 ⑤转移 ⑥定容 ⑦摇匀 ⑧装瓶。操作中还缺少一个重要步骤是______________________;
(7)下列错误操作可使所配制氯化钠溶液浓度偏低的是(_________)
a.容量瓶洗净后残留了部分的水
b.转移时溶液溅到容量瓶外面
c.定容时俯视容量瓶的刻度线
d.摇匀后见液面下降,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧铅蓄电池经粗加工可得到铅膏,其主要成分为PbO、PbO2、PbSO4等。以铅膏为原料回收PbSO4,流程如下:
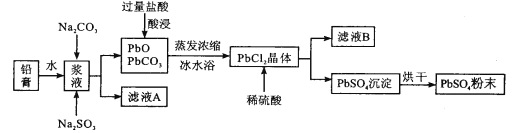
已知:PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq)ΔH>0
PbCl42-(aq)ΔH>0
(1)用Na2CO3作转化剂,将铅膏中的硫酸铅转化为碳酸铅,其离子方程式为_______。
(2)浆液中加入Na2SO3溶液的目的是________。
(3)从滤液A提取Na2SO4·10H2O晶体,主要步骤为______、______、过滤、洗涤、干燥;上述流程中可循环利用的物质是_________(写化学式)。
(4)采用冰水浴得PbCl2晶体的原因是________。
(5)理论上要得到a吨的PbSO4,则铅膏的质量范围为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl为白色粉末,微溶于水,溶于浓盐酸或NaCl浓溶液,不溶于乙醇。一种由海绵铜(Cu和少量CuO等)为原料制备CuCl的工艺流程如下:
(1)“溶解浸取”时,下列措施不能提高铜的浸取率的是__________(填序号)。
a.将海绵铜粉末与水搅拌成浆液 b.投料时,NaNO3适当过量
c.缩短浸取时间 d.将滤渣1返回再次溶解浸取
(2)“还原,氯化”时,Na2SO3和NaCl的用量对CuCl产率的影响如图-1、图-2所示:
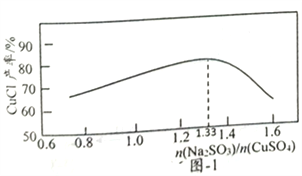

①CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl的离了方程式为__________。
②当n(Na2SO3)/n(CuSO4)>1.33时,比值越大CuCl产率越小,其原因是__________。
③当1.0<n(NaCl)/n(CuSO4)<1.5时,比值越大CuCl产率越大,其原因是__________。
(3)“过滤2”所得滤液中溶质的主要成分为__________(填化学式)。
(4)用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为Cu2(OH)3Cl。CuCl被氧化为Cu2(OH)3Cl的化学方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A.二氧化硅分子由1个硅原子和2个氧原子构成
B.二氧化硅和晶体硅都是良好的半导体材料
C.玛瑙和红宝石的主要成分都是二氧化硅
D.二氧化硅属于酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强酸性溶液X中仅含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下
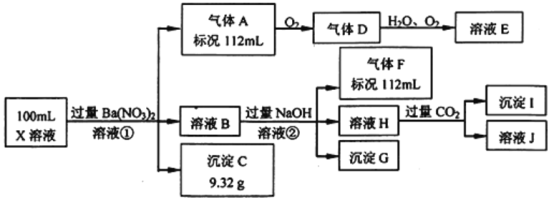
根据以上信息,回答下列问题:
(1)仅根据上述连续实验不能确定溶液X中是否含有的离子分别是________。
(2)若②中所用氢氧化钠浓度为2 mol/L,当加入10 mL时开始产生沉淀,55 mL时沉淀的量达到最大值0.03 mol,继续滴加沉淀的量保持不变,随后再滴加沉淀部分溶解,到60 mL时沉淀的量降为0.025 mol且保持不变,则原溶液中:c(Fe2+)为_____mol/L、c(Fe3+)为______mol/L、c(Cl-)为_____mol/L。(若有些离子不存在,请填0 mol/L)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com