
����Ŀ����һ��С�ձ������20g Ba��OH��28H2O��ĩ����С�ձ����������ѵ���3��4��ˮ�IJ���Ƭ�ϣ�Ȼ�����ձ��ڼ���Լ10g NH4C���壬���ò�����Ѹ�ٽ��裮
��1��ʵ���в�������������
��2��д���÷�Ӧ�Ļ�ѧ����ʽ
��3��ͨ������˵���÷�ӦΪ��Ӧ��������ȡ����ȡ����������ڷ�Ӧ������������С�ڡ������ڡ����ڡ������������������
��4��ijͬѧ��ʵ��������ͼ֮�Ľ���ʹ�ý���ϡ���������Ŀ���� 
���𰸡�
��1�����裬ʹ������Ͼ���
��2��Ba��OH��2?8H2O+2NH4Cl�TBaCl2+2NH3��+10H2O
��3������Ƭ�Ͻ�������ȣ�С��
��4�����շ�Ӧ�в����İ���
���������⣺��1��Ba��OH��28H2O������Ȼ�茶���֮��ķ�Ӧ�ǹ���֮��ķ�Ӧ�������ʹ������ֽӴ���������Ӧ�����Դ��ǣ����裬ʹ������Ͼ��ȣ�
��2.�������������Ȼ�立�Ӧ�����Ȼ�����������ˮ����Ӧ�Ļ�ѧ����ʽΪ��Ba��OH��28H2O+2NH4Cl�TBaCl2+2NH3��+10H2O�����Դ��ǣ�Ba��OH��28H2O+2NH4Cl�TBaCl2+2NH3��+10H2O��
��3.��ͨ������Ƭ�Ͻ��������ձ��͵ײ��IJ���Ƭճ��һ������ִ����ձ�����б����ĸо�������֪����������������Ȼ��֮��ķ�Ӧ�����ȵģ���Ӧ���������С��������������������Դ��ǣ�����Ƭ�Ͻ�������ȣ�С�ڣ�
��4.���÷�Ӧ���а������ɣ������������к������壬��Ի��������Ⱦ�����Բ���ֱ���ŷŵ������У�Ӧ��������ȫ����װ�ã�����ʹ��ϡ�������գ����Դ��ǣ����շ�Ӧ�в����İ�����
�����㾫����ͨ������������ȷ�Ӧ�ͷ��ȷ�Ӧ�����ջ�ѧ�ϰ����������Ļ�ѧ��Ӧ��Ϊ���ȷ�Ӧ����ѧ�ϰѷų������Ļ�ѧ��Ӧ��Ϊ���ȷ�Ӧ�����Խ����⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����绷�����˽���ȫ���ֹʹ��������������ˮ����������������ø�Ч����ɫ���������������ȡ�����������һ�ּ��ױ�ը��ǿ���������壬������ˮ�����ȶ����ʻ���ɫ����������ʹ��ʱ���뾡����ϡ���������ϡ�ͣ�ͬʱ��Ҫ������ա�����ȡ�ʵ�����Ե�ⷨ�Ʊ�ClO2���������£�

��֪����NCl3�ǻ�ɫ��״Һ���б���ξ��壬���ױ�ը�������������Ĵ̼�����ζ����Ȼ��ը��Ϊ95 �棬����ˮ���ֽ⣬�ڿ������ӷ������ȶ���
������B��ʹʪ��ĺ�ɫʯ����ֽ������
�ش��������⣺
��1��ʵ���Ҹ�������B�ķ�����___________________��Ϊ��֤ʵ��İ�ȫ���ڵ��ʱ��ע��������ǣ��ٿ��ƺ�����NCl3��Ũ�ȣ���________________________��
��2��NCl3��NaClO2(��������)�����ʵ���֮��Ϊ1��6��ϣ�����Һ��ǡ�÷�Ӧ����ClO2���÷�Ӧ�����ӷ���ʽΪ______________��
��3����ҵ��ͨ�����Ե缫����Ȼ�狀�����ķ����Ʊ�ClO2ԭ�����£�

�����������缫�IJ���ֱ���NCl3��H2��д�������ܷ�Ӧ�����ӷ���ʽΪ_____________________________��
��4��ClO2�ܲ��ȶ������������ƣ�������ˮ���յõ�ClO2��Һ��Ϊ�ⶨ������Һ��ClO2�ĺ���������������ʵ�飺
����1��ȷ��ȡClO2��Һ10mL��ϡ�ͳ�100mL������
����2����ȡV1 mL�������뵽��ƿ�У�����������pH��2.0������������KI���壬ҡ�ȣ��ڰ������� 30 min��
����3���Ե�����Һ��ָʾ������c mol/L Na2S2O3��Һ�ζ����յ㣬����Na2S2O3��ҺV2 mL��(��֪I2��2S2O![]() ===2I����S4O
===2I����S4O![]() )
)
����������3�еζ��յ��������______________________��
�ڸ�����������ɼ����ԭClO2��Һ��Ũ��Ϊ___________g/L(�ú���ĸ�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���γɵ����ʷ��ӽṹ�IJ�Σ���С����������(����)
�ٰ����ᡡ��C��H��O��N��Ԫ�ء��۰�������ˮ���ϡ���һ������������������һ�𡡢ݶ��ġ�������
A. �ڡ��١��ۡ��ܡ��ޡ���
B. �١��ڡ��ۡ��ܡ��ޡ���
C. �ڡ��١��ޡ��ۡ��ܡ���
D. �ڡ��١��ۡ��ݡ��ܡ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���A��C��H��O����Ԫ����ɣ���Է�������Ϊ90����9.0gA��ȫȼ�յIJ�������ͨ��������Ũ����ͼ�ʯ�ң��ֱ�����5.4g��13.2g��A����NaHCO3��Һ������Ӧ����2����A֮����ˮ��������Ԫ��������й�A��˵����ȷ����( )
A. ����ʽ��C3H8O3
B. A�������IJ����ܷ���������Ӧ
C. 0.1molA������Na��Ӧ����2.24L H2(��״��)
D. A��һ�������·������۷�Ӧ�IJ�����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������0.1 molL-1 NaOH��Һ�ֱ�ζ������Ϊ20.00 mL��Ũ�Ⱦ�Ϊ0.1 molL-1������ʹ�����Һ���õ��ζ���������ҺpH�����NaOH��Һ������仯�������ζ����ߡ�

�ٵζ������������______________���I��������
�ڵζ���ʼǰ��������Һ����ˮ�������c(H+)������_____________________��
��V1��V2�Ĺ�ϵ��V1 _____ V2�����������������������
������֪25��ʱ��2.0��103 mol/L�����ˮ��Һ�У�������ҺpH(��������仯)���õ�c(HF)��c(F)����ҺpH�ı仯��ϵ��ͼ��ʾ��

��1��25��ʱ��HF�ĵ���ƽ�ⳣ��Ka=_____________��
��2����֪HF(aq)![]() H+(aq)+F(aq) ��H=10.4 kJ/mol���ֽ�������0.1 mol/L HF��Һ������30�������������ʺ��ܼ��Ļӷ��������и����������__________��
H+(aq)+F(aq) ��H=10.4 kJ/mol���ֽ�������0.1 mol/L HF��Һ������30�������������ʺ��ܼ��Ļӷ��������и����������__________��
a��Ka b��Kw c��n(H+) d�� 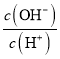
��3��25��ʱ����20 mL 0.1 mol/L������м���V mL 0.1 mol/L NaOH��Һ����û����Һ��pH�仯������ͼ��ʾ������˵����ȷ����__________________��

a��pH=3��HF��Һ��pH=11��NaF��Һ�У���ˮ�������c(H+)���
b���ٵ�ʱpH=6����ʱ��Һ�У�c(F)c(Na+)=9.9��107 mol/L
c���ڵ�ʱ����Һ�е�c(F)=c(Na+)
d���۵�ʱV=20 mL����ʱ��Һ��c(F)��c(Na+)=0.1 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�����������ԭ�Ӷ����������Ϊ8���ӽṹ����
A. ��2�� B. BF3 C. ��l2 D. ��l5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��������¶���ڿ����У��۲쵽������������ɫ����Ұ������ɫ������Һ������ɫ���塣����ʹ����в����ܲ�����������
A. Na2O B. NaOH
C. Na2CO3 D. NaHCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС����̽��ԭ��ص��γ�����������ͼ��ʾװ�ý������鲢�õ��±�ʵ������ 
��� | A | B | �ձ��е�Һ�� | ����������ָ���Ƿ�ƫת |
1 | Zn | Cu | ϡ���� | �� |
2 | Zn | Cu | �Ҵ� | �� |
3 | Cu | C | �Ȼ�����Һ | �� |
4 | Mg | Al | ����������Һ | �� |
�����������ݣ��ش��������⣺
��1��ʵ��1�е����������������A����B����
��2��ʵ��4�е�����B�� ����A���������������缫���þ����������
��3��ʵ��3 ����
A.ͭ�ڳ�ʪ�����в��ᱻ��ʴ
B.ͭ�ĸ�ʴ�ǻᷢ����
��4�������ϱ��й���Ϣ������˵������ȷ����
A.��Ի��õĽ���һ��������
B.ʧȥ���ӵĵ缫�Ǹ���
C.�ձ��е���Һ�������ǵ������Һ
D.����ͬһ�������Һ�е������缫���ǻ����Բ�ͬ�����ֽ�����������һ�ַǽ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��2SO2(g)+O2(g) ![]() 2SO3(g) ��H=Q��Q<0������ͬ�¡�ͬ�������������ܱ������зֱ����������������2molSO2��1molO2��������1molSO2 ��0.5molO2��������2molSO3�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ������ ��
2SO3(g) ��H=Q��Q<0������ͬ�¡�ͬ�������������ܱ������зֱ����������������2molSO2��1molO2��������1molSO2 ��0.5molO2��������2molSO3�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ������ ��
A. ������ѹǿp:p��=p��<2p��
B. SO3������m:m��=m��<2m��
C. c(SO2)��c(O2)֮��k:k��=k��>2k��
D. ��Ӧ�ų���������������ֵQ:Q��=Q��>2Q��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com