
| A. | 纯碱、汽油去除油污的原理相同 | |
| B. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 | |
| C. | 铁表面镀铜时,铜与电源的正极相连,铁与电源的负极相连 | |
| D. | 分馏、蒸馏、煤的液化都是物理变化,干馏、裂化、裂解都是化学变化 |
分析 A.纯碱的去污原理是水解,汽油的去污原理是溶解;
B.铜与浓硝酸发生反应而溶解;
C.电镀时,镀层金属为阳极,待镀金属为阴极;
D.煤的液化为化学变化.
解答 解:A.纯碱去油污的原理是纯碱水解溶液呈碱性,油污在碱性条件下水解,生成易溶于水的高级脂肪酸钠和甘油,从而去污,汽油为有机物,油污也为有机物,根据结构相似相溶的原理,汽油能去油污,所以纯碱与汽油去除油污的原理不相同,故A错误;
B.常温下铝可与浓硝酸发生钝化反应在表面生成一层致密的氧化膜而阻碍反应的继续进行,所以可用铝罐贮运浓硝酸,但铜与浓硝酸发生反应而溶解,不能用铜罐,故B错误;
C.电镀时,镀层金属为阳极,待镀金属为阴极,阴极与电源负极相连,阳极与电源正极相连,则铁表面镀铜时,铜与电源的正极相连,铁与电源的负极相连,故C正确;
D.煤的液化是把固体炭通过化学加工过程,使其转化成为液体燃料,为化学变化,故D错误.
故选C.
点评 本题考查较为综合,涉及盐类的水解、物质的性质、电镀以及化学反应类型的判断等知识,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,本题注意电镀的原理以及铝的性质,为高频考点,难度不大.


科目:高中化学 来源: 题型:解答题
 硼和氮元素在化学中有很重要的地位,回答下列问题:
硼和氮元素在化学中有很重要的地位,回答下列问题: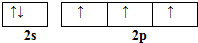 .预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为sp3.
.预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为sp3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,16g14CH4所含中子数目为8NA | |
| B. | 标准状况下,7.8g苯中含碳碳双键的数目为0.3NA | |
| C. | 含0.2NA个阴离子的Na2O2和水完全反应转移0.2mol电子 | |
| D. | 5.6g铁粉在足量的氯气中充分燃烧,得到电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
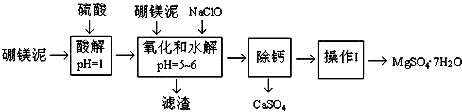
| 温度/℃ | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 五氯化磷(PCl5) | B. | 次氯酸(HClO) | C. | 二氧化碳(CO2) | D. | 三氟化硼(BF3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中Cl2发生还原反应 | |
| B. | 根据该反应可判断还原性:S2O32->Cl- | |
| C. | 脱氯反应后,溶液的酸性增强 | |
| D. | SO2与氯气的漂白原理相同,所以也可以用SO2作纺织工业的漂白剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
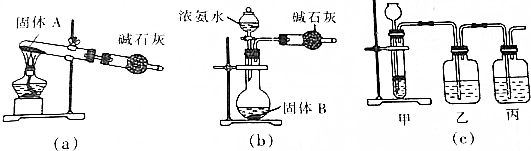
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com