
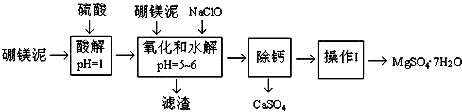
| 温度/℃ | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
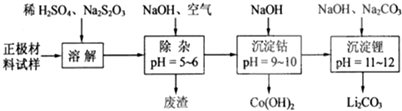
分析 硼镁泥主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,加入硫酸,MgO、CaO、MnO、Fe2O3、FeO、Al2O3都和硫酸反应,SiO2不与硫酸反应,次氯酸钠具有强氧化性,加入的NaClO可与Mn2+反应生成MnO2,把亚铁离子氧化成铁离子,溶液pH升高,铁离子生成氢氧化铁沉淀,铝离子形成氢氧化铝沉淀,过滤除去滤渣Fe(OH)3、Al(OH)3、MnO2、SiO2,滤液中含钙离子、镁离子,除钙后,只剩镁离子,蒸发冷却结晶得到硫酸镁晶体.
(1)从影响反应速率的因素分析;
(2)二氧化硅不与稀硫酸反应,所以在滤渣中存在;
(3)NaClO溶液在加热条件下将溶液中的Mn2+氧化成MnO2,溶液中含有Fe2+,具有还原性,可与NaClO发生氧化还原反应;
(4)根据检验三价铁离子的方法完成;
(5)根据表中温度对硫酸镁、硫酸钙的影响完成;根据分离晶体与溶液方法分析;
(6)根据硼镁泥中MgO的质量分数(占40%),计算出生成MgSO4•7H2O质量.
解答 解:(1)升高温度,增大接触面积,搅拌、增大反应物的浓度都可加快反应速率,
故答案为:升温;把硼镁泥粉碎、搅拌等;
(2)SiO2不与硫酸反应,次氯酸钠具有强氧化性,加入的NaClO可与Mn2+反应生成MnO2,把亚铁离子氧化成铁离子,溶液PH升高,铁离子生成氢氧化铁沉淀,铝离子形成氢氧化铝沉淀,过滤得滤渣Fe(OH)3、Al(OH)3、MnO2、SiO2,
故答案为:SiO2;
(3)NaClO溶液在加热条件下将溶液中的Mn2+氧化成MnO2,反应的离子方程式为Mn2++ClO-+H2O=MnO2↓+2H++Cl-,溶液中含有Fe2+,具有还原性,可与NaClO发生氧化还原反应,反应的离子方程式为2Fe2++ClO-+2H+=2Fe3++Cl-+H2O,
故答案为:Mn2++ClO-+H2O═MnO2↓+2H++Cl-;2Fe2++ClO-+2H+═2Fe3++Cl-+H2O;
(4)可以向溶液中加入硫氰化钾溶液检验溶液中是否存在三价铁离子,方法为:取少量滤液,向其中加入硫氰化钾溶液,如果溶液不变红色,说明滤液中不含Fe3+;如果溶液变红色,说明滤液中含Fe3+,
故答案为:取少量滤液,向其中加入硫氰化钾溶液,如果溶液不变红色,说明滤液中不含Fe3+;如果溶液变红色,说明滤液中含Fe3+;
(5)有温度对硫酸镁、硫酸钙的溶解度影响,温度越高,硫酸钙溶解度越小,可以采用蒸发浓缩,趁热过滤方法除去硫酸钙;操作I”是将滤液继续蒸发浓缩,冷却结晶,再经过过滤,便得到了MgSO4•7H2O,
故答案为:蒸发浓缩(结晶);趁热过滤;
(6)1.6t硼镁泥中氧化镁的物质的量为:$\frac{1.6×10{\;}^{6}g×40%}{40g/mol}$=1.6×104mol,根据镁原子守恒,生成MgSO4•7H2O的物质的量为1.6×104mol,质量为246g/mol×1.6×104mol=3.936×106g,若生产过程的产率为50%,则能生产出MgSO4•7H2O的质量为:3.936×106g×50%=1.968×106g=1.97t;
故答案为:1.97.
点评 本题考查物质的制备、除杂,涉及物质的检验以及沉淀的转化等知识,题目较为综合,有一定难度,本题注意要认真分析题中数据,考查学生的分析能力.


科目:高中化学 来源: 题型:选择题
| A. | v正(N2)=v逆(NH3) | B. | v正(N2)=3v正(H2) | ||
| C. | v正(H2)=$\frac{3}{2}$ v逆(NH3) | D. | N2、H2、NH3的体积比为1:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
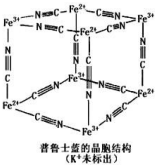 普鲁士蓝晶体结构如图所示(每两个立方体中,一个 K+在其中一个立方体中心,另一个则无 K+),下列说法正确的是( )
普鲁士蓝晶体结构如图所示(每两个立方体中,一个 K+在其中一个立方体中心,另一个则无 K+),下列说法正确的是( )| A. | 化学式可以表示为 KFe2(CN)6 | |
| B. | 每一个立方体中平均含有 24 个π键 | |
| C. | 普鲁士蓝不属于配位化合物 | |
| D. | 每个 Fe3+周围与之相邻的 Fe2+离子有 12 个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸锌溶液 | B. | 氢氧化钠固体 | C. | 碳酸钠固体 | D. | 硫酸铜固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱、汽油去除油污的原理相同 | |
| B. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 | |
| C. | 铁表面镀铜时,铜与电源的正极相连,铁与电源的负极相连 | |
| D. | 分馏、蒸馏、煤的液化都是物理变化,干馏、裂化、裂解都是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氯丙烷(C3H6Cl2)的同分异构体共有3种 | |
| B. | 蛋白质溶液具有丁达尔效应,说明该蛋白质分子直径约1nm~100nm | |
| C. | 光导纤维被广泛应用,制造它的主要原料是二氧化硅 | |
| D. | 福尔马林溶液可以使蛋白质变性,所以农业上可以用福尔马林溶液浸制生物标本 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com