
【题目】CuSO4是一种重要的化工原料,其有关制备途径如图所示。下列说法正确的是

A. 途径①所用混酸中H2SO4与HNO3物质的量之比最好为2∶3
B. 利用途径③制备16g硫酸铜,消耗硫酸的物质的量为0.1mol
C. 生成等量的硫酸铜,三个途径中参加反应的硫酸的物质的量:①=②=③
D. 与途径①、③相比,途径②更好地体现了绿色化学思想
【答案】D
【解析】A、Cu与混酸反应,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,离子反应为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,从方程式知,硝酸根离子由硝酸提供,氢离子由硝酸和硫酸提供,所以硝酸为2mol时,硫酸为3mol,用混酸中H2SO4与HNO3物质的量之比最好为3:2,故A错误;B、16g硫酸铜的物质的量为![]() =0.1mol,在途径③中,发生的反应为2H2SO4(浓) + Cu
=0.1mol,在途径③中,发生的反应为2H2SO4(浓) + Cu![]() CuSO4 + 2H2O +SO2↑,消耗硫酸0.2mol,故B错误;C. 若均生成1mol硫酸铜,途径①消耗硫酸1mol硫酸;途径②消耗1mol硫酸,途径③消耗2mol硫酸,故C错误;D、相对于途径①、③均有污染空气的气体产生,途径②的优点:铜与氧气反应生成氧化铜,氧化铜再被硫酸溶解生成硫酸铜,制取等质量胆矾需要的硫酸少、途径2无污染性气体产生,故D正确;故选D。
CuSO4 + 2H2O +SO2↑,消耗硫酸0.2mol,故B错误;C. 若均生成1mol硫酸铜,途径①消耗硫酸1mol硫酸;途径②消耗1mol硫酸,途径③消耗2mol硫酸,故C错误;D、相对于途径①、③均有污染空气的气体产生,途径②的优点:铜与氧气反应生成氧化铜,氧化铜再被硫酸溶解生成硫酸铜,制取等质量胆矾需要的硫酸少、途径2无污染性气体产生,故D正确;故选D。


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
【题目】硫酸铵[(NH4)2SO4]一种优良的氮肥(俗称肥田粉),适用于一般土壤和作物,能使枝叶生长旺盛,提高果实品质和产量,增强作物对灾害的抵抗能力,可作基肥、追肥和种肥,与氢氧化钙在加热的条件下可以生成氨气。根据所学知识回答下列问题:
(1)基态S原子的价电子排布式为____________,能量最高的电子所处的能层的符号为_________。
(2)SO42-空间构型为__________,中心原子的轨道杂化方式是________,写出一个与SO42-互为等电子体的分子的化学式__________。
(3)氨气的沸点(-33.5℃)高于硫化氢的沸点(-60.4℃)的主要原因是:_____________________________。
(4)O、N、S的第一电离能从大到小的顺序是___________________。
(5)硫酸铜溶液中通入过量的氨气会生成[Cu(NH3)4]SO4,1mol的[Cu(NH3)4]2+中σ键的个数为________。
(6)以四氯化钛、碳化钙、叠氮酸盐作原料,可以生成碳氮化钛化合物。其结构如下图所示,这种碳氮化钛化合物的化学式为________。若将该晶体的晶胞重新切割,使碳原子位于新晶胞的上下面心,则氮原子在新晶胞中的位置是__________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使湿润的红色石蕊试纸变蓝的气体,它们之间能发生如下反应:①A+H2O→B+C;②C+F→D;③D+NaOH![]() F+E+H2O。
F+E+H2O。
(1)写出它们的化学式:A________、C________、D________、F________。
(2)写出下列反应的离子方程式,并按要求填空:
①_____________,这个反应的氧化剂是________,还原剂是________;
③____________________________。
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O,写出该步反应的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列6种与人们生产生活相关的有机物:
① HCOOH(基础化工原料) ② CH3CH2COOH (防霉剂)
③ CH3CH2CH2CH3(打火机燃料) ④ ![]() (冷冻剂)
(冷冻剂)
⑤ HO—CH2—CH2—OH(汽车防冻液) ⑥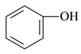 (杀菌剂)
(杀菌剂)
请回答:
(1)属于酚的是______(填序号)。
(2)与①互为同系物的是______(填序号)。
(3)与③互为同分异构体的是______(填序号)。
(4)用系统命名法给④命名,其名称为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)根据右图回答①②:
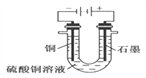
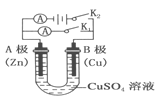
①断开 K2,闭合 K1。B 极的电极反应式为__________。
②断开 K1,闭合 K2。B 极的电极反应式为__________。
(2)根据右图回答③④:
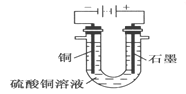
③将较纯净的CuSO4溶液放入如图2 所示的装置中进行电解电解反应的离子方程式为___________________。
④实验完成后,铜电极增重a g,石墨电极产生标准状况下的气体体积________L。
(3)以连二硫酸根(S2O42-)为媒介,使用间接电化学法也可处理燃煤烟气中的 NO),装置如图所示:
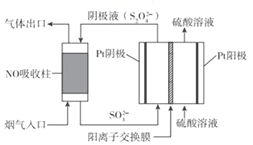
阴极区的电极反应式为_________。
(4)银锌碱性电池的电解质溶液为 KOH 溶液,电池放电时正极的 Ag2O2 (Ag 为+2价) 转化为Ag ,负极的Zn转化为K2Zn(OH)4,写出该电池总反应方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下某容积不变的密闭容器中,可逆反应C(s)+H2O(g)![]() CO(g)+H2(g)可建立平衡状态。下列状态中不能确定该反应已达到平衡状态的是( )
CO(g)+H2(g)可建立平衡状态。下列状态中不能确定该反应已达到平衡状态的是( )
A. 体系的压强不再发生变化 B. v正(CO)=v逆(H2O)
C. 生成n mol CO的同时生成n mol H2 D. 1 mol H—H键断裂的同时断裂2 mol H-O键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1-氯丙烷和2-氯丙烷分别在NaOH的乙醇溶液中加热,发生反应,下列说法正确的是
A. 生成的产物相同 B. 生成的产物不同
C. C—H键断裂的位置相同 D. C—Cl键断裂的位置相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积一定的密闭容器中,给定物质A、B、C的量,在一定条件下发生反应,建立如下化学平衡:aA(g) + bB(g)![]() xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指( )
xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指( )
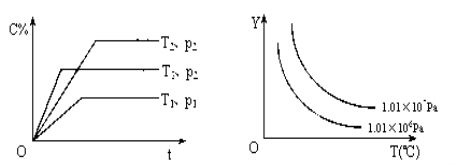
A.反应物A的百分含量
B.反应物B的平衡转化率
C.平衡混合气的密度
D.平衡混合气的总物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】意大利的一位科学家合成了一种新型的氧分子(其分子式为O4),在相同条件下,等质量的O4和O2具有相同的
A.分子数B.原子数C.体积D.物质的量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com