
【题目】完成下列实验所需的装置或仪器都正确的是( )
A.分离植物油和氯化钠溶液: 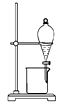
B.除去氯化钠晶体中混有的I2晶体: 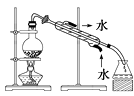
C.分离CCl4中的Br2: 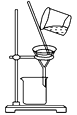
D.除去CO2气体中的HCl气体: 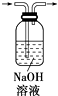
【答案】A
【解析】A.植物油和氯化钠溶液互不相溶,可用分液的方法分离,故A正确;B.除去氯化钠晶体中混有的I2晶体,可用加热升华的方法,I2晶体在加热条件下易升华,不能用蒸馏的方法,否则碘会在冷凝管中凝华,故B错误;C.二者互溶,但沸点不同,分离CCl4中的Br2应用蒸馏的方法,不能用过滤的方法,故C错误;D.除去CO2气体中的HCl气体,应用饱和碳酸氢钠溶液洗气,不能用NaOH溶液,因二者都与NaOH溶液反应,故D错误。
所以答案是:A
【考点精析】解答此题的关键在于理解蒸馏与分馏的相关知识,掌握蒸馏是将液态物质加热到沸腾变为蒸气,又将蒸气冷却为液体这两个过程联合操作.用这一操作可分离、除杂、提纯物质;分馏和蒸馏一样,也是利用混合物中各物质的沸点不同,严格控制温度,进行分离或提纯物质的操作,是多次的蒸馏.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A.氢氧燃料电池在酸性介质中的正极反应式:O2+4H++4e﹣═2H2O
B.用铁棒作阳极、碳棒作阴极电解饱和氯化钠溶液的离子方程式为:2C1﹣+2H2O ![]() H2↑+Cl2↑+2OH﹣
H2↑+Cl2↑+2OH﹣
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu一2e﹣=Cu2+
D.反应HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H<0,在理论上能用于设计原电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用如图装置电解CuSO4溶液,测定铜的相对原子质量. 
(1)若实验中测定在标准状况下放出的氧气的体积VL,B连接直流电源的(填“正极”或“负极”),并写出B极发生反应的电极反应式 .
(2)电解开始一段时间后,在U形管中可观察到的现象 .
并写出该电解反应总的离子方程式 .
(3)实验中还需测定的数据是(填写序号).
①A极的质量增重mg ②B极的质量增重mg
(4)铜的相对原子质量为:(用含有m、V的计算式表示).
(5)如果用碱性(KOH为电解质)甲烷燃料电池作为电源进行实验,放电时负极的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL 0.50molL﹣1盐酸与50mL 0.55molL﹣1 NaOH溶液,在如图所示的装置中进行中和反应,测定强酸与强碱反应的反应热. 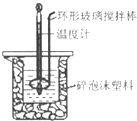
起始温度t1/℃ | 终止温度t2/℃ | 温度差 | |||
HCl | NaOH | 平均值 | |||
1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
2 | 24.5 | 24.2 | 24.45 | 27.6 | 3.15 |
3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
(1)在该实验中,量取50mL盐酸或NaOH溶液,需要用到的玻璃仪是;
(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是;
(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指温度;
(4)计算该实验发生中和反应时放出的热量为kJ[中和后生成的溶液的比热容c=4.18J(g℃)﹣1 , 稀溶液的密度都为1gcm﹣3];
(5)如果用50mL 0.55mol/L的氨水(NH3H2O)代替NaOH溶液进行上述实验,通过测得的反应热计算中和热,其中和热△H会偏大,其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学做如表实验:下列说法正确的是( )
装 |
|
|
现象 | 电流计指针未发生偏转 | 电流计指针发生偏转 |
A.“电流计指针未发生偏转”,说明铁片Ⅰ、铁片Ⅱ均未被腐蚀
B.铁片Ⅳ的电极反应式可能为Fe﹣3e﹣=Fe3+
C.用K3Fe(CN)6]溶液检验铁片Ⅲ、Ⅳ附近溶液,可判断装置的正、负极
D.铁片Ⅰ、Ⅲ所处的电解质溶液浓度相同,所以二者的腐蚀速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学键的说法中正确的是( )
A.构成单质分子的微粒中一定含有共价键
B.由非金属元素组成的化合物不一定是共价化合物
C.非极性键只存在于双原子单质分子里
D.不同元素组成的多原子分子里的化学键一定是极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中只可能含有K+、Ag+、Ba2+、Cu2+、Cl-、OH-、CO ![]() 、SO
、SO ![]() 中的一种或几种,对其进行如下实验操作:( )
中的一种或几种,对其进行如下实验操作:( )
⑴取少量溶液,滴加无色酚酞试液,酚酞变红;
⑵另取少量溶液,加入足量BaCl2溶液,产生白色沉淀;
⑶向(2)所得混合物中加足量盐酸,沉淀部分溶解,并有无色气体生成;
⑷将(3)所得混合物过滤,向滤液中加入AgNO3溶液,有白色沉淀生成。
下列对该溶液的说法正确的是
A.一定含有OH-、CO ![]() 、SO
、SO ![]() 、Cl-
、Cl-
B.可能含有K+、Cl-
C.一定不含有Ag+、Ba2+、Cu2+
D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:
CO(g)+H2O(g) ![]() CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:
CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= , 该反应为反应(选填“吸热”、“放热”).
(2)能判断该反应是否达到化学平衡状态的依据是;
A.容器中压强不变
B.混合气体中c(CO)不变
C.v逆(H2)=v正(H2O)
D.c(CO2)=c(CO)
(3)830℃时,容器中的反应已达到平衡.在其他条件不变的情况下,在此温度下,若该容器中含有1molCO2、1.2molH2、0.75molCO、1.5molH2O,这状态(是或否)处于平衡状态?若不是,反应向哪个方向进行? . (选填“向正反应方向”、“向逆反应方向”).
(4)若830℃时,向容器中充入lmolCO、5molH2O,反应达到平衡后,CO的转化率为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com