
【题目】有机物X常被用于制香料或作为饮料酸化剂,在医学上也有广泛用途。物质X的结构简式如下图所示,下列关于物质X的说法正确的是( )
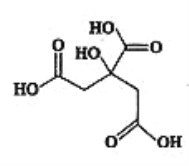
A. X的分子式为C6H7O7
B. X不能发生消去反应,但能发生水解反应
C. 1mol物质X最多可以和4molNaOH发生反应
D. 足量的X分别与等物质的量的NaHCO3、Na2CO3反应得到的气体的物质的量相同
科目:高中化学 来源: 题型:
【题目】25℃时,由水电离产生的c(H+)和c(OH-)的乘积为1×10-18的溶液里,可能大量共存的离子组是
A. NH4+、Na+、Cl-、I- B. Na+、K+、Fe3+、SCN-
C. Na+、Al3+、Cl-、AlO2- D. Na+、K+、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 等质量的乙烯和乙醇完全燃烧,消耗O2的物质的量相同
B. 乙醇与浓硫酸混合,加热至170℃制乙烯的反应属于消去反应
C. 用酸性重铬酸钾溶液检验酒驾,发生的反应属于乙醇的氧化反应
D. 乙醛使溴水或酸性KMnO4溶液褪色均属于氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有兴趣研究小组用工业废渣(主要成分为Cu2S和Fe2O3)制取氯化亚铜并同时生成电路板蚀刻液。资料显示:氯化亚铜(化学式为CuCl)常用作有机合成工业中的催化剂,通常是一种白色粉末,微溶于水、不溶于乙醇,在潮湿空气中易水解氧化成绿色;见光则分解。
他们设计流程如下:
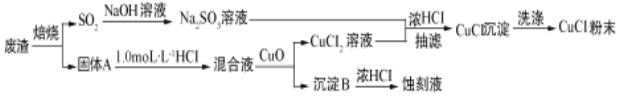
据此流程和以上信息回答下列问题:
(1)验证焙烧气体产物是SO2的方法______________________________________;溶解固体A对应的化学方程式为_____________________________________。
(2)SO2吸收用NaOH溶液,为得到纯净的Na2SO3溶液,其操作应为_____________________________________________________________________。
(3)在Na2SO3的水溶液中逐滴加入CuCl2溶液,再加入少量浓盐酸混匀,倾出清液,抽滤即得CuCl沉淀.写出该反应的离子方程式______。
(4)CuCl沉淀的洗涤需要经过酸洗、水洗和醇洗,水洗操作为____________________;醇洗不能省略,原因是______。
(5)得到CuCl沉淀要迅速真空干燥、冷却,密封包装。这样操作的目的是_______________________________________________________。
(6)氯化亚铜在热水中迅速与水反应生成砖红色固体,写出该反应的化学方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:锂离子电池的总反应为:LixC+Li1-xCoO2![]() C+LiCoO2锂硫电池的总反应为:2Li+S
C+LiCoO2锂硫电池的总反应为:2Li+S![]() Li2S。有关上述两种电池说法正确的是
Li2S。有关上述两种电池说法正确的是
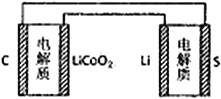
A. 锂离子电池放电时,Li+向负极迁移 B. 锂硫电池充电时,锂电极发生还原反应
C. 理论上两种电池的比能量相同 D. 右图表示用锂离子电池给锂硫电池充电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在航天飞机返回地球大气层时,为防止其与空气剧烈摩擦而被烧毁,需在航天飞机外表面安装保护层.该保护层的材料可能为( )
A.铝合金
B.合金钢
C.新型陶瓷
D.塑料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同主族常见的三种元素 X、Y、Z,它们最高价氧化物对应水化物的酸性强弱顺序为:HXO4<HYO4<HZO4 , 下列判断不正确的是( )
A.Y 单质可以在海水中提取
B.单质氧化性:Y>Z
C.气态氢化物稳定性:HX<HZ
D.离子半径:X﹣>Y﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求填空:
(1)FeSO4可转化为FeCO3,FeCO3在空气中加热可制得铁系氧化物材料
已知25℃,101kPa时:4Fe(s)+3O2(g)=2Fe2O3(s)ΔH=-1648kJ/mol
C(s)+O2(g)=CO2(g) ΔH=-393kJ/mol
2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1480kJ/mol
FeCO3在空气中加热反应生成Fe2O3的热化学方程式为_______.
(2)某温度时水的离子积Kw=1.0×10-13,则该温度时纯水的pH____7(填“>”、“<”或“=”)。该温度下,pH=2的CH3COOH溶液中,c(OH-)=_________。
(3)向2份0.1mol/LCH3COONa溶液中分别加人少量NH4NO3、Na2SO3固体(忽略体积变化),则CH3COO-浓度的变化依次为_____、______ (填“减小”“增大”或“不变”)。
(4)同浓度的NaA和NaB两种溶液pH前者大于后者,比较两份溶液中所含阴阳离子总浓度大小, NaA_______NaB (填">”、“<”或“=")。
(5)25℃时,某溶液中Fe3+的浓度为0.010mol/L,使Fe3+沉淀完全的pH为____。(Ksp[Fe(OH)3]=4×10-38,1g2=0.3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com