
ЁОЬтФПЁПЦћГЕЗЂЖЏЛњжаЩњГЩ NO ЕФЗДгІЮЊЃКN2(g) + O2(g)![]() 2NO(g)ЃЌtЁцЪБЃЌK= 0.09ЁЃдк tЁцЯТМзЁЂввЁЂБћШ§ИіКуШнУмБеШнЦїжаЃЌЭЖШы N2(g)КЭ O2(g)ФЃФтЗДгІЃЌЦ№ЪМХЈЖШШчЯТБэЫљЪОЁЃ
2NO(g)ЃЌtЁцЪБЃЌK= 0.09ЁЃдк tЁцЯТМзЁЂввЁЂБћШ§ИіКуШнУмБеШнЦїжаЃЌЭЖШы N2(g)КЭ O2(g)ФЃФтЗДгІЃЌЦ№ЪМХЈЖШШчЯТБэЫљЪОЁЃ
Ц№ЪМХЈЖШ | Мз | вв | Бћ |
c(N2)/molЁЄL-1 | 0.46 | 0.46 | 0.92 |
c(O2)/molЁЄL-1 | 0.46 | 0.23 | 0.92 |
ЯТСаХаЖЯВЛе§ШЗЕФЪЧ
A.Ц№ЪМЪБЃЌЗДгІЫйТЪЃКБћЃОМзЃОввB.ЦНКтЪБЃЌN2 ЕФзЊЛЏТЪЃКМзЃОвв
C.ЦНКтЪБЃЌc(NO)ЃКМзЃНБћЃОввD.ЦНКтЪБЃЌМзжа c(N2)= 0.4molЁЄL-1
ЁОД№АИЁПC
ЁОНтЮіЁП
N2(g) + O2(g)![]() 2NO(g)ЃЌЮЊЗДгІЧАКѓЦјЬхЬхЛ§ВЛБфЕФЗДгІЃЌИљОнгАЯьЫйТЪКЭЦНКтЕФЬѕМўНјааЗжЮіЃЌСаГіШ§ЖЮЪНЃЌРћгУЦНКтГЃЪ§ЧѓГіБфЛЏЕФСПЃЌдйЧѓГіЦНКтЪБЕФХЈЖШЁЃ
2NO(g)ЃЌЮЊЗДгІЧАКѓЦјЬхЬхЛ§ВЛБфЕФЗДгІЃЌИљОнгАЯьЫйТЪКЭЦНКтЕФЬѕМўНјааЗжЮіЃЌСаГіШ§ЖЮЪНЃЌРћгУЦНКтГЃЪ§ЧѓГіБфЛЏЕФСПЃЌдйЧѓГіЦНКтЪБЕФХЈЖШЁЃ
AЃЎдкtЁцЯТМзЁЂввЁЂБћШ§ИіКуШнУмБеШнЦїжаЃЌЗДгІЮяХЈЖШдНДѓЗДгІЫйТЪдНПьЃЌЦ№ЪМЪББћжаN2КЭO2ЕФХЈЖШЖМзюДѓЃЌМзЁЂввжаN2ХЈЖШЯрЕШЃЌМзжаO2ЕФХЈЖШДѓгкввжаO2ЕФХЈЖШЃЌдђЦ№ЪМЪБЗДгІЫйТЪЃКБћЃОМзЃОввЃЌЙЪAе§ШЗЃЛ
BЃЎМзЁЂввжаЕЊЦјЕФХЈЖШЯрЕШЃЌМзЯрЕБгкдкввЕФЛљДЁЩЯдіДѓбѕЦјЕФХЈЖШЃЌЦНКте§ЯђвЦЖЏЃЌдђМзжаЕЊЦјЕФзЊЛЏТЪДѓгкввжаЃЌМДЦНКтЪБN2ЕФзЊЛЏТЪЃКМзЃОввЃЌЙЪBе§ШЗЃЛ
CЃЎN2(g) + O2(g)![]() 2NO(g)ЮЊЗДгІЧАКѓЦјЬхЬхЛ§ВЛБфЕФЗДгІЃЌБћжаЦ№ЪМИїЮяжЪЕФХЈЖШЪЧМзжаЕФСНБЖЃЌБћЯрЕБгкдкМзЕФЛљДЁЩЯНЋЬхЛ§ЫѕаЁвЛАыЃЌдіДѓбЙЧПЦНКтВЛвЦЖЏЃЌдђЦНКтЪББћжаNOХЈЖШЮЊМзЕФ2БЖЃЌМДcЃЈNOЃЉЃК2Мз=БћЃЌМзЁЂввжаЕЊЦјЕФХЈЖШЯрЕШЃЌМзЯрЕБгкдкввЕФЛљДЁЩЯдіДѓбѕЦјЕФХЈЖШЃЌЦНКте§ЯђвЦЖЏЃЌдђЦНКтЪБcЃЈNOЃЉЃКМзЃОввЃЌЙЪCДэЮѓЃЛ
2NO(g)ЮЊЗДгІЧАКѓЦјЬхЬхЛ§ВЛБфЕФЗДгІЃЌБћжаЦ№ЪМИїЮяжЪЕФХЈЖШЪЧМзжаЕФСНБЖЃЌБћЯрЕБгкдкМзЕФЛљДЁЩЯНЋЬхЛ§ЫѕаЁвЛАыЃЌдіДѓбЙЧПЦНКтВЛвЦЖЏЃЌдђЦНКтЪББћжаNOХЈЖШЮЊМзЕФ2БЖЃЌМДcЃЈNOЃЉЃК2Мз=БћЃЌМзЁЂввжаЕЊЦјЕФХЈЖШЯрЕШЃЌМзЯрЕБгкдкввЕФЛљДЁЩЯдіДѓбѕЦјЕФХЈЖШЃЌЦНКте§ЯђвЦЖЏЃЌдђЦНКтЪБcЃЈNOЃЉЃКМзЃОввЃЌЙЪCДэЮѓЃЛ
DЃЎtЁцЪБЃЌK=0.09ЃЌЩшМзШнЦїДгЦ№ЪМЕНЦНКтЕЊЦјЯћКФЕФХЈЖШЮЊxmol/LЃЌСаГіЗДгІЕФШ§ЖЮЪНЃК
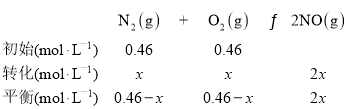
ЦНКтГЃЪ§K=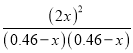 =0.09ЃЌНтЕУx=0.06ЃЌЫљвдЦНКтЪБМзжаcЃЈN2ЃЉ=0.4 molЁЄLЃ1ЃЌЙЪDе§ШЗЃЛ
=0.09ЃЌНтЕУx=0.06ЃЌЫљвдЦНКтЪБМзжаcЃЈN2ЃЉ=0.4 molЁЄLЃ1ЃЌЙЪDе§ШЗЃЛ
ЙЪбЁCЁЃ


 ЧсЧЩЖсЙкжмВтдТПМжБЭЈУћаЃЯЕСаД№АИ
ЧсЧЩЖсЙкжмВтдТПМжБЭЈУћаЃЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПбаОПЗДгІЙ§ГЬЕФШШСПБфЛЏЖдгкЩњВњЩњЛюгаживЊвтвхЁЃ
Ђё.МзДМЪЧживЊЕФЛЏЙЄдСЯЁЃРћгУКЯГЩЦј(жївЊГЩЗжЮЊCOЁЂCO2КЭH2)дквЛЖЈЬѕМўЯТКЯГЩМзДМЁЃЧыАДвЊЧѓЛиД№ЯТСаЮЪЬтЃК
(1)ЗДгІCO2(g)ЃЋ3H2(g) ![]() CH3OH(g)ЃЋH2O(g)дкЪЙгУКЭЮДЪЙгУДпЛЏМСЪБЃЌЗДгІЙ§ГЬКЭФмСПЕФЖдгІЙиЯЕШчЭМЫљЪОЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ___(ЬюзжФИДњКХ)ЁЃ
CH3OH(g)ЃЋH2O(g)дкЪЙгУКЭЮДЪЙгУДпЛЏМСЪБЃЌЗДгІЙ§ГЬКЭФмСПЕФЖдгІЙиЯЕШчЭМЫљЪОЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ___(ЬюзжФИДњКХ)ЁЃ

AЃЎИУПЩФцЗДгІЕФе§ЗДгІЮЊЮќШШЗДгІ
BЃЎЖЯСбЗДгІЮяжаЕФЛЏбЇМќЫљЮќЪеЕФзмФмСПаЁгкаЮГЩЩњГЩЮяжаЕФЛЏбЇМќЫљЪЭЗХЕФзмФмСП
CЃЎЧњЯпbЪЧЪЙгУСЫДпЛЏМСЖдгІЕФЧњЯпЃЌЧвМгШыДпЛЏМСКѓЃЌЗДгІШШБфаЁ
(2)COЁЂCO2КЭH2дкКЯГЩЙ§ГЬжаЗЂЩњЕФжївЊЗДгІШчЯТЃК
ЂйCO(g)ЃЋ2H2(g) ![]() CH3OH(g)ЁЁІЄH1ЃНЃ99 kJЁЄmolЃ1
CH3OH(g)ЁЁІЄH1ЃНЃ99 kJЁЄmolЃ1
ЂкCO2(g)ЃЋ3H2(g) ![]() CH3OH(g)ЃЋH2O(g)ЁЁІЄH2ЃНЃ58 kJЁЄmolЃ1
CH3OH(g)ЃЋH2O(g)ЁЁІЄH2ЃНЃ58 kJЁЄmolЃ1
ЂлCO2(g)ЃЋH2(g) ![]() CO(g)ЃЋH2O(g)ЁЁІЄH3
CO(g)ЃЋH2O(g)ЁЁІЄH3
дђІЄH3ЃН____ЁЃ
(3)жБНгМзДМШМСЯЕчГи(МђГЦDMFC)гЩгкЦфНсЙЙМђЕЅЁЂФмСПзЊЛЏТЪИпЁЂЖдЛЗОГЮоЮлШОЃЌПЩзїЮЊГЃЙцФмдДЕФЬцДњЦЗЖјдНРДдНЪмЕНЙизЂЁЃDMFCЕФЙЄзїдРэШчЭМЫљЪОЃК

дђЭЈШыaЦјЬхЕФЕчМЋЪЧЕчГиЕФ____(ЬюЁАе§ЁБЛђЁАИКЁБ)МЋЃЌЦфЕчМЋЗДгІЪНЮЊ___ЁЃ
Ђђ.вбжЊЕЅжЪСђдкЭЈГЃЬѕМўЯТвдS8(аБЗНСђ)ЕФаЮЪНДцдкЃЌЖјдкеєЦјзДЬЌЯТЃЌгаS2ЁЂS4ЁЂS6МАS8ЕШЖржжЭЌЫивьаЮЬхЃЌЦфжаS4ЁЂS6КЭS8ОпгаЯрЫЦЕФНсЙЙЬиЕуЃЌЦфНсЙЙШчЭМЫљЪОЃК
![]()
(1)дквЛЖЈЮТЖШЯТЃЌВтЕУСђеєЦјЕФЦНОљФІЖћжЪСПЮЊ80 gЁЄmolЃ1ЃЌдђИУеєЦјжаS2ЕФЬхЛ§ЗжЪ§ВЛаЁгк_____ЁЃ
(2)ШєвбжЊСђбѕМќЕФМќФмЮЊd kJЁЄmolЃ1ЃЌбѕбѕМќЕФМќФмЮЊe kJЁЄmolЃ1ЃЌS(s)ЃЋO2(g)===SO2(g)ІЄHЃНЃa kJЁЄmolЃ1ЃЌдђS8жаСђСђМќЕФМќФмЮЊ_____ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЛЏбЇаЁзщЮЊСЫбаОПЭтНчЬѕМўЖдЛЏбЇЗДгІЫйТЪЕФгАЯьЃЌНјааСЫЫсадИпУЬЫсМигыВнЫсЕФЗДгІЃЌМЧТМвдЯТЪЕбщЪ§ОнЃЈвбжЊ![]() ЮЊАЂЗќйЄЕТТоГЃЪ§ЕФжЕЃЉЃК
ЮЊАЂЗќйЄЕТТоГЃЪ§ЕФжЕЃЉЃК
ЪдЙмжаЫљМгЪдМСМАЦфгУСП/mL | ШмвКЭЫжСЮоЩЋЫљашЪБМф/min | |||||
ЪЕбщБрКХ | ЪЕбщЮТЖШ/Ёц | 0.6 mol/LH2C2O4ШмвК | H2O | 3 mol/LH2SO4ШмвК | 0.05 mol/LKMnO4ШмвК | |
Ђй | 25 | 3.0 | v1 | 2.0 | 3.0 | 1.5 |
Ђк | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
Ђл | 50 | 2.0 | v2 | 2.0 | 3.0 | 1.0 |
ЃЈ1ЃЉЧыаДГіИУЗДгІЕФРызгЗНГЬЪНЃК___ЃЌЕБИУЗДгІвдЪЕбщЂйжаЪ§ОнЗДгІЭъШЋЪБзЊвЦЕчзгЪ§ЮЊ_____![]() ЁЃ
ЁЃ
ЃЈ2ЃЉЪЕбщЂйЂкЪЧЬНОПХЈЖШЖдЗДгІЫйТЪЕФгАЯьЃЌЪЕбщЂкЂлЪБЬНОПЮТЖШЖдЗДгІЫйТЪЕФгАЯьЃЌдђБэжаV1=_______ЃЌV2=__________ЁЃ
ЃЈ3ЃЉИљОнЪЕбщЂйЁЂЂкЕФЪ§ОнЃЌПЩвдЕУЕНЕФНсТлЪЧ____ЁЃ
ЃЈ4ЃЉИУаЁзщЭЌбЇИљОнОбщЛцжЦСЫnЃЈMn2+ЃЉЫцЪБМфБфЛЏЕФЧїЪЦШчЭМ1ЫљЪОЃЌЕЋгаЭЌбЇВщдФвбгаЕФЪЕбщзЪСЯЗЂЯжЃЌИУЪЕбщЙ§ГЬжаnЃЈMn2+ЃЉЫцЪБМфБфЛЏЕФЪЕМЪЧїЪЦШчЭМ2ЫљЪОЁЃ

ИУаЁзщЭЌбЇИљОнЩЯЪіаХЯЂЬсГіСЫаТЕФМйЩшЃЌВЂЩшМЦвЛЯТЪЕбщЗНАИМЬајНјааЪЕбщЬНОПЁЃ
ЪЕбщБрКХ | ЪЕбщЮТЖШ/Ёц | ЪдЙмжаЫљМгЪдМСМАЦфгУСП/ml | дйМгШыФГжжЙЬЬх | ШмвКЭЫжСЮоЩЋЫљашЪБМф/min | |||
0.6 mol/LH2C2O4ШмвК | H2O | 3 mol/LH2SO4ШмвК | 0.05 mol/L KMnO4 ШмвК | ||||
Ђм | 25 | 3.0 | 2.0 | 2.0 | 3.0 | MnSO4 | t |
ЂйИУаЁзщЭЌбЇЬсГіЕФаТМйЩшЪЧ__________ЁЃ
ЂкШєИУаЁзщЭЌбЇЬсГіЕФМйЩшГЩСЂЃЌгІЙлВьЕН__________ЃЈЬюЪЕбщЯжЯѓЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛЖЈЬѕМўЯТЃЌРћгУ CO2 КЯГЩ CH3OH ЕФЗДгІШчЯТЃКCO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g)ЁїH1ЃЌбаОПЗЂЯжЃЌЗДгІЙ§ГЬжаЛсгаИБЗДгІЃКCO2(g) + H2(g)
CH3OH(g) + H2O(g)ЁїH1ЃЌбаОПЗЂЯжЃЌЗДгІЙ§ГЬжаЛсгаИБЗДгІЃКCO2(g) + H2(g)![]() CO(g) + H2O(g) ЁїH2ЁЃЮТЖШЖд CH3OHЁЂCO ЕФВњТЪгАЯьШчЭМЫљЪОЁЃЯТСаЫЕЗЈжаЃЌВЛе§ШЗЕФЪЧ
CO(g) + H2O(g) ЁїH2ЁЃЮТЖШЖд CH3OHЁЂCO ЕФВњТЪгАЯьШчЭМЫљЪОЁЃЯТСаЫЕЗЈжаЃЌВЛе§ШЗЕФЪЧ
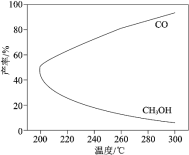
A.ЁїH1 < 0ЃЌЁїH2 > 0
B.діДѓбЙЧППЩвдЫѕЖЬКЯГЩЗДгІДяЕНЦНКтЫљашЕФЪБМф
C.ЩњВњЙ§ГЬжаЃЌЮТЖШдНИпдНгаРћгкЬсИп CH3OH ЕФВњТЪ
D.КЯГЩ CH3OH ЗДгІЕФЦНКтГЃЪ§БэДяЪНЪЧK=![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЭМЪОФкШнЕФЖдгІЫЕУїе§ШЗЕФЪЧ
БрКХ | A | B | C | D |
ЭМЪО |
ЪГбЮЫЎ |
ЦЌПЬКѓдкFe ЕчМЋИННќЕЮШыK3[Fe(CN)6]ШмвК |
|
|
ЫЕУї | бщжЄЬњЖЄЗЂЩњ ЮќбѕИЏЪД | бщжЄ Fe ЕчМЋБЛБЃЛЄ | ИУзАжУЪЧЮўЩќбєМЋЕФвѕМЋБЃЛЄЗЈ | ИУЛЏбЇЗДгІЮЊЗХШШЗДгІ |
A.AB.BC.CD.D
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПКЯГЩАБЪЧШЫРрПЦбЇММЪѕЩЯЕФвЛЯюжиДѓЭЛЦЦЃЌЦфЗДгІдРэЮЊЃКN2(g)+3H2(g)2NH3(g) ЁїH=-92.4kJmol-1
вЛжжЙЄвЕКЯГЩАБЕФМђвзСїГЬЭМШчЭМЃК
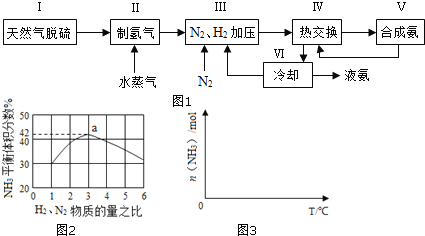
ЃЈ1ЃЉЬьШЛЦјжаЕФH2SдгжЪГЃгУГЃгУАБЫЎЮќЪеЃЌВњЮяЮЊNH4HSЁЃвЛЖЈЬѕМўЯТЯђNH4HSШмвКжаЭЈШыПеЦјЃЌЕУЕНЕЅжЪСђВЂЪЙЮќЪевКдйЩњЃЌаДГідйЩњЗДгІЕФЛЏбЇЗНГЬЪНЃК___ЁЃ
ЃЈ2ЃЉВНжшIIжажЦТШЦјдРэШчЯТЃК
ЂйCH4(g)+H2O(g)=CO2(g)+3H2(g) ЁїH=+206.4kJmol-1
ЂкCO(g)+H2O(g)=CO2(g)+H2(g) ЁїH=-41.2kJmol-1
ЖдгкЗДгІЂйЃЌвЛЖЈПЩвдЬсИпЦНКтЬхЯЕжаH2АйЗжКЌСПЃЌгжФмМгПьЗДгІЫйТЪЕФЪЧ___ЁЃ
a.Щ§ИпЮТЖШ b.діДѓЫЎеєЦјХЈЖШ c.МгШыДпЛЏМС d.НЕЕЭбЙЧП
РћгУЗДгІЂкЃЌНЋCOНјвЛВНзЊЛЏЃЌПЩЬсИпH2ВњСПЁЃШє1molCOКЭH2ЕФЛьКЯЦјЬх(COЕФЬхЛ§ЗжЪ§ЮЊ20%)гыH2OЗДгІЃЌЕУЕН1.18molCOЁЂCO2КЭH2ЕФЛьКЯЦјЬхЃЌдђCOзЊЛЏТЪЮЊ___ЁЃ
ЃЈ3ЃЉЭМ2БэЪО500ЁцЁЂ60.0MPaЬѕМўЯТЃЌдСЯЦјЭЖСЯБШгыЦНКтЪБNH3ЬхЛ§ЗжЪ§ЕФЙиЯЕЁЃИљОнЭМжаaЕуЪ§ОнМЦЫуN2ЕФЦНКтЬхЛ§ЗжЪ§ЃК___ЁЃ
ЃЈ4ЃЉвРОнЮТЖШЖдКЯГЩАБЗДгІЕФгАЯьЃЌдкЭМ3зјБъЯЕжаЃЌЛГівЛЖЈЬѕМўЯТЕФУмБеШнЦїФкЃЌДгЭЈШыдСЯЦјПЊЪМЃЌЫцЮТЖШВЛЖЯЩ§ИпЃЌNH3ЮяжЪЕФСПБфЛЏЕФЧњЯпЪОвтЭМ___ЁЃ
ЃЈ5ЃЉЩЯЪіСїГЬЭМжаЃЌЪЙКЯГЩАБЗХГіЕФШШСПЕУЕНГфЗжРћгУЕФжївЊВНжшЪЧ___(ЬюађКХ)ЃЌМђЪіБОСїГЬжаЬсИпКЯГЩАБдСЯзмзЊЛЏТЪЕФЗНЗЈЃК___ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГаЫШЄаЁзщРћгУЮФЯззЪСЯЩшМЦЗНАИЖдТШМАЦфЛЏКЯЮяНјааЬНОПЁЃ
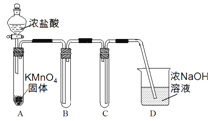
Ђё.гУИпУЬЫсМиКЭХЈбЮЫсЗДгІжЦШЁТШЦј
ЃЈ1ЃЉИУаЁзщРћгУгвЭМзАжУМАЪдМСжЦБИВЂЪеМЏЪЪСПCl2ЃЌзАжУBЁЂCЕФзїгУЗжБ№ЪЧ___________ЁЂ_______________ЁЃ
ЃЈ2ЃЉжЦЕУЕФТШЦјжаМгШыЪЪСПЫЎЃЌЕУЕНБЅКЭТШЫЎЃЌБЅКЭТШЫЎжаКЌТШдЊЫиЕФЮЂСЃга____________ЃЈаДГіШЋВПЮЂСЃЃЉЁЃ
ЃЈ3ЃЉБЅКЭТШЫЎгыЪЏЛвЪЏЕФЗДгІЪЧжЦШЁНЯХЈHC1OШмвКЕФЗНЗЈжЎвЛЁЃдкЙ§СПЕФЪЏЛвЪЏжаМгШыБЅКЭТШЫЎГфЗжЗДгІЃЌгаЩйСПЦјХнВњЩњЃЌШмвКЧГЛЦТЬЩЋЭЪШЅЃЌЙ§ТЫЃЌЕУЕНЕФТЫвКЦфЦЏАзадБШБЅКЭТШЫЎИќЧПЁЃ
ЂйТЫвКЦЏАзаддіЧПЕФдвђЪЧ________________ЃЈгУЛЏбЇЦНКтвЦЖЏдРэНтЪЭЃЉЁЃ
ЂкБЅКЭТШЫЎгыЪЏЛвЪЏЗДгІЩњГЩHC1OЕФЗНГЬЪНЪЧ___________________ЁЃ
Ђђ. ClO3ЁЊЁЂClЁЊКЭH+ЗДгІЕФЬНОП
ЃЈ4ЃЉKClO3ЁЂKClгыСђЫсПЩвдЗДгІЁЃИУаЁзщЩшМЦСЫЯЕСаЪЕбщбаОПЗДгІЬѕМўЖдЗДгІЕФгАЯьЃЌЪЕбщМЧТМШчЯТЃЈЪЕбщдкЪвЮТЯТНјааЃЉЃК
ЩеББрКХ | 1 | 2 | 3 | 4 |
ТШЫсМиБЅКЭШмвК | 1mL | 1mL | 1mL | 1mL |
ТШЛЏМиЙЬЬх | 1g | 1g | 1g | 1g |
ЫЎ | 8mL | 6mL | 3mL | 0mL |
СђЫсЃЈ6mol/LЃЉ | 0mL | 2mL | (____)mL | 8mL |
ЯжЯѓ | ЮоЯжЯѓ | ШмвКГЪЧГЛЦЩЋ | ШмвКГЪЛЦТЬЩЋЃЌЩњГЩЧГЛЦТЬЩЋЦјЬх | ШмвКГЪЛЦТЬЩЋЃЌ |
ЂйИУЯЕСаЪЕбщЕФФПЕФ_______________________ЁЃ
ЂкЩеБ3ШЁгУСђЫсЕФЬхЛ§гІЮЊ______________mLЁЃ
ЃЈ5ЃЉИУаЁзщЭЌбЇВщзЪСЯЕУжЊЃКНЋТШЫсМиЙЬЬхКЭХЈбЮЫсЛьКЯвВФмЩњГЩТШЦјЃЌЭЌЪБгаДѓСПClO2ЩњГЩЃЛClO2ЗаЕуЮЊ10ЁцЃЌШлЕуЮЊЃ59ЁцЃЌвКЬхЮЊКьЩЋЃЛCl2ЗаЕуЮЊЃ34ЁцЃЌвКЬЌЮЊЛЦТЬЩЋЁЃЩшМЦзюМђЕЅЕФЪЕбщбщжЄCl2жаКЌгаClO2______________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПMg-H2O2ЕчГиПЩгУгкЧ§ЖЏЮоШЫМнЪЛЕФЧБКНЦїЁЃИУЕчГивдКЃЫЎЮЊЕчНтжЪШмвКЃЌЪОвтЭМШчЯТЁЃИУЕчГиЙЄзїЪБЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ

A. Mg ЕчМЋЪЧИУЕчГиЕФе§МЋ
B. H2O2дкЪЏФЋЕчМЋЩЯЗЂЩњбѕЛЏЗДгІ
C. ЪЏФЋЕчМЋИННќШмвКЕФpH діДѓ
D. ШмвКжаClЃЯђе§МЋвЦЖЏ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈе§ШЗЕФЪЧ
A. МќНЧЃКBF3ЃОCH4ЃОH2OЃОNH3
B. CO2ЁЂHClOЁЂHCHOЗжзгжавЛЖЈМШгаІвМќгжгаІа Мќ
C. вбжЊЗДгІN2O4(l)ЃЋ2N2H4(l) = 3N2(g)ЃЋ4H2O(l)ЃЌШєИУЗДгІжага4 mol NЁЊHМќЖЯСбЃЌдђаЮГЩЕФІаМќЪ§ФПЮЊ1.5NA
D. дкЙшЫсбЮжаЃЌSiO44ЃЫФУцЬхЭЈЙ§ЙВгУЖЅНЧбѕРызгаЮГЩвЛжжЮоЯоГЄЕЅСДНсЙЙЕФЖрЙшЫсИљШчЭМЃЌЦфжаSiдзгЕФдгЛЏЗНЪНгыЭМжаS8ЕЅжЪжаSдзгЕФдгЛЏЗНЪНЯрЭЌ


ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com