
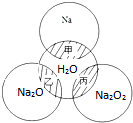
 ��ͼ��ʾ����ԲȦ�ཻ����Ӱ���ּס��ҡ�����ʾԲȦ������������ķ�Ӧ���Ƽ�������������ʵ�����Ϊ0.1mol��ˮ������Ϊ100g������˵����ȷ���ǣ�������
��ͼ��ʾ����ԲȦ�ཻ����Ӱ���ּס��ҡ�����ʾԲȦ������������ķ�Ӧ���Ƽ�������������ʵ�����Ϊ0.1mol��ˮ������Ϊ100g������˵����ȷ���ǣ�������| A���ס��ҡ���������������ԭ��Ӧ |
| B������Ӧ�е���������Na2O2����ԭ��ʱH2O |
| C������Ӧ������1molNa2O2����ת��1mol���� |
| D�����ס��ҡ�����Ӧ��������Һ�����������ֱ�Ϊw1��w2��w3����2w1=w2=w3 |
| 1 |
| 2 |
| 1 |
| 2 |
| 4g |
| 100g+2.2g |
| 8g |
| 100g+6.2g |
| 8g |
| 100g+6.2g |


 ��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д� �����������Ż�ѧϰϵ�д�
�����������Ż�ѧϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2H2O+O2+4e��4OH- |
| B��Fe2++2OH-��Fe��OH��2�� |
| C��Fe-3e��Fe3+ |
| D��4Fe��OH��2+O2+2H2O��4Fe��OH��3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��20�棬101kPa |
| B��0�棬101Pa |
| C��25�棬101kPa |
| D��0�棬101kPa |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��d��e��f |
| B��b��d��e |
| C��b��d��e��f |
| D��b��c��e��f |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
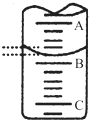 ij�о���С����0.20mol/L NaOH��Һ�ζ�δ֪Ũ�ȵİ״ף�ָʾ��Ϊ��̪����
ij�о���С����0.20mol/L NaOH��Һ�ζ�δ֪Ũ�ȵİ״ף�ָʾ��Ϊ��̪����| �ζ� ���� | ��NaOH��Һ���/mL | |
| �ζ�ǰ����/mL | �ζ������/mL | |
| ��һ�� | 0.02 | 25.00 |
| �ڶ��� | 0.01 | 25.03 |
| ������ | 0.03 | 26.35 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com