
【题目】按要求回答下列问题:
![]() 用浓硫酸给竹筒“刻字”是利用浓硫酸的______性。
用浓硫酸给竹筒“刻字”是利用浓硫酸的______性。
![]() 生产硅酸盐产品水泥和玻璃都需要用到的原料是______。
生产硅酸盐产品水泥和玻璃都需要用到的原料是______。
![]() 从石油中获得汽油、柴油、煤油等燃料,可用______方法分离。
从石油中获得汽油、柴油、煤油等燃料,可用______方法分离。
![]() 清晨,在茂密的树林中,常常可以看到从枝叶间透过的一道道光柱,这种现象在化学上可称为______。
清晨,在茂密的树林中,常常可以看到从枝叶间透过的一道道光柱,这种现象在化学上可称为______。
![]() 溴和碘及其化合物在生产生活中具有广泛的应用,如______可用于人工降雨。
溴和碘及其化合物在生产生活中具有广泛的应用,如______可用于人工降雨。
![]() 、
、![]() 、
、![]() 三者质量之比为1:2:5,则它们的氧原子数之比为______。
三者质量之比为1:2:5,则它们的氧原子数之比为______。
![]() 某金属氯化物
某金属氯化物![]() 中含有
中含有![]() ,则
,则![]() 的摩尔质量为______。
的摩尔质量为______。
![]() 高岭石化学式为
高岭石化学式为![]() ,将其改写成氧化物形式的化学式为______。
,将其改写成氧化物形式的化学式为______。
【答案】脱水 ![]() 蒸馏 丁达尔效应 AgI 1:1:3
蒸馏 丁达尔效应 AgI 1:1:3 ![]()
![]()
【解析】
(1)用浓硫酸给竹筒“刻字”是利用浓硫酸的脱水性;
(2)根据制备水泥和玻璃的原料分析;
(3)汽油、柴油、煤油等沸点不同;
(4)胶体具有丁达尔效应的性质;
(5)碘化银都易见光分解;
(6)根据![]() 计算
计算![]() 、
、![]() 、
、![]() 三者质量之比为1:2:5时含有的氧原子数之比;
三者质量之比为1:2:5时含有的氧原子数之比;
(7)由![]() 的物质的量及
的物质的量及![]() 来确定
来确定![]() 的物质的量,利用
的物质的量,利用![]() 来计算摩尔质量;
来计算摩尔质量;
(8)根据化学式改写成相应的氧化物得形式,按照活泼金属氧化物。较活泼金属氧化物。![]() 得顺序来书写,并要遵守原子守恒来分析解答。
得顺序来书写,并要遵守原子守恒来分析解答。
(1)用浓硫酸给竹筒“刻字”是利用浓硫酸的脱水性,故答案为:脱水;
(2)制备水泥的原料是粘土、石灰石;制备玻璃的原料是纯碱、石灰石、石英,所以都用到![]() ,故答案为:
,故答案为:![]() ;
;
(3)汽油、柴油、煤油等沸点不同,则利用蒸馏法从石油中获得汽油、柴油、煤油等燃料,故答案为:蒸馏;
(4)清晨的雾属于胶体,人们经常看到阳光穿过茂密的森林时产生美丽的景象是胶体的丁达尔现象,和胶体性质有关,故答案为:丁达尔效应;
(5)银颗粒是主要的成像物质,人工降雨其实就是将固态的凝结核打入云层中,要求就是固态微粒越多越好,碘化银可以提供银微粒,效果更好,所以溴化银是一种感光材料,碘化银可用于人工降雨,故答案为:AgI;
(6)根据![]() 可知,
可知,![]() 、
、![]() 、
、![]() 三者质量之比为1:2:5,则
三者质量之比为1:2:5,则![]() 、
、![]() 、
、![]() 的物质的量之比为:
的物质的量之比为:![]() :
:![]() :
:![]() :1:2,它们的氧原子数之比为:
:1:2,它们的氧原子数之比为:![]() :
:![]() :
:![]() :1:3,故答案为:1:1:3;
:1:3,故答案为:1:1:3;
(7)由![]() 含有
含有![]() ,则
,则![]() 的物质的量为
的物质的量为![]() ,则该氯化物的摩尔质量为
,则该氯化物的摩尔质量为![]() ,故答案为
,故答案为![]() ;
;
(8)铝的氧化物为![]() ,硅的氧化物为
,硅的氧化物为![]() ,氢的氧化物为
,氢的氧化物为![]() ,则根据活泼金属氧化物、较活泼金属氧化物、
,则根据活泼金属氧化物、较活泼金属氧化物、![]() 、
、![]() 得顺序可知,
得顺序可知,![]() 可改成
可改成![]() ,故答案为:
,故答案为:![]() 。
。


 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
【题目】(1)有一包白色固体粉末可能为Na2CO3或NaHCO3其中的一种,请设计实验确定该白色粉末的成分________________________________________;
(2)某同学根据CO32-的性质用纯碱溶液、酚酞试剂、氯化钙溶液,设计了一个探究纯碱溶液呈碱性是由CO32--引起的实验方案,主要实验步骤及实验现象为:
① CO32-水解的离子反应方程式为____________________________________________;
② 取少量氯化钙溶液滴入酚酞,不变红色,说明:_____________________________;
③ 取少量碳酸钠溶液,滴入酚酞后显红色,再加入氯化钙溶液的现象为:____________________________。说明_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过实验得出的结论正确的是![]()
A.将固体完全溶于水,滴加稀盐酸,出现白色沉淀,则该固体中存在![]()
B.将气体溶于水,再滴加硝酸银,出现白色沉淀,则该气体为HCl
C.向某无色溶液加NaOH溶液,加热,将湿润的蓝色石蕊试纸靠近试管口,若试纸变红,则说明原溶液中一定含![]()
D.向某无色溶液中滴加NaOH溶液,产生白色沉淀,则该溶液中可能存在![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学与生活、生产的叙述错误的是
A.推广“低碳经济”,减少温室气体的排放
B.利用晶体硅制作的太阳能电池将太阳能直接转化为电能
C.采用催化设施,将汽车尾气中CO和NO转化为无害气体
D.推进小火力发电站的兴建,缓解地方用电困难,促进地方经济的快速发展
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能够跟1mol ![]() 起反应的Br2或H2的最大用量分别是
起反应的Br2或H2的最大用量分别是
A.1mol,1molB.3.5mol,7mol
C.1mol,7molD.6mol,7mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】软锰矿的主要成分是MnO2,还含有少量金属铁、镁、铝、锌、铜的化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上用软锰矿制备碳酸锰并回收硫酸铵,其主要流程如下:

已知金属离子从开始形成氢氧化物沉淀,到沉淀时溶液的pH如下表:
金属离子 | Fe2+ | Fe3+ | Al3+ | Cu2+ | Mn2+ |
开始沉淀pH | 7.5 | 2.7 | 4.1 | 5.9 | 8.8 |
完全沉淀pH | 9.5 | 3.7 | 5.4 | 6.9 | 10.8 |
(1)提高浸出率的可采取的措施有____。
a.适当升高温度 b.搅拌 c.加适量纯碱 d.加压
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,则浸取时发生的主要反应的化学方程式是__________________________。
(3)调节pH为5.4~5.8的目的是______________。
(4)滤渣3的主要成分的化学式是_______。
(5)采用50℃碳化的原因是_________________________________。该过程发生反应的离子方程式是__________________。
(6)检验碳酸锰产品完全洗净的方法是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P akJ·mol—1、P—O bkJ·mol—1、P="O" ckJ·mol—1、O="O " dkJ·mol—1。

根据图示的分子结构和有关数据估算该反应的△H,其中正确的是( )
A. (6a+5d-4c-12b)kJ·mol—1B(4c+12b-6a-5d)kJ·mol—1 B. (4c+12b-4a-5d)kJ·mol—1
C. (4a+5d-4c-12b)kJ·mol—1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】数十年来,化学工作者对氮的氧化物、碳的氧化物做了广泛深入的研究并取得一些重要成果。
I.已知2NO(g)+O2(g) ![]() 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
第一步:2NO(g) ![]() N2O2(g) (快) H1<0;v1正=k1正c2(NO) ;v1逆=k1逆c(N2O2)
N2O2(g) (快) H1<0;v1正=k1正c2(NO) ;v1逆=k1逆c(N2O2)
第二步:N2O2(g)+O2(g) ![]() 2NO2(g) (慢) H2< 0; v2正=k2正c(N2O2)c(O2);v2逆=k2逆c2(NO2)
2NO2(g) (慢) H2< 0; v2正=k2正c(N2O2)c(O2);v2逆=k2逆c2(NO2)
①2NO(g)+O2(g) ![]() 2NO2(g)的反应速率主要是由______(填“第一步”或“第二步”)反应决定。
2NO2(g)的反应速率主要是由______(填“第一步”或“第二步”)反应决定。
②一定温度下,反应2NO(g)+O2(g) ![]() 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=____________;
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=____________;
II.利用CO2和CH4重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放(1)已知重整过程中部分反应的热化方程式为:
① CH4(g)=C(s)+2H2(g) ΔH>0
② CO2(g)+H2(g)=CO(g)+H2O(g) ΔH>0
③ CO(g)+H2(g)=C(s)+H2O(g) ΔH<0
固定n(CO2)=n(CH4),改变反应温度,CO2和CH4的平衡转化率见图甲。
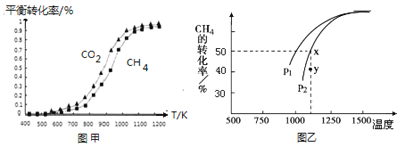
同温度下CO2的平衡转化率________(填“大于”“小于”或“等于”)CH4的平衡转化率。
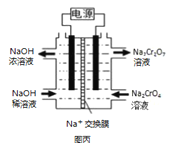
(2)在密闭容器中通入物质的量均为0.1mol的CH4和CO2,在一定条件下发生反应CO2(g) + CH4(g) ![]() 2CO(g) + 2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)_____v(逆)(填“大于”“小于”或“等于”)。已知气体分压(p分)=气体总压(p总)×气体的物质的量分数。用平衡分压代替平衡浓度可以得到平衡常数Kp,求x点对应温度下反应的平衡常数Kp=__________________。
2CO(g) + 2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)_____v(逆)(填“大于”“小于”或“等于”)。已知气体分压(p分)=气体总压(p总)×气体的物质的量分数。用平衡分压代替平衡浓度可以得到平衡常数Kp,求x点对应温度下反应的平衡常数Kp=__________________。
III.根据2CrO42﹣+2H+ ![]() Cr2O72﹣+H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中右侧电极连接电源的__极,电解制备过程的总反应方程式为__。测定阳极液中Na和Cr的含量,若Na与Cr的物质的量之比为a:b,则此时Na2CrO4的转化率为__。若选择用熔融K2CO3作介质的甲醇(CH3OH)燃料电池充当电源,则负极反应式为__。
Cr2O72﹣+H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中右侧电极连接电源的__极,电解制备过程的总反应方程式为__。测定阳极液中Na和Cr的含量,若Na与Cr的物质的量之比为a:b,则此时Na2CrO4的转化率为__。若选择用熔融K2CO3作介质的甲醇(CH3OH)燃料电池充当电源,则负极反应式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化钛在一定波长光的照射下,可有效降解甲醛、苯等有机物,效果持久,且自身对人体无害。某课题组研究了溶液的酸碱性对TiO2光催化染料R降解反应的影响,结果如图所示。下列判断正确的是

A. 在0~50 min之间,R的降解百分率pH=2大于pH=7
B. 溶液酸性越强,R的降解速率越大
C. R的起始浓度不同,无法判断溶液的酸碱性对R的降解速率的影响
D. 在20~25 min之间,pH=10时R的降解速率为0.04 mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com