
| 9g |
| 18g/mol |
| 35.2g |
| 44g/mol |
| 9g |
| 18g/mol |
| 35.2g |
| 44g/mol |
 ��
�� ��
�� ��
�� ��
�� ��
�� ��
�� ��
�� ��
��


 ÿ�α���ϵ�д�
ÿ�α���ϵ�д� ��ѧ����ϵ�д�
��ѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
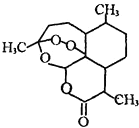 2011���ҹ�Ů��ѧ������������������--һ����������ű����ҩ������ȫ���ر��Ƿ�չ�й��ҵ��������˵��������������ŵ������������ꡱ֮������˹���ٴ�ҽѧ���������ؽṹʽ��ͼ��ʾ����֪һ��̼ԭ��������4����ͬ��ԭ�ӻ���ţ���̼ԭ�ӳơ�����̼ԭ�ӡ��������й������ص�˵������ȷ���ǣ�������
2011���ҹ�Ů��ѧ������������������--һ����������ű����ҩ������ȫ���ر��Ƿ�չ�й��ҵ��������˵��������������ŵ������������ꡱ֮������˹���ٴ�ҽѧ���������ؽṹʽ��ͼ��ʾ����֪һ��̼ԭ��������4����ͬ��ԭ�ӻ���ţ���̼ԭ�ӳơ�����̼ԭ�ӡ��������й������ص�˵������ȷ���ǣ�������| A�������ط�����6������̼ԭ�� |
| B�������صĻ�ѧʽΪ��C15H22O5 |
| C����������һ������������NaOH��Һ��Ӧ������������ |
| D����������֬���Ե� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ˮ����������¶ȶ����Լӿ�þ��ˮ�ķ�Ӧ���� |
| B�����������Ũ�ȿ��Լӿ�п�����ᷴӦ��ȡ���������� |
| C������CaCO3���Լ���CaCO3�ķֽⷴӦ���� |
| D��������̬��Ӧ������ʵ�����δ�������䷴Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
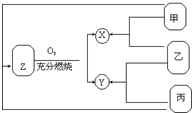 �мס��ҡ������ֳ������ʣ���һ�������¿ɰ���ͼ��ϵת��ΪX��Y��Z���ֳ����Ļ�����ʣ�
�мס��ҡ������ֳ������ʣ���һ�������¿ɰ���ͼ��ϵת��ΪX��Y��Z���ֳ����Ļ�����ʣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ҺPH��7 |
| B���Ի����Һ�����ȣ�K1����K2��С |
| C�����ڻ����Һ��PHֵ�����ԣ����ʱ��Һ��c��Na+���Tc��CH3COO-�� |
| D���¶Ȳ��䣬���ڻ����Һ�м�������NaOH���壬c��CH3COO-����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
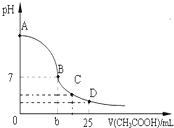 ��25mL 0.1mol/L��NaOH��Һ����μ���0.2mol/L��CH3COOH��Һ����ҺpH�仯������ͼ��ʾ��������������ȷ���ǣ�������
��25mL 0.1mol/L��NaOH��Һ����μ���0.2mol/L��CH3COOH��Һ����ҺpH�仯������ͼ��ʾ��������������ȷ���ǣ�������| A��25��ʱ��A����Һ��ˮ�������C��OH-��=0.1 mol/L |
| B��B��ʱNaOH��Һ��CH3COOH��Һǡ����ȫ��Ӧ |
| C��C��ʱ����Һ������Ũ���ɴ�С��˳���ǣ�C��Na+����C��CH3COO-����C��H+����C��OH-�� |
| D����D��ʱ����Һ��C��CH3COO-��+C��CH3COOH���T2C��Na+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ͨ��ŨH2SO4�� |
| B��ϡH2SO4�������������� |
| C��ŨH2SO4��C2H5OH���ȵ�170�� |
| D����ʪ������ͨ��ʢ��ŨH2SO4��ϴ��ƿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѡ�� | ���� | ���� | ���� |
| A | �������ữ��Ba��NO3��2��Һ��ͨ��SO2 | �а�ɫ�������� | BaSO3�������� |
| B | ���Ũ�ȵ�KCl��KI���Һ�еμ�AgNO3��Һ | �ȳ��ֻ�ɫ���� | Ksp��AgCl����Ksp��AgI�� |
| C | ��������NaOHˮ��Һ���Ⱥ�HNO3�ữ���μ�AgNO3��Һ | ���ֵ���ɫ���� | �����麬��Ԫ�� |
| D | ȡ���õ�Na2O2��ĩ�������еμӹ��������� | ������ɫ���� | Na2O2û�б��� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
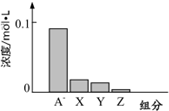 �����£�0.2mol/L ��һԪ�� HA ���Ũ�ȵ� NaOH ��Һ�������Ϻ�������Һ�в�������ּ�Ũ����ͼ��ʾ����ش��������⣺
�����£�0.2mol/L ��һԪ�� HA ���Ũ�ȵ� NaOH ��Һ�������Ϻ�������Һ�в�������ּ�Ũ����ͼ��ʾ����ش��������⣺�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com