
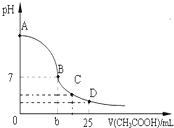
 在25mL 0.1mol/L的NaOH溶液中逐滴加入0.2mol/L的CH3COOH溶液,溶液pH变化曲线如图所示.下列叙述中正确的是( )
在25mL 0.1mol/L的NaOH溶液中逐滴加入0.2mol/L的CH3COOH溶液,溶液pH变化曲线如图所示.下列叙述中正确的是( )| A、25℃时,A点溶液中水电离出的C(OH-)=0.1 mol/L |
| B、B点时NaOH溶液与CH3COOH溶液恰好完全反应 |
| C、C点时,溶液中离子浓度由大到小的顺序是:C(Na+)>C(CH3COO-)>C(H+)>C(OH-) |
| D、在D点时,溶液中C(CH3COO-)+C(CH3COOH)═2C(Na+) |
| 10-14 |
| 0.1 |


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
| A、2.5×1019个 |
| B、2.5×1022个 |
| C、5×1019个 |
| D、5×1022个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、丁达尔现象不是胶体特有的,溶液也具备 |
| B、欲配制1.00 L 1.00 mol?L-1的NaCl溶液,可将58.5g NaCl溶于1.00 L水中 |
| C、质子数为53,中子数为78的碘原子可表示为:131 53I |
| D、煤的干馏和石油的分馏均属化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、为增加明矾净水效果,可同时加入氢氧化钡溶液 |
| B、为了缓解干旱,许多地方使用AgBr人工降雨 |
| C、为防止铁制品生锈,可在铁制品的外层涂油漆 |
| D、计算机硅芯片,光导纤维,普通玻璃都属于硅酸盐产品 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.12 mol |
| B、0.1 mol |
| C、0.11 mol |
| D、0.2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol?L-1的NH4Cl溶液C(Cl-)>C(NH4+)>C(OH-)>C(H+) |
| B、0.1mol?L-1的(NH4)2SO4溶液中:C(NH4+)=2 C(SO42-) |
| C、0.2mol?L-1的Na2CO3溶液中:C(OH-)=C(HCO3-)+C(H+)+C(H2CO3) |
| D、C(NH4+)相等的NH4HSO4溶液,NH4HCO3溶液和NH4Cl溶液中,C(NH4H SO4)<C( NH4Cl)<C(NH4HCO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com