
【题目】已知反应①:CO(g)+CuO(s) CO2(g)+Cu(s)和反应②:H2(g)+CuO(s) Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2该温度下反应③:CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A.反应①的平衡常数K1=![]()
B.对于反应③,恒容时,温度升高,H2浓度减小,则K变大
C.反应③的平衡常数K=![]()
D.对于反应③,恒温恒容下,增大压强,H2浓度一定减小
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,乙醛可发生分解:CH3CHO(l)![]() CH4+CO,已知该反应的活化能为190kJ.mol-1,在含有少量I2的溶液中,该反应的机理为:
CH4+CO,已知该反应的活化能为190kJ.mol-1,在含有少量I2的溶液中,该反应的机理为:
反应Ⅰ:CH3CHO+ I2![]() CH3I2+HI+CO (慢)
CH3I2+HI+CO (慢)
反应Ⅱ:CH3I+HI![]() CH4+ I2
CH4+ I2
下列有关该反应的叙述中正确的是( )
A.反应速率与I2的浓度有关
B.HI在反应Ⅰ中是氧化产物
C.反应焓变的绝对值等于190kJ.mol-1
D.乙醛的反应速率主要取决于反应Ⅱ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是3种物质的溶解度![]() ,下列说法中正确的是
,下列说法中正确的是![]()
物质 |
|
|
|
溶解度 | 74 |
|
|
A.已知![]() 的
的![]()
![]() ,则所有含有固体
,则所有含有固体![]() 的溶液中,都有
的溶液中,都有![]() ,且
,且![]()
![]()
B.除去粗盐中含有的![]() 杂质,最佳除杂试剂为
杂质,最佳除杂试剂为![]() 溶液
溶液
C.将表中三种物质与水混合,加热、灼烧,最终的固体产物相同
D.用石灰水处理含有![]() 和
和![]() 的硬水,发生的离子反应方程式为
的硬水,发生的离子反应方程式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人尿中可以分离出具有生长素效应的化学物质——吲哚乙酸,其结构简式如图所示。下列有关说法正确的是( )

A.吲哚乙酸分子中所有碳原子全部共面
B.吲哚乙酸苯环上的二氯代物共有四种
C.1 mol吲哚乙酸与足量氢气发生反应,最多消耗5 mol H2
D.吲哚乙酸可以发生取代反应、氧化反应和中和反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应热的说法正确的是( )
A.已知甲烷的燃烧热为890.3kJ·mol-1,则表示甲烷燃烧热的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3kJ·mol-1
B.将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6kJ·mol-1
2NH3(g) ΔH=-38.6kJ·mol-1
C.已知C(石墨,s)=C(金刚石,s) ΔH=+1.9kJ·mol-1,说明金刚石具有的能量比石墨低
D.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.4kJ·mol-1,20g氢氧化钠固体溶于稀盐酸中恰好完全反应时放出的热量大于28.7kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答下列问题:
(1)生活中明矾常作净水剂,其净水的原理是___(用离子方程式表示)。
(2)在25℃时,pH等于9和pH等于11的两种氢氧化钠溶液等体积混合后(忽略溶液体积的变化),溶液中的氢离子浓度为___。
(3)现将0.2mol·L-1的NH3·H2O溶液与0.1mol·L-1的HCl溶液等体积混合,写出该混合溶液质子守恒式:___。
(4)FeCl2溶液蒸干并灼烧得到的物质是___(填化学式)。
(5)浓度均为0.1molL﹣1的①H2S、②NaHS、③Na2S、④H2S和NaHS混合液,溶液pH从大到小的顺序是___。(用序号表示)
(6)在常温下,现有下列四种溶液:①0.1mol·L-1 CH3COONH4溶液,②0.1mol·L-1NH4HSO4溶液,③0.1mol·L-1 NH3·H2O和0.1mol·L-1 NH4Cl混合溶液,④0.1mol·L-1 NH3·H2O溶液。比较①、②、③、④溶液中c(NH4+)由小到大的顺序为___(用序号表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组借助![]() 的仪器装置完成有关实验。
的仪器装置完成有关实验。

(1)用装置A收集NO气体,正确的操作是 ______ ![]() 填序号
填序号![]() 。
。
a.从①口进气,用排水法集气
b.从①口进气,用排气法集气
c.从②口进气,用排水法集气
d.从②口进气,用排气法集气
(2)B装置中的恒压分液漏斗有两个作用,其一是平衡气压使分液漏斗内的液体能顺利滴下,其另一个作用是 ______。
(3)三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校一化学实验小组通过实验来探究一红色粉末是![]() 、
、![]() 或二者混合物。探究过程如下:
或二者混合物。探究过程如下:
查阅资料:
![]() 是一种碱性氧化物,溶于稀硫酸生成Cu和
是一种碱性氧化物,溶于稀硫酸生成Cu和![]() ,在空气中加热生成CuO
,在空气中加热生成CuO
提出假设:
假设1:红色粉末是![]()
假设2:红色粉末是![]()
假设3:红色粉末是![]() 和
和![]() 的混合物
的混合物
设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN试剂。
①若滴加KSCN试剂后溶液不变红色,甲同学认为原固体粉末中一定不含三氧化二铁.乙同学认为其结论不正确,乙同学的理由是 ______。
②若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则证明原固体粉末是 ______。
![]() 经分析,确定红色粉末为
经分析,确定红色粉末为![]() 和
和![]() 的混合物.实验小组欲利用该红色粉末制取较纯净的胆矾
的混合物.实验小组欲利用该红色粉末制取较纯净的胆矾![]() 。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使
。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使![]() 、
、![]() 、
、![]() 分别生成沉淀的pH如下:
分别生成沉淀的pH如下:
物质 |
|
|
|
开始沉淀pH | 6.0 |
|
|
沉淀完全pH | 13 | 14 |
|
实验室有下列试剂可供选择:![]() 氯水
氯水 ![]()
![]()
![]()
实验小组设计如下实验方案:
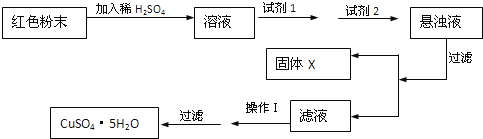
试回答:
①试剂为1____ ![]() 填字母
填字母![]() ,写出溶液中发生反应的离子方程式
,写出溶液中发生反应的离子方程式![]() 写出一个即可
写出一个即可![]() ___。
___。
②试剂为2______ ![]() 填字母
填字母![]() 。
。
③固体X的化学式为 ______。
④操作I为 ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某气态化石燃料X中只含有碳、氢两种元素,为探究该气体中碳和氢两种元素的质量比,某同学设计了燃烧法测量的实验方案,通过测量装置C和D的增重即可求得碳和氢两种元素的质量比.实验装置如下图所示![]() 已知CuO可以作为碳氢化合物燃烧的催化剂
已知CuO可以作为碳氢化合物燃烧的催化剂![]() :
:

(1)若A装置中所盛放的药品是浓NaOH溶液,装置A的作用有:
①______;
②______
(2)D装置中所盛放的药品是______,
(3)E装置的作用是______,
(4)上述装置中有一处缺陷,请改正______.
(5)若实验装置经过改正后,得到的实验数据如下:
质量 | 实验前 | 实验后 |
药品 |
|
|
药品 |
|
|
则该气体中碳和氢两种元素的质量比为______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.HF在水溶液中的电离方程式:HF+H2O![]() F-+H3O+
F-+H3O+
B.向0.1 mol·L-1氨水中加入少量水,溶液中![]() 减少
减少
C.将NH4Cl溶液从20℃升温至30℃,溶液中![]() 增大
增大
D.CH3COOK水解的离子方程式:CH3COO-+H2O=CH3COOH+OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com