
����Ŀ��Ϊ̽�������Ļ�ԭ�ԣ�ijͬѧ���������ʵ��װ��( ���мг�װ����ȥ)����ʵ�����н���ʵ��̽�����ش���������:
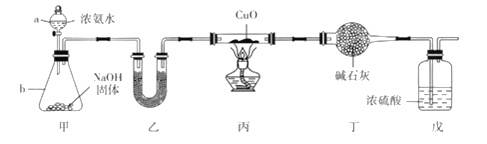
��1������b��������_____________________���Խ���װ���в���NH3��ԭ��:____________��
��2��װ������ʢ�е��Լ�������__________________��
��3��װ������Ũ�����������_______________________________________________��
��4��+1��Cu �����Ի����в��ȶ����ɷ�����Ӧ:Cu2O+2H+==Cu2++Cu + H2O��ijͬѧȡ������Ӧ�������ڵ��������Թ��У�����ϡ���ᣬ������ҺΪ��ɫ�����Թܵײ��к�ɫCu�����ó�����:NH3��ԭCuO����Cu2O����ͬѧ���ж��Ƿ���ȷ?________(������ȷ����������ȷ��)��������__________________________________________________________________��
��5����֪װ�ñ��IJ�������CuO��ĩΪmg��ʵ��������ò������ڹ����ĩΪn g����CuO ��ȫ����ԭ Ϊ Cu���� m:n=______��д���������ڷ�����Ӧ�Ļ�ѧ����ʽ:__________________��װ�ö��еĸ��������Ϊ_______g(�ú�m ��n �Ĵ���ʽ��ʾ)��
���𰸡� ��ƿ NH3+H2O![]() NH3��H2O
NH3��H2O![]() NH4++OH-��NaOH �ڰ�ˮ�е������OH-��ʹƽ�������ƶ�����NaOH�ܽ���� ��ʯ�� ����NH3β������ֹ�����е�ˮ��������װ�ö� ����ȷ ����Ӧ����ȫ���������л����CuO ��Cu����ϡ����Ҳ������ͭ�κ�Cu 5:4 3CuO+2NH3
NH4++OH-��NaOH �ڰ�ˮ�е������OH-��ʹƽ�������ƶ�����NaOH�ܽ���� ��ʯ�� ����NH3β������ֹ�����е�ˮ��������װ�ö� ����ȷ ����Ӧ����ȫ���������л����CuO ��Cu����ϡ����Ҳ������ͭ�κ�Cu 5:4 3CuO+2NH3![]() 3Cu+3H2O+N2 9/8(m-n)��9n/32��9m/40
3Cu+3H2O+N2 9/8(m-n)��9n/32��9m/40
������������ʵ��Ŀ����̽�������Ļ�ԭ�������������ͼ��֪������Ũ��ˮ���������ƹ������÷ų������������ҵĸ���õ�����İ������ڱ���������ͭ��Ӧ����ͭ�͵������Լ�ˮ�������������������ɵ�ˮ����������Ũ�����������δ��Ӧ�İ�������ֹ��Ⱦ��ͬʱ���Է�ֹ�����е�ˮ��������װ�ö���
(1)����װ��ͼ������bΪ��ƿ����װ����NH3+H2O![]() NH3��H2O
NH3��H2O![]() NH4++OH-��NaOH�ڰ�ˮ�е������OH-��ʹƽ�������ƶ�����NaOH�ܽ���ȣ�ʹ��ˮ�ֽ⣬�ų��������ʴ�Ϊ����ƿ��NH3+H2O
NH4++OH-��NaOH�ڰ�ˮ�е������OH-��ʹƽ�������ƶ�����NaOH�ܽ���ȣ�ʹ��ˮ�ֽ⣬�ų��������ʴ�Ϊ����ƿ��NH3+H2O![]() NH3��H2O
NH3��H2O![]() NH4++OH-��NaOH�ڰ�ˮ�е������OH-��ʹƽ�������ƶ�����NaOH�ܽ���ȣ�
NH4++OH-��NaOH�ڰ�ˮ�е������OH-��ʹƽ�������ƶ�����NaOH�ܽ���ȣ�
(2)װ���ҵ������Ǹ��ﰱ��������ѡ�ü�ʯ�ң��ʴ�Ϊ����ʯ�ң�
(3)װ������Ũ�����������NH3β������ֹ�����е�ˮ��������װ�ö����ʴ�Ϊ������NH3β������ֹ�����е�ˮ��������װ�ö���
(4)+1��Cu�����Ի����в��ȶ����ɷ�����Ӧ:Cu2O+2H+==Cu2++Cu+H2O��ijͬѧȡ������Ӧ�������ڵ��������Թ��У�����ϡ���ᣬ������ҺΪ��ɫ�����Թܵײ��к�ɫCu�����ó�������NH3��ԭCuO����Cu2O����ͬѧ���жϲ���ȷ����Ϊ���練Ӧ����ȫ���������л����CuO��Cu����ϡ����Ҳ������ͭ�κ�Cu���ʴ�Ϊ������ȷ������Ӧ����ȫ���������л����CuO��Cu����ϡ����Ҳ������ͭ�κ�Cu��
(5)��֪װ�ñ��IJ�������CuO��ĩΪmg��ʵ��������ò������ڹ����ĩΪng����CuO��ȫ����ԭΪCu������ͭԪ���غ㣬��m:n=![]() =
=![]() ���������ڷ�����Ӧ�Ļ�ѧ����ʽΪ3CuO+2NH3
���������ڷ�����Ӧ�Ļ�ѧ����ʽΪ3CuO+2NH3![]() 3Cu+3H2O+N2��װ�ö��еĸ�������յ���ˮ����������Ϊmg��
3Cu+3H2O+N2��װ�ö��еĸ�������յ���ˮ����������Ϊmg��![]() ��
��![]() =
=![]() g���ʴ�Ϊ��5:4��3CuO+2NH3
g���ʴ�Ϊ��5:4��3CuO+2NH3![]() 3Cu+3H2O+N2��
3Cu+3H2O+N2��![]() ��9/8(m-n)��9n/32��
��9/8(m-n)��9n/32��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��SO2����������Fe2(SO4)3��Һ��ȫ��Ӧ���ټ���K2Cr2O7��Һ����������������ѧ��Ӧ��
��SO2��2Fe3����2H2O��SO42-��2Fe2����4H����
��Cr2O72-��6Fe2����14H����2Cr3����6Fe3����7H2O��
�����й�˵���������
A. �����ԣ�Cr2O72->Fe3��>SO2
B. K2Cr2O7�ܽ�Na2SO3������Na2SO4
C. ÿ��1 mol K2Cr2O7�μӷ�Ӧ��ת�Ƶ��ӵ���ĿΪ6NA
D. ����6.72 L SO2(��״��)�μӷ�Ӧ������������0.2 mol K2Cr2O7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ˮ�е����������������˵������ȷ����
A. c(H��)��c(OH��)����
B. pH������
C. ˮ�ĵ���̶�������
D. ˮ�������c(H��)������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�������һ�����ʵ���Ũ�ȵ���Һʱ�����в�����ʹ��õ���ҺŨ��ƫС����
A. ����Ͳ��ȡŨ����ʱ����Һ��
B. ��Һ���ձ�ת�Ƶ�����ƿ�к�û��ϴ���ձ�
C. ����ʱ����Һ��
D. �ý�ͷ�ιܼ�ˮʱ��������ˮ�ε�����ƿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ѱ�(TiO2)����Ҫ�İ�ɫ������LiFePO4������ӵ�ص��������ϡ�һ������������( ��Ҫ�ɷ�ΪFeTiO3 ������Fe2O3 )�����Ѱۺ�LiFePO4 ������������������ͼ��ʾ:

�ش���������:
��1�� LiFePO4��Fe�Ļ��ϼ���_______________________��
��2����������������ǰ��Ҫ���з����������Ŀ����__________________________________��
��3�������ӷ���ʽ��ʾ����I�������۵�Ŀ��:__________________________������IIΪһϵ�в����������Ǽ���Ũ������ȴ�ᾧ�������������õ����մ�������������___________��
��4��TiO2+��ˮ��������ˮ������ӷ���ʽΪ______________________����ת�������õ���TiO2+��ˮ���������Ҫ����Һ���ȣ����ȵ�Ŀ����________________________________��
��5�����������ĵ���ʹFe3+����FePO4������Һ��c(PO43-)= 1.0��10-17mol/Lʱ����ΪFe3+ ������ȫ������Һ��Fe3+������ȫʱ��c(Fe3+)=_______mol/L[��֪:���¶�����Ksp(FePO4)=1.0��10-22]��
��6���������������Ʊ�LiFePO4�Ĺ����У�����17% H2O2��Һ�����( H2C2O4)����������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ǽ���ԭ�ӵĻ�̬�����Ų�����һ����������ԭ����( )
A. 1s22s22p6 B. 1s22s22p63s23p3
C. 1s22s22p63s23p2 D. 1s22s22p63s23p64s2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л��������˵����ȷ����
A. ����Ķ���ȡ������3��
B. ![]() �ͱ���ϩ��Ϊͬϵ��
�ͱ���ϩ��Ϊͬϵ��
C. ����(NH4)2SO4��Һ�������־���ʹ��������Һ������������ԭ����ͬ
D. �ۺ���(![]() )���ɵ���CH3CH��CH2��CH2��CH2�Ӿ��Ƶ�
)���ɵ���CH3CH��CH2��CH2��CH2�Ӿ��Ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡŨ����ȵ�NaOH��HCl��Һ����3��2��������ͣ�������Һ�е�c(OH��)��0.01 mol/L����ԭ��Һ��Ũ��Ϊ(����)
A.0.01 mol/LB.0.017 mol/LC.0.05 mol/LD.0.50 mol/L
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com