
ЎҫМвДҝЎҝO2әНO3КЗСхФӘЛШөДБҪЦЦөҘЦКЈ¬ёщҫЭЖд·ЦЧУКҪНкіЙПВБРёчМвЈә
(1)өИОВөИС№ПВЈ¬өИЦКБҝөДO2әНO3Лщә¬·ЦЧУёцКэұИОӘ________Ј¬ФӯЧУёцКэұИОӘ________Ј¬Ме»эЦ®ұИОӘ________ЎЈ
(2)ЙиNAОӘ°ў·ьјУөВВЮіЈКэөДКэЦөЈ¬Из№ыa gСхЖшЦРә¬УРөД·ЦЧУКэОӘbЈ¬Фтc gСхЖшФЪұкЧјЧҙҝцПВөДМе»эФјКЗ________(УГә¬NAөДКҪЧУұнКҫ)ЎЈ
(3)ЕдЦЖ500 mL 1 mol/LөДПЎH2SO4ИЬТәЈ¬РиТӘУГБҝНІБҝИЎЕЁH2SO4(ГЬ¶ИОӘ1.84 g/mLЈ¬ЦКБҝ·ЦКэОӘ98%)өДМе»эОӘ________ mLЎЈ
Ўҫҙр°ёЎҝ3Јә2 1Јә1 3Јә2 ![]() L 27.2
L 27.2
ЎҫҪвОцЎҝ
(1)ёщҫЭn=![]() јЖЛгЖшМеөДОпЦКөДБҝЈ¬И»әуёщҫЭN=nЎӨNAјЖЛг·ЦЧУКэДҝЈ¬n=
јЖЛгЖшМеөДОпЦКөДБҝЈ¬И»әуёщҫЭN=nЎӨNAјЖЛг·ЦЧУКэДҝЈ¬n=![]() јЖЛгЖшМеә¬УРФӯЧУөДОпЦКөДБҝЈ»ФЩёщҫЭV=nЎӨVmјЖЛгЖшМеөДМе»эЈ»
јЖЛгЖшМеә¬УРФӯЧУөДОпЦКөДБҝЈ»ФЩёщҫЭV=nЎӨVmјЖЛгЖшМеөДМе»эЈ»
(2)ПИјЖЛгc g O2ә¬УРөДЖшМе·ЦЧУКэЈ¬И»әуёщҫЭn=![]() ј°V=nЎӨVmјЖЛгЖшМеөДМе»эЈ»
ј°V=nЎӨVmјЖЛгЖшМеөДМе»эЈ»
(3)ёщҫЭc=![]() јЖЛгіцИЬТәөДЕЁ¶ИЈ¬И»әуёщҫЭПЎКН¶ЁВЙcЕЁЎӨVЕЁ=cПЎЎӨVПЎАҙјЖЛгЎЈ
јЖЛгіцИЬТәөДЕЁ¶ИЈ¬И»әуёщҫЭПЎКН¶ЁВЙcЕЁЎӨVЕЁ=cПЎЎӨVПЎАҙјЖЛгЎЈ
(1)јЩЙиЖшМеөДЦКБҝОӘmЈ¬УЙn(O2)=![]() Ј»n(O3)=
Ј»n(O3)=![]() Ј¬ЛщТФөИОВөИС№ПВЈ¬өИЦКБҝөДO2әНO3өДОпЦКөДБҝөДұИОӘn(O2)Јәn(O3)=
Ј¬ЛщТФөИОВөИС№ПВЈ¬өИЦКБҝөДO2әНO3өДОпЦКөДБҝөДұИОӘn(O2)Јәn(O3)=![]() Јә
Јә![]() =3Јә2Ј¬ёщҫЭN=nЎӨNAҝЙЦӘЖшМеөДОпЦКөДБҝУлЖдә¬УРөДЖшМе·ЦЧУКэіКХэұИЈ¬ЛщТФN(O2)ЈәN(O3)= n(O2)Јәn(O3)=3Јә2Ј»
=3Јә2Ј¬ёщҫЭN=nЎӨNAҝЙЦӘЖшМеөДОпЦКөДБҝУлЖдә¬УРөДЖшМе·ЦЧУКэіКХэұИЈ¬ЛщТФN(O2)ЈәN(O3)= n(O2)Јәn(O3)=3Јә2Ј»
O2ЎўO3¶јКЗУЙOФӯЧУ№№іЙЈ¬OФӯЧУөДЦКБҝЎўДҰ¶ыЦКБҝПаН¬Ј¬ТтҙЛУЙn=![]() ҝЙЦӘөИОВөИС№ПВЈ¬өИЦКБҝөДO2әНO3Лщә¬ФӯЧУёцКэПаН¬Ј¬ТтҙЛә¬УРөДФӯЧУКэөДұИОӘ1Јә1Ј»
ҝЙЦӘөИОВөИС№ПВЈ¬өИЦКБҝөДO2әНO3Лщә¬ФӯЧУёцКэПаН¬Ј¬ТтҙЛә¬УРөДФӯЧУКэөДұИОӘ1Јә1Ј»
ёщҫЭV=nЎӨVmҝЙЦӘЖшМеөДМе»эУлЖшМеөДОпЦКөДБҝіКХэұИЈ¬УЙУЪn(O2)Јәn(O3) =3Јә2Ј¬ЛщТФV(O2)ЈәV(O3) =3Јә2Ј»
(2)a gСхЖшЦРә¬УРөД·ЦЧУКэОӘbЈ¬Фтc g O2ә¬УРөДЖшМе·ЦЧУКэN(O2)=![]() Ј¬ФтёщҫЭn=
Ј¬ФтёщҫЭn=![]() ҝЙЦӘO2өДОпЦКөДБҝОӘn(O2)=
ҝЙЦӘO2өДОпЦКөДБҝОӘn(O2)=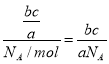 molЈ¬ЛщТФёГСхЖшФЪұкЧјЧҙҝцПВөДМе»эV=nЎӨVm=
molЈ¬ЛщТФёГСхЖшФЪұкЧјЧҙҝцПВөДМе»эV=nЎӨVm=![]() molЎБ22.4 L/mol=
molЎБ22.4 L/mol=![]() LЈ»
LЈ»
(3)ГЬ¶ИОӘ1.84 g/mLЈ¬ЦКБҝ·ЦКэОӘ98%өДЕЁH2SO4өДОпЦКөДБҝЕЁ¶Иc=![]() mol/L=18.4 mol/LЈ¬ёщҫЭПЎКН№«КҪҝЙөГЈә18.4 mol/LЎБV=500 mLЎБ1 mol/LЈ¬ҪвөГV=27.2 mLЎЈ
mol/L=18.4 mol/LЈ¬ёщҫЭПЎКН№«КҪҝЙөГЈә18.4 mol/LЎБV=500 mLЎБ1 mol/LЈ¬ҪвөГV=27.2 mLЎЈ


 ҝЪЛгРДЛгЛЩЛгУҰУГМвПөБРҙр°ё
ҝЪЛгРДЛгЛЩЛгУҰУГМвПөБРҙр°ё Н¬ІҪНШХ№ФД¶БПөБРҙр°ё
Н¬ІҪНШХ№ФД¶БПөБРҙр°ё
| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДіРЛИӨРЎЧйөДН¬С§ЙијЖКөСйЦЖұёCuBr(°ЧЙ«Ҫбҫ§РФ·ЫД©Ј¬ОўИЬУЪЛ®Ј¬І»ИЬУЪТТҙјөИУР»ъИЬјБ)Ј¬КөСйЧ°ЦГ(јРіЦЎўјУИИТЗЖчВФ)ИзНјЛщКҫЎЈ
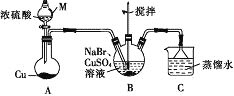
(1)ТЗЖчMөДГыіЖКЗ________ЎЈ
(2)ИфҪ«MЦРөДЕЁБтЛб»»іЙ70%өДH2SO4Ј¬ФтФІөЧЙХЖҝЦРөД№ММеКФјБОӘ______(Мо»ҜС§КҪ)ЎЈ
(3)BЦР·ўЙъ·ҙУҰөД»ҜС§·ҪіМКҪОӘ_______Ј¬ДЬЛөГчBЦР·ҙУҰТСНкіЙөДТАҫЭКЗ_____ЎЈИфBЦРCu2+ИФОҙНкИ«ұ»»№ФӯЈ¬ККТЛјУИлөДКФјБКЗ_______(МоұкәЕ)ЎЈ
a.Тәде b.Na2SO4 c.Мъ·Ы d.Na2S2O3
(4)ПВБР№ШУЪ№эВЛөДРрКцІ»ХэИ·өДКЗ_______ (МоұкәЕ)ЎЈ
a.В©¶·Д©¶ЛҫұјвҝЙТФІ»ҪфҝҝЙХұӯұЪ
b.Ҫ«ВЛЦҪИуКӘЈ¬К№ЖдҪфМщВ©¶·ДЪұЪ
c.ВЛЦҪұЯФөҝЙТФёЯіцВ©¶·ҝЪ
d.УГІЈБ§°фФЪВ©¶·ЦРЗбЗбҪБ¶ҜТФјУҝм№эВЛЛЩВК
(5)ПҙөУКұЈ¬ПИУГЧ°ЦГCЦРөДОьКХТәЗеПҙЈ¬ЖдДҝөДКЗ_______Ј¬ФЩТАҙОУГИЬҪвSO2өДТТҙјЎўТТГСПҙөУөДДҝөДКЗ________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБР·ҪіМКҪХэИ·өДКЗ
A. AlCl3ИЬТәЦРјУИл№эБҝ°ұЛ®ЈәAl3++4NH3ЎӨH2OЈҪAlO2-+2H2O+4NH4+
B. МјЛбөДөзАл·ҪіМКҪЈәH2CO3![]() 2H++CO32-
2H++CO32-
C. јЧНйөДұкЧјИјЙХИИОӘ890.3 kJЎӨmol-1Ј¬ФтјЧНйИјЙХөДИИ»ҜС§·ҪіМКҪҝЙұнКҫОӘЈәCH4(g)+2O2(g)ЈҪCO2(g)+2H2O(g) ЎчH=-890.3kJЎӨmol-1
D. ПтFe(NO3)2ПЎИЬТәЦРјУИлСОЛбЈә3Fe2Ј«+4HЈ«+NO3ЈӯЈҪ3Fe3Ј«+NOЎь+2H2O
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРЛө·ЁЦРЈ¬ХэИ·өДКЗЈЁ Ј©
A.1molОпЦКҫщФјә¬УР6.02ЎБ1023ёц·ЦЧУB.6.02ЎБ1023ёцЗв·ЦЧУҫНКЗ1mol H2
C.1gH2Ул1mol H2Лщә¬·ЦЧУКэПаөИD.1mol H2OУл1molH2SO4өДЦКБҝПаөИ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝіхЦР»ҜС§ЦӘК¶ёҙП°Јә
(1)°ҙТӘЗуМоҝХ
HCOOHЦРCөД»ҜәПјЫ_________Ј»K2MnO4ЦРMnөД»ҜәПјЫ________Ј»
FeCl2өДГыіЖКЗ_________Ј»ФӯЧУРтКэОӘ18өДФӘЛШөД·ыәЕКЗ________Ј»
(2)°ҙТӘЗуёчРҙіцТ»ёц»ҜС§·ҪіМКҪЈә
»ҜәП·ҙУҰЈә_____________Ј»·ЦҪв·ҙУҰЈә_____________Ј»
ЦГ»»·ҙУҰЈә_____________Ј»ёҙ·ЦҪв·ҙУҰЈә_____________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝNOУГНҫ№г·әЈ¬¶ФЖдҪшРРСРҫҝҫЯУРЦШТӘөДјЫЦөәНТвТе
ЈЁ1Ј©2NOЈЁgЈ©+O2ЈЁgЈ©=2NO2ЈЁgЈ©ЎчH=akJmol-1өД·ҙУҰАъіМУлДЬБҝұд»Ҝ№ШПөИзНјЛщКҫЎЈТСЦӘЈәөЪўтІҪ·ҙУҰОӘЈәNO3ЈЁgЈ©+NOЈЁgЈ©=2NO2ЈЁgЈ©ЎчH=bkJmol-1
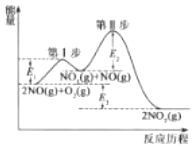
ўЩөЪIІҪ·ҙУҰөДИИ»ҜС§·ҪіМКҪОӘ__ЎЈ
ўЪ№ШУЪ2NOЈЁgЈ©+O2ЈЁgЈ©=2NO2ЈЁgЈ©өД·ҙУҰАъіМЈ¬ПВБРЛө·ЁХэИ·өДКЗ__ЎЈ
AЈ®ПаН¬МхјюПВЈ¬ҫц¶ЁёГ·ҙУҰҝмВэөДІҪЦиОӘөЪўтІҪ·ҙУҰ
BЈ®К№УГәПККөДҙЯ»ҜјБ»бК№E1ЎўE2ЎўE3Н¬КұјхРЎ
CЈ®өЪIІҪ·ҙУҰОӘОьИИ·ҙУҰЈ¬өЪўтІҪ·ҙУҰОӘ·ЕИИ·ҙУҰ
DЈ®·ҙУҰөДЦРН¬ІъОпКЗNO3әНNO
ЈЁ2Ј©NOөДЗв»Ҝ»№Фӯ·ҙУҰОӘ2NOЈЁgЈ©+2H2ЈЁgЈ©N2ЈЁgЈ©+2H2OЈЁgЈ©ЎЈСРҫҝұнГчЈәДіОВ¶ИКұЈ¬vХэ=kcmЈЁNOЈ©cnЈЁH2Ј©Ј¬ЖдЦРk=2.5ЎБ103molЈЁm+n-1Ј©LЈЁm+n-1Ј©s-1Ј®ёГОВ¶ИПВЈ¬өұcЈЁH2Ј©=4.0ЎБ10-3molL-1КұЈ¬КөСйІвөГvХэУлcЈЁNOЈ©өД№ШПөИзНјТ»ЛщКҫЈ¬Фтm=___Ј¬n=___ЎЈ
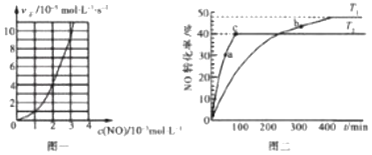
ЈЁ3Ј©NOТЧ·ўЙъ¶юҫЫ·ҙУҰ2NOЈЁgЈ©N2O2ЈЁgЈ©ЎЈФЪПаН¬өДёХРФ·ҙУҰЖчЦРідИлөИБҝөДNOЈ¬·Цұр·ўЙъёГ·ҙУҰЎЈІ»Н¬ОВ¶ИПВЈ¬NOөДЧӘ»ҜВКЛжКұјдЈЁtЈ©өДұд»Ҝ№ШПөИзНј¶юЛщКҫЎЈ
ўЩёГ·ҙУҰөДЎчH___0ЈЁМоЎ°ЈҫЎұЎ°ЈјЎұ»тЎ°=ЎұЈ©ЎЈ
ўЪT1ОВ¶ИПВЈ¬УыМбёЯNOөДЖҪәвЧӘ»ҜВКЈ¬ҝЙІЙИЎөДҙлК©ОӘ__ЈЁИОРҙТ»МхјҙҝЙЈ©ЎЈ
ўЫaЎўbҙҰХэ·ҙУҰЛЩВКva__vbЈЁМоЎұЈҫЎұЎ°ЈјЎұ»тЎ°=ЎұЈ©Ј¬ФӯТтОӘ___ЎЈ
ўЬeөг¶ФУҰМеПөөДЧЬС№ЗҝОӘ200kPaЈ¬ФтT2ОВ¶ИПВЈ¬ёГ·ҙУҰөДЖҪәвіЈКэkp=___kPa-1ЈЁKpОӘТФ·ЦС№ұнКҫөДЖҪәвіЈКэЈ©
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝҪрКфовФЪ№ӨТөәН№ъ·АҪЁЙиЦРУРЦШТӘөДЧчУГЎЈов(Mo)өДіЈјы»ҜәПјЫОӘ+6Ўў+5Ўў+4ЎЈУЙовҫ«ҝу(ЦчТӘіЙ·ЦКЗMoS2)ҝЙЦЖұёөҘЦКовәНовЛбДЖҫ§Ме(Na2MoO4ЎӨ2H2O)Ј¬Іҝ·ЦБчіМИзНј1ЛщКҫЈә
ТСЦӘЈәовЛбОўИЬУЪЛ®Ј¬ҝЙИЬУЪТәјоәН°ұЛ®ЎЈ
»ШҙрПВБРОКМвЈә
ЈЁ1Ј©ұәЙХовҫ«ҝуКұ·ўЙъөД»ҜС§·ҪіМКҪОӘ_____________________________ЎЈ
ЈЁ2Ј©овҫ«ҝуұәЙХКұЕЕ·ЕөДОІЖш¶Ф»·ҫіөДЦчТӘОЈәҰКЗ___________________Ј¬ЗлМбіцТ»ЦЦКөСйКТіэИҘёГОІЖшөД·Ҫ·Ё____________________________________ЎЈ
ЈЁ3Ј©ІЩЧч2өДГыіЖОӘ________ЎЈУЙовЛбөГөҪMoO3ЛщУГөҪөД№иЛбСОІДБПТЗЖчөДГыіЖКЗ________ЎЈ
ЈЁ4Ј©ұәЙХовҫ«ҝуЛщУГөДЧ°ЦГКЗ¶аІгұәЙХВҜЈ¬Нј2ОӘёчВҜІг№ММеОпБПөДОпЦКөДБҝөД°Щ·ЦКэ(ҰХ)ЎЈ
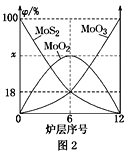
ўЩxЈҪ________ЎЈ
ўЪұәЙХВҜЦРТІ»б·ўЙъMoS2УлMoO3·ҙУҰЙъіЙMoO2әНSO2өД·ҙУҰЈ¬ИфёГ·ҙУҰЧӘТЖ6molөзЧУЈ¬ФтПыәДөДСх»ҜјБөД»ҜС§КҪј°ОпЦКөДБҝ·ЦұрОӘ________Ўў________ЎЈ
ЈЁ5Ј©ІЩЧч1ЦРЈ¬јУИлМјЛбДЖИЬТәід·Ц·ҙУҰәуЈ¬јоҪюТәЦРc(MoO42-)ЈҪ0.80molЎӨL1Ј¬c(SO42-)ЈҪ0.04 molЎӨL1Ј¬ФЪҪбҫ§З°РијУИлBa(OH)2№ММеТФіэИҘИЬТәЦРөДSO42-ЎЈөұBaMoO4ҝӘКјіБөнКұЈ¬SO42-өДИҘіэВККЗ________ЎЈ[Ksp(BaSO4)ЈҪ1.1ЎБ1010ЎўKsp(BaMoO4)ЈҪ4.0ЎБ108Ј¬ИЬТәМе»эұд»ҜҝЙәцВФІ»јЖ]
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ¶юВИ»Ҝ¶юБт(S2Cl2)КЗТ»ЦЦЦШТӘөД»Ҝ№ӨФӯБП,іЈУГЧчПрҪәБт»ҜјБ,ёДұдЙъПрҪәКЬИИ·ўХіЎўУцАдұдУІөДРФЦКЎЈІйФДЧКБПҝЙЦӘS2Cl2ҫЯУРПВБРРФЦК:
ОпАнРФЦК | ¶ҫРФ | Й«М¬ | »У·ўРФ | ИЫөг | ·Рөг |
ҫз¶ҫ | Ҫр»ЖЙ«ТәМе | ТЧ»У·ў | -76Ўж | 138Ўж | |
»ҜС§РФЦК | ўЩ300 ЎжТФЙПНкИ«·ЦҪв ўЪS2Cl2Ј«Cl2 ўЫУцёЯИИ»тУлГч»рҪУҙҘ,УРТэЖрИјЙХөДОЈПХ ўЬКЬИИ»тУцЛ®·ЦҪв·ЕИИ,·ЕіцёҜКҙРФСМЖш | ||||
(1)ЦЖИЎЙЩБҝS2Cl2
КөСйКТҝЙАыУГБтУлЙЩБҝВИЖшФЪ110~140Ўж·ҙУҰЦЖөГS2Cl2ҙЦЖ·Ј¬ВИЖш№эБҝФт»бЙъіЙSCl2ЎЈ

ўЩТЗЖчm өДГыіЖОӘ__________,Ч°ЦГF ЦРКФјБөДЧчУГКЗ_________ЎЈ
ўЪЧ°ЦГБ¬ҪУЛіРт: A![]() ______
______![]()
![]()
![]() E
E![]() DЎЈ
DЎЈ
ўЫКөСйЗ°ҙтҝӘK1,НЁИлТ»¶ОКұјдөДөӘЖшЕЕҫЎЧ°ЦГДЪҝХЖшЎЈКөСйҪбКшНЈЦ№јУИИәуЈ¬ФЩНЁИлТ»¶ОКұјдөДөӘЖш,ЖдДҝөДКЗ_____________ЎЈ
ўЬОӘБЛМбёЯS2Cl2өДҙҝ¶И,КөСйөД№ШјьКЗҝШЦЖәГОВ¶ИәН____________ЎЈ
(2)ЙЩБҝS2Cl2Р№В©КұУҰЕзЛ®ОнјхВэЖд»У·ў(»тА©Йў),ІўІъЙъЛбРФРьЧЗТә,ө«І»ТӘ¶ФР№В©Оп»тР№В©өгЦұҪУЕзЛ®,ЖдФӯТтКЗ______________ЎЈ
(3)S2Cl2УцЛ®»бЙъіЙSO2ЎўHClБҪЦЦЖшМе,ДіН¬С§ЙијЖБЛИзПВКөСй·Ҫ°ёАҙІв¶ЁёГ»мәПЖшМеЦРSO2өДМе»э·ЦКэЎЈ

ўЩWИЬТәҝЙТФКЗ_____(МоұкәЕ)ЎЈ
a.H2O2ИЬТә b.KMnO4ИЬТә(БтЛбЛб»Ҝ) c.ВИЛ®
ўЪёГ»мәПЖшМеЦР¶юСх»ҜБтөДМе»э·ЦКэОӘ_________(УГә¬VЎўm өДКҪЧУұнКҫ)ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ¶ФУЪПВБРСх»Ҝ»№Фӯ·ҙУҰЈ¬Зл°ҙТӘЗуМоҝХЎЈ
Cu + 4HNO3(ЕЁ)=== Cu(NO3)2+ 2NO2Ўь + 2H2O
ўЩУГЛ«ПЯЗЕ·ЁұкіцөзЧУЧӘТЖөД·ҪПтәНКэДҝ_____________Ј»
ўЪСх»ҜјБ________Ј¬Сх»ҜІъОп__________Ј»
ўЫұ»»№ФӯөДHNO3УлІОјУ·ҙУҰөДHNO3ОпЦКөДБҝЦ®ұИКЗ_______Ј»ИфУР1molCuұ»Сх»ҜЈ¬Фтұ»»№ФӯөДПхЛбЦКБҝОӘ _____ gЈ»ИфІОјУ·ҙУҰөДПхЛбОӘ1.6molЈ¬Фт·ЕіцЖшМеөДМе»э(ФЪұкЧјЧҙҝцПВ)ОӘ___LЈ»
ўЬАлЧУ·ҪіМКҪЈә_______ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com