
【题目】美国计划2020年再次登陆月球,并在月球上建立永久性基地,为人类登陆新的行星做好前期准备。为了解决基地人员的供氧问题,科学家设想利用月球富氧岩石制取氧气。其提氧原理是用氢气还原富氧岩石获取水,再利用太阳能电池电解水得到氢气和氧气。
玄武岩(含钛铁矿)是月球的主要岩石之一,其质地坚硬,钛铁矿的主要成分为钛酸亚铁(![]() )。用上述提氧原理,理论上,从1 kg
)。用上述提氧原理,理论上,从1 kg ![]() 中可获取105.3g
中可获取105.3g ![]() 。
。
(1)写出![]() 与
与![]() 反应的化学方程式:______________________________________________。
反应的化学方程式:______________________________________________。
(2)研究表明,月球上平均直径为40微米的小圆珠形成的堆积物(富含![]() )是最适合提氧的矿物。这种堆积物作为提氧原料的优点是____________________________________________________________。
)是最适合提氧的矿物。这种堆积物作为提氧原料的优点是____________________________________________________________。
(3)研究人员查阅文献后,得知钛铁矿在高温下还能被炭粉还原: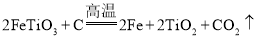 ,
,![]() 通过植物的光合作用可获得
通过植物的光合作用可获得![]() ,化光学方程式为
,化光学方程式为![]() (葡萄糖)
(葡萄糖)![]() 。他们设计了两套实验装置来测定钛铁矿中可提取氧的质量分数。
。他们设计了两套实验装置来测定钛铁矿中可提取氧的质量分数。
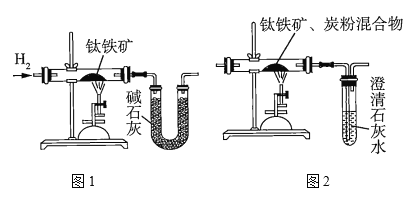
研究人员用图1装置从钛铁矿中提取氧,实验中得出的可提取氧的质量分数大于理论值,产生这种情况的原因可能是______________________;用图2装置进行实验的过程中,称得反应前钛铁矿的质量为![]() ,炭粉的质量为
,炭粉的质量为![]() ,钛铁矿完全反应后,测得生成
,钛铁矿完全反应后,测得生成![]() 的质量为
的质量为![]() ,则钛铁矿中可提取氧的质量分数为________________。
,则钛铁矿中可提取氧的质量分数为________________。
(4)在钛铁矿提氧过程中科学家们常选用![]() 而不用其他还原剂,其主要原因是______________________。
而不用其他还原剂,其主要原因是______________________。
【答案】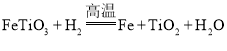 无需进行岩石破碎工作、可提取氧的质量分数大
无需进行岩石破碎工作、可提取氧的质量分数大 ![]() 未经干燥、U形管中碱石灰吸收了空气中的水分
未经干燥、U形管中碱石灰吸收了空气中的水分 ![]()
![]() 的氧化产物水无污染,电解水产生的
的氧化产物水无污染,电解水产生的![]() 能够循环利用
能够循环利用
【解析】
钛铁矿的主要成分为钛酸亚铁(![]() )与氢气发生氧化还原反应得到水,再电解水得到氧气,根据得失电子守恒,推知
)与氢气发生氧化还原反应得到水,再电解水得到氧气,根据得失电子守恒,推知![]() 中铁元素化合价降低;
中铁元素化合价降低;
(1)![]() 的物质的量为6.58 mol,105.3g
的物质的量为6.58 mol,105.3g ![]() 中含O的物质的量为6.58 mol,故结合提氧原理可知
中含O的物质的量为6.58 mol,故结合提氧原理可知![]() 生成
生成![]() 的物质的量也为6.58 mol,
的物质的量也为6.58 mol,![]() 与
与![]() 的物质的量之比为
的物质的量之比为![]() ,据此可确定反应的化学方程式。
,据此可确定反应的化学方程式。
(2)无需进行岩石破碎工作、可提取氧的质量分数大,故平均直径为40微米的小圆珠形成的堆积物(富含![]() )是最适合提氧的矿物。
)是最适合提氧的矿物。
(3)图1中测得的可提取氧的质量分数大于理论值,则可能是通入的![]() 未经干燥、U形管中的碱石灰吸收了空气中的水蒸气;因为图2中生成
未经干燥、U形管中的碱石灰吸收了空气中的水蒸气;因为图2中生成![]() 的质量为
的质量为![]() ,故
,故![]() 经光合作用可获得的
经光合作用可获得的![]() 的质量为
的质量为![]() ,所以钛铁矿中可提取氧的质量分数为
,所以钛铁矿中可提取氧的质量分数为![]() 。
。
(4)![]() 作还原剂的优点为:
作还原剂的优点为:![]() 的氧化产物水无污染,电解水产生的
的氧化产物水无污染,电解水产生的![]() 能够循环利用。
能够循环利用。


科目:高中化学 来源: 题型:
【题目】根据下列框图关系填空,已知反应![]() 、
、![]() 是我国工业生产中的重要反应,X常温下为无色无味透明液体;C焰色反应火焰呈黄色,J为红褐色沉淀;D、E常温下为气体,且E能使品红溶液褪色;A固体中仅含两种元素,其中金属元素的质量分数约为
是我国工业生产中的重要反应,X常温下为无色无味透明液体;C焰色反应火焰呈黄色,J为红褐色沉淀;D、E常温下为气体,且E能使品红溶液褪色;A固体中仅含两种元素,其中金属元素的质量分数约为![]() .
.
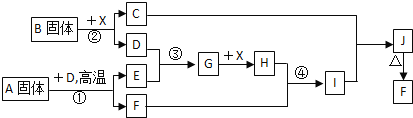
(1)![]() 的化学式为______;
的化学式为______;
(2)固体A中所包含的化学键与固体B类似,则A的电子式为______;
(3)反应![]() 的离子方程式:______;
的离子方程式:______;
(4)反应![]() 的离子方程式:______;
的离子方程式:______;
(5)已知每生成![]() ,放出
,放出![]() 热量,则反应
热量,则反应![]() 的热化学方程式为:______.
的热化学方程式为:______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题。
(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度。

①100℃时1 mol·L-1的NaOH溶液中,由水电离出的c(H+)=______mol·L-1,Kw(25℃)________Kw(100℃) (填“>”、“<”或“=”)。
②25℃时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是_____(填“促进”、“抑制”或“不影响”)。
(2)电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
化学式 | 电离平衡常数(25℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25℃时,有等浓度的a.NaCN溶液b.CH3COONa 溶液c.Na2CO3溶液,三种溶液的pH由大到小的顺序为_____________________;(填序号)
②25℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,则c(Na+)__________c(CH3COO-)(填“>”、“<”或“=”);
(3)25℃,两种酸的电离平衡常数如下表。
Ka1 | Ka2 | |
H2SO3 | 1.3×10-2 | 6.3×10-4 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
①HSO3-的电离平衡常数表达式K=_________。
②H2SO3溶液和NaHCO3溶液反应的主要离子方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷的分子结构可简写成键线式结构∧,有机物A的键线式结构为![]() ,有机物B与等物质的量的H2发生加成反应可得到有机物A。下列有关说法错误的是( )
,有机物B与等物质的量的H2发生加成反应可得到有机物A。下列有关说法错误的是( )
A.有机物A的一氯代物只有4种
B.用系统命名法命名有机物A,名称为2,2,3-三甲基戊烷
C.有机物A的分子式为C8H18
D.B的结构可能有3种,其中一种的名称为3,4,4-三甲基-2-戊烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.0100mol·L-1的NaOH溶液滴入浓度为0.0100mol·L-1,体积为20.00mL的CH3COOH溶液.在滴加过程中n(CH3COOH)和n(CH3COO-)随溶液pH的分布关系如图。下列说法不正确的是( )
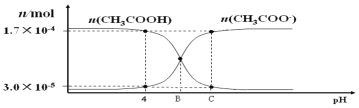
A.pH=4时,醋酸的电离常数Ka≈1.8×10-5
B.B点时,c(CH3COOˉ)=c(CH3COOH)
C.B点时,在溶液中滴入酚酞试剂,溶液显红色
D.C点时,c(CH3COOˉ)>c(Na+)>c(H+)>c(OHˉ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鲜花保鲜剂S-诱抗素制剂,可保证鲜花盛开。S-诱抗素的分子结构如下图,下列关于该物质的说法不正确的是( )
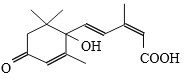
A.其分子式为C15H20O4
B.既能发生加成反应,又能发生取代反应
C.1mol该物质完全燃烧,需要消耗403.2L氧气
D.既能使紫色石蕊试剂显红色,又能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)1mol氢气在氯气中充分燃烧生成氯化氢气体时放出184.6 kJ的热量,试写出对应的热化学方程式___________________。标准状况下11.2L氢气在氯气中充分燃烧放出的热量是______kJ。
(2)A(g)+B(g)![]() C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
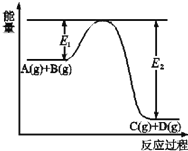
①反应物A(g)和B(g)具有的总能量_______(填大于、小于、等于)生成物C(g)和D(g)具有的总能量。
②该反应是_______反应(填吸热、放热),△H=_____(用E1和E2表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】500 mL KNO3和Cu(NO3)2的混合溶液中c(NO![]() )=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是
)=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是
A.原混合溶液中c(K+)为0.2 mol·L-1
B.上述电解过程中共转移0.2 mol电子
C.电解得到的Cu的物质的量为0.05 mol
D.电解后溶液中c(H+)为0.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+B![]() C(ΔH < 0)分两步进行:①A+B
C(ΔH < 0)分两步进行:①A+B![]() X(ΔH>0); ②X
X(ΔH>0); ②X![]() C(ΔH<0)。下列示意图中,能正确表示总反应过程中能量变化的是( )。
C(ΔH<0)。下列示意图中,能正确表示总反应过程中能量变化的是( )。
A.
B.
C.
D.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com