
【题目】丙烷的分子结构可简写成键线式结构∧,有机物A的键线式结构为![]() ,有机物B与等物质的量的H2发生加成反应可得到有机物A。下列有关说法错误的是( )
,有机物B与等物质的量的H2发生加成反应可得到有机物A。下列有关说法错误的是( )
A.有机物A的一氯代物只有4种
B.用系统命名法命名有机物A,名称为2,2,3-三甲基戊烷
C.有机物A的分子式为C8H18
D.B的结构可能有3种,其中一种的名称为3,4,4-三甲基-2-戊烯
【答案】A
【解析】
A. 根据信息可知,A的结构简式为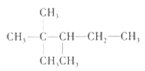 ,分子中有5种化学环境不同的氢原子,故其一氯代物有5种,A项错误;
,分子中有5种化学环境不同的氢原子,故其一氯代物有5种,A项错误;
B. 最长的主链含有5个C原子,从距离甲基近的一段编碳号, 的名称为:2,2,3-三甲基戊烷,B项正确;
的名称为:2,2,3-三甲基戊烷,B项正确;
C. 由A的结构简式可知,A的分子式为C8H18,C项正确;
D. A是有机物B与等物质的量的H2发生加成产物,则B中含有1个C=C双键,根据加成反应还原双键,A中相邻碳原子上都含有H原子的可以含有碳碳双键,故B的结构简式可能有如下三种: 、
、 、
、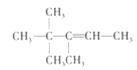 ,它们名称依次为:3,3-二甲基-2-乙基-1-丁烯、3,4,4-三甲基-1-戊烯、3,4,4-三甲基-2-戊烯,D项正确;
,它们名称依次为:3,3-二甲基-2-乙基-1-丁烯、3,4,4-三甲基-1-戊烯、3,4,4-三甲基-2-戊烯,D项正确;
答案选A。


科目:高中化学 来源: 题型:
【题目】利用废铅蓄电池的铅泥(PbO、Pb及PbSO4等)可制备精细无机化工产品“三盐”(3PbO·PbSO4·H2O),主要制备流程如下:

(1)步骤①PbSO4转化为难溶PbCO3的离子方程式为 ____________________________。
(2)滤液1和滤液3经脱色、蒸发、结晶可得到的副产品为____________(写化学式)。
(3)步骤③酸溶时,其中的铅与硝酸生成Pb(NO3)2及NO的离子方程式为____________________________;滤液2中溶质主要成分为________(写化学式)。
(4)步骤⑥合成三盐的化学方程式为 _______________________________________。
(5)步骤⑦洗涤操作时,检验沉淀是否洗涤干净的方法是 ___________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示。下列说法不正确的是( )
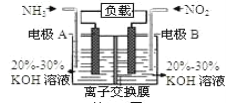
A.电流从右侧电极经过负载后流向左侧电极
B.A电极上发生氧化反应,B为正极
C.当有2.24LNO2(标准状况)被处理时,转移电子为0.4mol
D.电极A极反应式为2NH3-6e-=N2+6H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所示装置回答以下问题。已知:①KMnO4常温下与浓盐酸反应可制得Cl2。②H2SiO3不溶于水。
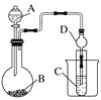
(1)利用如图装置可以验证元素非金属性的变化规律。图中A装置的名称是________________。干燥管D的作用是____________。
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性强于硫:烧瓶中发生反应的离子方程式为____________________________。装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_____________________。
(3)若要用此装置证明酸性:HNO3>H2CO3>H2SiO3,进而证明非金属性:N>C>Si,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀HNO3 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2。试剂A与C分别为________(填序号);试管中发生反应的离子方程式为__________________。有同学认为此实验不能说明N、C、Si的非金属性强弱,你认为原因是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:①![]()
②2![]()
③![]()
则![]() 的△H=______________。
的△H=______________。
(2)汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:![]()
![]() 2
2![]() ,已知该反应在2404℃,平衡常数
,已知该反应在2404℃,平衡常数![]() . 请回答:
. 请回答:
①某温度下,向2L的密闭容器中充入![]() 和
和![]() 各1mol,5分钟后
各1mol,5分钟后![]() 的物质的量为0.5
的物质的量为0.5![]() ,则
,则![]() 的反应速率为________________
的反应速率为________________
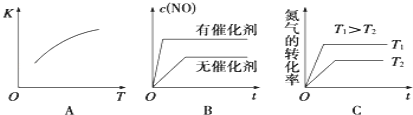
②将![]() 、
、![]() 混合气体充入恒温恒容密闭容器中,如图变化趋势正确的是_____(填字母序号).
混合气体充入恒温恒容密闭容器中,如图变化趋势正确的是_____(填字母序号).
③该温度下,某时刻测得容器内![]() 、
、![]() 、NO的浓度分别为
、NO的浓度分别为![]() 、
、![]() 和
和![]() ,此时反应__________________(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是______________________________.
,此时反应__________________(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是______________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00 mL 0.1000 mol·L—1 (NH4)2SO4溶液中逐滴加入0.2000 mol·L—1NaOH时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。下列说法正确的是

A.点a所示溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-)
B.点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-)
C.点c所示溶液中:c(SO42-)+ c(H+)= c(NH3·H2O )+ c(OH-)
D.点d所示溶液中:c(SO42-)>c(NH3·H2O )>c(OH-)>c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】D是一种催眠药,F是一种香料,它们的合成路线如下:
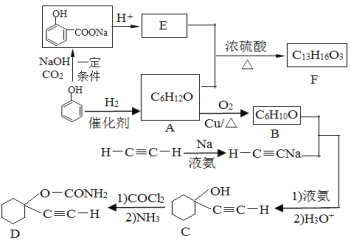
(1)A的化学名称是___________,C中含氧官能团的名称为__________。
(2)F的结构简式为____________________________。
(3)A生成B的化学方程式为_______________________________。
(4)写出由C合成D的第二个反应的化学方程式_____________________。
(5)同时满足下列条件的E的同分异构体有_____________种(不含立体异构)。
①遇FeCl3溶液发生显色反应 ②能发生银镜反应
(6)以乙炔和甲醛为起始原料,选用必要的无机试剂合成1,3-丁二烯,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用稀硝酸与铜反应制备NO气体,如果采用图Ⅰ装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不是十分理想,因为观察到的现象不能有力证明反应产物是NO。有人设计了图Ⅱ装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果。
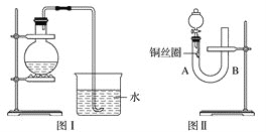
(1)用图Ⅰ装置做实验时,用排水法收集到的气体的颜色为_____色;实验过程中由于______,不易观察到____________生成,从而不能有力证明反应产物是NO。
(2)用图Ⅱ装置做实验时,将有关操作补充完全:
①将分液漏斗的活塞打开,从U形管的B侧管口注入稀硝酸,一直注到____________为止。
②关闭活塞,用酒精灯在U形管的A侧加热,当______时,立即撤去酒精灯。
(3)根据图Ⅱ装置的实验完成下列问题:
①反应在什么情况下可以自动停止?________________________。
可在何处观察到无色的NO气体?____________________________________________。
②如果将分液漏斗的活塞慢慢打开,可立即观察到哪些明显现象?_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数由小到大排列的四种短周期主族元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2离子化合物。
(1)写出Y2O2的电子式:__,其中含有的化学键是__。
(2)将ZO2通入品红溶液再加热的现象是__。
(3)写出X的最高价氧化物对应的水化物的稀溶液与铜反应的化学方程式__。
(4)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是_(填化学式)。
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com