
【题目】Ⅰ.化工工业中常用乙苯脱氢的方法制备苯乙烯。已知某温度下:
反应①:CO2(g) +H2 (g)→CO(g) + H2O(g),ΔH= +41.2 kJ/mol
反应②:![]() (g)→
(g)→![]() (g)+H2(g),ΔH= +117.6kJ/mol
(g)+H2(g),ΔH= +117.6kJ/mol
②的化学反应平衡常数分别为K1、K2。
(1)请写出二氧化碳氧化乙苯制备苯乙烯的热化学反应方程式__________________。该反应的化学平衡常数K=_________(用K1、K2表示)。
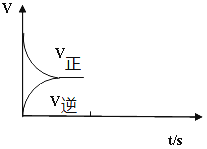
(2)温恒容条件下,反应①达到平衡后;t1时刻通入少量CO2;请在下图中画出t1之后的正逆反应曲线,并作出标注。__________________
Ⅱ.一定条件下,合成氨反应为:如图表示在此反应过程中的能量的变化,如图表示在2L的密闭中反应时N2的物质的量随时间的变化曲线.如图表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
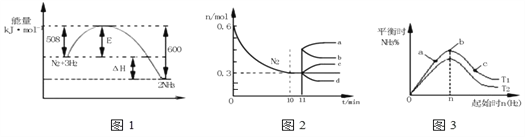
(3)由如图信息,计算10min内该反应的平均速率v(H2)=______,从11min起其它条件不变,压缩容器的体积,则n(N2)的变化曲线为____(填“a”或“b”或“c”或“d”)
(4)如图a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是____点,温度T1____T2(填“>”或“=”或“<”)
Ⅲ.H2O2是一种常用绿色氧化剂,工业上利用电解法制备H2O2的装置如图所示:
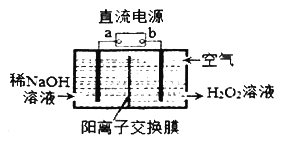
(5)a为______(正极、负极)
(6)通入空气的电极反应式为__________
【答案】 CO2(g)+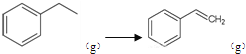 (g)+CO(g)+H2O(g)△H=+158.8 kJ/mol K=K1·K2
(g)+CO(g)+H2O(g)△H=+158.8 kJ/mol K=K1·K2 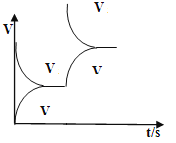 0.045mol/(L·min) d c < 正极 O2+2H2O+2e=H2O2+2OH-
0.045mol/(L·min) d c < 正极 O2+2H2O+2e=H2O2+2OH-
【解析】本题分析:本题主要考查化学平衡。
Ⅰ. (1)①+②可得二氧化碳氧化乙苯制备苯乙烯的热化学方程式:
CO2(g)+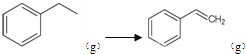 (g)+CO(g)+H2O(g)△H=+158.8 kJ/mol 。
(g)+CO(g)+H2O(g)△H=+158.8 kJ/mol 。
该反应的化学平衡常数K=K1K2。
(2)t1时刻通入少量CO2, t1之时刻正反应速率增大,逆反应速率不变,t1后正反应速率减小,逆反应速率增大。t1之后的正逆反应曲线为:
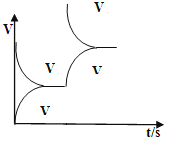
Ⅱ. (3)v(H2)=3v(N2)=(0.3/2/10×3)mol/(L·min)=0.045mol/(L·min)。从11min起其它条件不变,压缩容器的体积,加压平衡右移,n(N2)减小,则n(N2)的变化曲线为d。
(4)因为增大氢气浓度可以提高氮气的转化率,所以反应物N2的转化率最高的是c点。因为升温平衡左移,氮气的转化率降低,所以温度T1<T2。
Ⅲ.(5)连接a电极的电极发生氧化反应,所以a为正极。
(6)通入空气的电极反应式为O2+2H2O+2e=H2O2+2OH-。


科目:高中化学 来源: 题型:
【题目】主族元素在周期表中的位置取决于该元素原子的
A. 相对原子质量和核外电子数 B. 相对原子质量和最外层电子数
C. 电了层数和最外层电子数 D. 电子层数和次外层电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在葡萄糖溶液中有一种环状结构的葡萄糖分子(分子式C6H12O6),且有下列平衡关系:
(1)这种环状结构的分子是通过链式葡萄糖分子中的__________基和___________基通过_______________________反应而形成的。
(2)用(1)反应方式写出由两种简单的有机物合成某一链状醇醚(如右)的反应方程式:________
![]()
(3)已知溴水(Br2+H2O)可以将多羟基醛基氧化成羧基。写出溴水与葡萄糖反应的化学方程式_________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油加工的各种处理过程中,属于裂化过程的是( )
A. 分离出汽油和煤油B. 原油脱盐、脱水
C. 十六烷变为辛烷和辛烯D. 将直链烃变为芳香烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和Ca,并含有3.5%(质量分数)CaO。
(1)Ca元素在周期表中位置是_________,其原子结构示意图_________。
(2)Ca与最活跃的非金属元素A形成化合物D,D的电子式为_________。
(3)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则金属M为______;检测Mn+的方法是_______________________________________(用离子方程式表达)。
(4)取1.6g钙线试样,与水充分反映,生成224ml.H2(标准状况),在想溶液中通入适量的CO2,最多能得到CaCO3_____________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某绿色农药结构简式为 ,回答下列问题。
,回答下列问题。
(1)N元素的基态原子核外有_____种空间运动状态的电子,该农药组成元素中,第一电离能较大的前三种元素是(按由大到小顺序排列)________(用元素符号回答,下同),基态硒原子的价层电子排布式为___________。
(2)该物质中,中心原子杂化轨道类型为sp2的原子有_____,分子中编号为① 的碳原子和与其成键的另外几个原子构成的空间结构为_________。
(3)碳、氢、氧元素可形成一系列的化合物,如CH4、C2H6、CH3OH等。三种物质的沸点高低顺序为CH42H63OH,其原因是________,三种物质中属于极性分子的物质是______, 与CH4互为等电子体的一种微粒是_________。
(4)硒化锌的晶胞结构如图所示,则硒的配位数为________,若晶胞边长为d pm ,设阿伏加德罗常数的值为NA,则硒化锌的密度为______(不必化简)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”是指从技术、经济上设计可行的化学反应,尽可能减少对环境的副作用, 下列化学反应,不符合绿色化学概念的是( )
A. 消除硫酸厂尾气排放:SO2+2NH3+H2O![]() (NH4)2SO3
(NH4)2SO3
B. 消除硝酸厂排放的氮氧化物:NO2+NO+2NaOH![]() 2NaNO2+H2O
2NaNO2+H2O
C. 制CuSO4:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
D. 制CuSO4:2Cu+O2![]() 2CuO; CuO+H2SO4(稀)
2CuO; CuO+H2SO4(稀)![]() CuSO4+H2O
CuSO4+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某共价化合物含碳、氢、氮三种元素,分子内有四个氮原子,且四个氮原子排列成内空的四而体(如白磷结构),每两个氮原子间都有一个碳原子。己知分子内无碳碳单键,也没有碳碳双键,则该化合物的分子式为( )
A. CH8N4 B. C6H12N4 C. C6H10N4 D. C4H8N4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】成语是中华名族灿烂文化中的瑰宝,许多成语中蕴含着丰富的化学原理,下列成语中涉及氧化还原反应的是
A. 木已成舟 B. 百炼成钢 C. 铁杵成针 D. 滴水成冰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com