
【题目】金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和Ca,并含有3.5%(质量分数)CaO。
(1)Ca元素在周期表中位置是_________,其原子结构示意图_________。
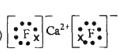
(2)Ca与最活跃的非金属元素A形成化合物D,D的电子式为_________。
(3)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则金属M为______;检测Mn+的方法是_______________________________________(用离子方程式表达)。
(4)取1.6g钙线试样,与水充分反映,生成224ml.H2(标准状况),在想溶液中通入适量的CO2,最多能得到CaCO3_____________g。
【答案】 第四周期第ⅡA族 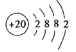
 Fe Fe3++3SCN-=Fe(SCN)3 1.1g
Fe Fe3++3SCN-=Fe(SCN)3 1.1g
【解析】(1)Ca是20号元素,钙原子核外电子数为20,有3个电子层,各层电子数为2、8、8、1,处于周期表中第四周期第ⅡA族,原子结构示意图为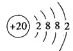 ,故答案为:第四周期第ⅡA族;
,故答案为:第四周期第ⅡA族; ;(2)最活跃的非金属元素A为F元素,钙与氟形成氟化钙,为离子化合物,电子式为
;(2)最活跃的非金属元素A为F元素,钙与氟形成氟化钙,为离子化合物,电子式为![]() ;(3)钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,M为Fe元素,Fe3+与SCN-结合生成红色物质检验Fe3+,离子方程式为Fe3++3SCN-=Fe(SCN)3;(4)224mlH2的物质的量为
;(3)钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,M为Fe元素,Fe3+与SCN-结合生成红色物质检验Fe3+,离子方程式为Fe3++3SCN-=Fe(SCN)3;(4)224mlH2的物质的量为![]() =0.01mol,钙与水反应生成氢氧化钙与氢气,根据电子转移守恒可知,Ca的物质的量为
=0.01mol,钙与水反应生成氢氧化钙与氢气,根据电子转移守恒可知,Ca的物质的量为![]() =0.01mol,样品中CaO质量分数为3.5%,故氧化钙的质量为1.6g×3.5%=0.056g,故氧化钙的物质的量为
=0.01mol,样品中CaO质量分数为3.5%,故氧化钙的质量为1.6g×3.5%=0.056g,故氧化钙的物质的量为![]() =0.001mol,氧化钙与水反应生成氢氧化钙,氢氧化钙与二氧化碳反应生成碳酸钙,根据钙元素守恒可知生成的n(CaCO3)=n(Ca)+n(CaO)=0.01mol+0.001mol=0.011mol,碳酸钙的质量为0.011mol×100g/mol=1.1g
=0.001mol,氧化钙与水反应生成氢氧化钙,氢氧化钙与二氧化碳反应生成碳酸钙,根据钙元素守恒可知生成的n(CaCO3)=n(Ca)+n(CaO)=0.01mol+0.001mol=0.011mol,碳酸钙的质量为0.011mol×100g/mol=1.1g


科目:高中化学 来源: 题型:
【题目】常温下,将某一元酸HX和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
试验编号 | HX的物质的量浓度(mol/L) | NaOH的物质的量浓度(mol/L) | 混合溶液的PH |
甲 | 0.2 | 0.2 | PH=a |
乙 | c1 | 0.2 | PH=7 |
丙 | 0.2 | 0.2 | PH>7 |
丁 | c2 | c3 | PH=10 |
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,若a________7(填“>”“<”或“=”),则HX为强酸;若a________7(填“>”“<”或“=”),则HX为弱酸.
(2)在乙组混合溶液中离子浓度c(X-)与c(Na+)的大小关系是________.
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)丙溶液中离子浓度由大到小的顺序是_____________________________.
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=________mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烷、乙烯、乙炔它们及其衍生物一氯乙烷、氯乙烯、乙醇、乙醛、乙酸、乙酸乙酯都有很重要的用途。
(1)乙炔在空气中燃烧的现象____________________________________________________
由乙烷制取一氯乙烷的反应条件___________________,由乙烯制取乙醇的反应类型_________
(2)一氯乙烷分子中的官能团为__________________。聚氯乙烯的结构简式为________________。
(3)写出由乙醛生成乙酸的化学反应方程式。__________________________________________
(4)写出乙酸的一种同分异构体的结构简式____________________________;检验该同分异构体是否含有醛基操作_________________________________________________________
______________________________________________________________
(5)乙二醇(HOCH2CH2OH)也是一种很重要的化工原料,请完成由一氯乙烷合成乙二醇的路线图(合成路线常用的表示方式为:![]() )
)
____________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铁矿是生产硫酸的原料,其主要成分为FeS2。850950℃时,在空气中煅烧,发生反应
4FeS2 + 11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
试回答下列问题:
(1)含硫35%的黄铁矿样品(杂质不含硫),其FeS2的含量为_____________
(2)可用来表示该反应的化学反应速率的物质为_________________(填化学式)。
(3)某时刻测得生成SO2的速率为0.64 mol·L-1·s-1,则氧气减少的速率为_____________
(4)为了提高SO2的生成速率,下列措施可行的是______________(填选项字母)。
A.增加硫铁矿石的投入量 B.增加炉的高度
C.将硫铁矿石粉碎 D.升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.化工工业中常用乙苯脱氢的方法制备苯乙烯。已知某温度下:
反应①:CO2(g) +H2 (g)→CO(g) + H2O(g),ΔH= +41.2 kJ/mol
反应②:![]() (g)→
(g)→![]() (g)+H2(g),ΔH= +117.6kJ/mol
(g)+H2(g),ΔH= +117.6kJ/mol
②的化学反应平衡常数分别为K1、K2。
(1)请写出二氧化碳氧化乙苯制备苯乙烯的热化学反应方程式__________________。该反应的化学平衡常数K=_________(用K1、K2表示)。
(2)温恒容条件下,反应①达到平衡后;t1时刻通入少量CO2;请在下图中画出t1之后的正逆反应曲线,并作出标注。__________________
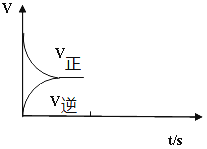
Ⅱ.一定条件下,合成氨反应为:如图表示在此反应过程中的能量的变化,如图表示在2L的密闭中反应时N2的物质的量随时间的变化曲线.如图表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
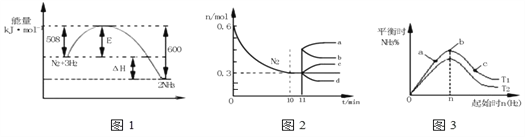
(3)由如图信息,计算10min内该反应的平均速率v(H2)=______,从11min起其它条件不变,压缩容器的体积,则n(N2)的变化曲线为____(填“a”或“b”或“c”或“d”)
(4)如图a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是____点,温度T1____T2(填“>”或“=”或“<”)
Ⅲ.H2O2是一种常用绿色氧化剂,工业上利用电解法制备H2O2的装置如图所示:
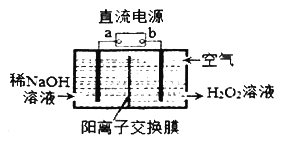
(5)a为______(正极、负极)
(6)通入空气的电极反应式为__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验过程中,始终无明显现象的是
A. SO2通入BaCl2溶液中 B. CO2通入澄清石灰水中
C. NH3通入MgCl2溶液中 D. Cl2通入KI淀粉溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓硫酸与蔗糖反应的实验,对现象的解释不合理的是
选项 | 现象 | 解释 |
A | 蔗糖变黑 | 浓硫酸具有脱水性 |
B | 有刺激性气味 | 浓硫酸具有强酸性 |
C | 固体体积膨胀 | 生成大量气体 |
D | 烧杯壁发烫 | 反应放热 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下饱和CO2溶液的pH约为5.6。向某未知浓度的Na2CO3溶液中滴入已知浓度的盐酸时,用 pH传感器测得混合溶液的pH变化曲线如图所示,下列说法正确的是

A. 该Na2CO3溶液的浓度为0.001mol/L
B. 在pH=7时,c(Na+)> c(Cl﹣)
C. 在pH=6时,c(Na+)>c(CO32﹣)>c(HCO3﹣)
D. c→d发生的主要离子反应为:CO32﹣+H+=HCO3﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com