
【题目】0.2L1mol·L-1的KCl溶液和0.5L1mol·L-1的FeCl3溶液中,Cl- 的物质的量浓度之比为 ( )
A.1∶3B.3∶1C.1∶1D.2∶15
 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】有机物G是一种“β﹣兴奋剂”,其合成路线如下: 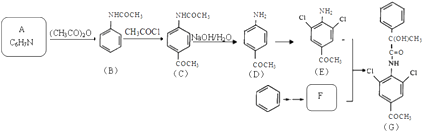 已知:
已知: 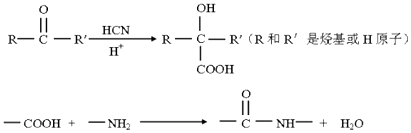
(1)写出化合物E同时符合下列条件的所有同分异构体的结构简式
①红外光谱显示含有三种官能团,其中无氧官能团与E相同,不含甲基
②1H﹣NMR谱显示分子中含有苯环,且苯环上只有一种不同化学环境的氢原子.
③苯环上只有4个取代基,能发生银镜反应
(2)下列说法不正确的是
A.化合物B生成C的反应为取代反应
B.1mol化合物D最多与4molH2发生加成反应
C.化合物D生成E的条件为浓氯水/铁屑
D.化合物G的分子式为C17H14Cl2NO3
(3)写出E+F→G的化学方程式
(4)根据题中信息,设计以苯和CH3COCl为原料制备F的合成路线(用流程图表示,其他无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( ) 
A.反应③最多能产生0.1 mol O2
B.反应①的离子方程式为Na+2H2O═Na++2OH﹣+H2↑
C.Na2O2中阴阳离子数目之比为1:1
D.①②③充分反应后所得溶液中溶质的质量分数:②=③>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天宫一号搭载的长征二号火箭使用的主要燃料是偏二甲肼(用R表示,其中碳元素显﹣2价、氮元素显﹣2价),N2O4作氧化剂,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:R + 2N2O4 = 3N2↑+ 4H2O↑+ 2CO2↑,下列叙述错误的是( )
A. 燃烧反应放出的巨大能量,把火箭送入太空
B. N2既是氧化产物也是还原产物,CO2是氧化产物
C. 每生成1mol N2,该反应转移电子8mol
D. 此反应中R的分子式为C2H8N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、(1)3.3gH3PO2物质的量为___________,其中含有_______ mol H,含有________个O,含磷元素_________ g,若它可与2g NaOH完全反应生成正盐,则H3PO2为_________元酸。
(2)在9.5g某二价金属的氯化物中含有0.2mol Cl-,此氯化物的摩尔质量为________________。
II、在原子序数1—18号元素中(稀有气体元素除外):
(1)原子半径最小的是____________________,原子半径最大的是____________________。
(2)最高价氧化物对应的水化物碱性最强的是____________________(填化学式)。
(3)最高价氧化物对应的水化物酸性最强的是____________________(填化学式)。
(4)与水反应最剧烈的金属是____________________。
(5)比较Si、N最简单氢化物的稳定性:____________________(用化学式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有丰富的Na+、Mg2+、Cl﹣、Br﹣等化学资源.将海水淡化与浓缩海水结合是综合利用海水资源的途径之一.以浓缩海水为原料,通过一系列工艺流程可以提取Mg、Br2等产品.
(1)如图是采用膜分离技术的海水淡化示意图.淡化膜可以让水分子通过,而海水中其他分子和离子均不能通过.加压后,左侧淡水中增加的是(填字母). 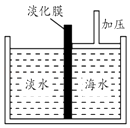
a.溶质质量 b.溶剂质量 c.溶质的质量分数
(2)从海水中提取镁的主要步骤如下: 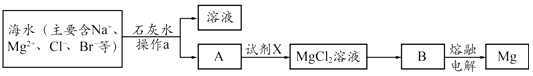
①操作a的名称是 .
②写出B冶炼金属镁的化学方程式 .
(3)空气吹出法是用于工业规模海水提溴的常用方法,其中一种工艺是以预先经过酸化的浓缩海水为原料,通过以下步骤提取溴: 步骤一:用氯气置换溴离子使之成为单质溴;
步骤二:通入空气和水蒸气,将溴吹入吸收塔,使溴蒸气和吸收剂SO2发生作用转化成氢溴酸;
步骤三:用氯气将氢溴酸氧化得到产品溴.
①步骤一和步骤二的目的是 .
②步骤二中发生反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酚酞是中学阶段常用的酸碱指示剂,己知其结构简式如图所示;下列关于酚酞的说法正确的是( ) 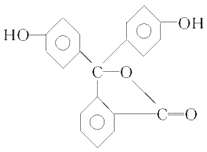
A.酚酞分子中含有两种官能团
B.酚酞的分子式为C20H12O4
C.酚酞属于芳香烃
D.酚酞结构中含有羟基(﹣OH),故酚酞属于醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com