
����Ŀ����ͼ��ԲȦ�ཻ�IJ��ֱ�ʾԲȦ�ڵ�����������ķ�Ӧ����֪�Ƽ�������������ʵ�����Ϊ0.1mol��ˮ������Ϊ100g������˵����ȷ���ǣ� �� 
A.��Ӧ������ܲ���0.1 mol O2
B.��Ӧ�ٵ����ӷ���ʽΪNa+2H2O�TNa++2OH��+H2��
C.Na2O2������������Ŀ֮��Ϊ1��1
D.�٢ڢ۳�ַ�Ӧ��������Һ�����ʵ�������������=�ۣ���
���𰸡�D
���������⣺A����Ӧ�ۣ�
2Na2O2+2H2O=4NaOH+ | O2�� |
2mol | 1mol |
0.1mol | 0.05mol |
���ݷ���ʽ֪��������0.05molO2����A����
B��Na+2H2O�TNa++2OH��+H2���е�ɲ��غ㣬��Ӧ����ȷ�����ӷ���ʽΪ��2Na+2H2O=2Na++2OH��+H2������B����
C��Na2O2���������ǹ��������ӣ����������������ӣ���������������Ŀ֮��Ϊ1��2����C����
D���ơ������ơ��������ƺ�ˮ��Ӧ�ķ���ʽ�ֱ����£�
Na+H2O=NaOH+ ![]() H2������Һ���ӵ�����=m��Na����m��H2��=2.3g��0.1g=2.2g��
H2������Һ���ӵ�����=m��Na����m��H2��=2.3g��0.1g=2.2g��
Na2O+H2O=2NaOH����Һ���ӵ�����=m��Na2O��=0.1mol��62g/mol=6.2g��
Na2O2+H2O=2NaOH+ ![]() O2������Һ���ӵ�����=m��Na2O2����m��O2��=m��Na2O��=6.2g
O2������Һ���ӵ�����=m��Na2O2����m��O2��=m��Na2O��=6.2g
������Һ���ӵ�������С˳��Ϊ���ƣ�������=�������ƣ�
������ԭ���غ�֪��0.1mol���ơ������ơ��������ơ�����ˮ�����������Ƶ����ʵ����ֱ�Ϊ��0.1mol��0.2mol��0.2mol��ͨ�����Ϸ�����֪��0.1mol���ơ������ơ��������ơ��ֱ�����ˮ������Һ�����������ֱ�Ϊ�� ![]() ��
�� ![]() ��
�� ![]() �����Ԣ١��ڡ��۳�ַ�Ӧ��������Һ�����������Ӵ�С���٣���=�ۣ���D��ȷ��
�����Ԣ١��ڡ��۳�ַ�Ӧ��������Һ�����������Ӵ�С���٣���=�ۣ���D��ȷ��
��ѡD��
A�����ݹ������ƺ�ˮ��Ӧ�ķ���ʽ�����������������ʵ�����
B�����ӷ���ʽҪ��ѭ��ԭ���غ�͵���غ�ȡ����ɣ�
C����������ˮ��Ӧ��Ԫ�ػ��ϼ۵ı仯��
D�����ݹ�������ʵ���������Һ�����ʵ���������Һ����������������������ʽ�ж�����������Դ�С��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Q��R��X��Y��ZΪ���ڱ�ǰ������Ԫ�أ�ԭ���������ε�������֪��
��QΪԪ�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�
��R�Ļ�̬ԭ���е���ռ������������ͬ��ԭ�ӹ������ÿ�ֹ���еĵ���������ͬ��
��Y�Ļ�̬ԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������3����
��Q��R��Y����Ԫ����ɵ�һ�ֻ�����M����װ�����г����е�һ���к����壬Q��R����Ԫ����ɵ�ԭ�Ӹ�����Ϊ1��1�Ļ�����N����ѧ��ѧ�г������л��ܼ���
��Z�С����������֮�ƣ�Z4+���Ӻ��ԭ�ӵĺ�������Ų���ͬ��
��ش��������⣨����ʱ��Q��R��X��Y��Z������Ӧ��Ԫ�ط��ű�ʾ��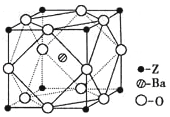
��1��������M�Ŀռ乹��Ϊ ��������ԭ�Ӳ�ȡ�� �ӻ���������N�ڹ�̬ʱ�ľ�������Ϊ
��2��R��X��Y����Ԫ�صĵ�һ��������С�����˳��Ϊ
��3��������һ�ֻ����Ԫ����ɵ���RY2��Ϊ�ȵ�����ķ���Ϊ ��д����ʽ��
��4����R��X��Y����Ԫ����ɵ�RXY�����������������¿���NaClO��Һ��Ӧ������X2��RY2�����ʣ��÷�Ӧ�����ӷ���ʽΪ
��5��Zԭ�ӻ�̬ʱ����Χ�����Ų�ʽΪ�� ��Z��һ�ֺ����ᱵ�εľ����ṹ��ͼ��ʾ����������ÿ��Zԭ�ӵȾ������������ԭ����Ϊ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ӦN2��3H2===2NH3�������仯��ͼ��ʾ���÷�Ӧ���Ȼ�ѧ����ʽ��(����)
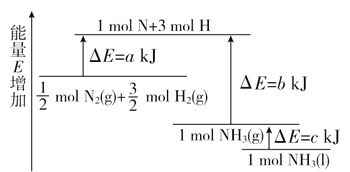
A. ![]() N2(g)��
N2(g)��![]() H2(g)��NH3(l)����H��(a��b��c) kJ/mol
H2(g)��NH3(l)����H��(a��b��c) kJ/mol
B. N2(g)��3H2(g)��2NH3(g)����H��2(b��a) kJ/mol
C. ![]() N2(g)��
N2(g)��![]() H2(g)��NH3(l)����H��(b��c��a) kJ/mol
H2(g)��NH3(l)����H��(b��c��a) kJ/mol
D. ![]() N2(g)��
N2(g)��![]() H2(g)��NH3(g)����H��(a��b) kJ/mol
H2(g)��NH3(g)����H��(a��b) kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ���������У�A��B��C��D��Ϊʯī�缫�����������й���0.02 mol����ͨ����������������ȷ���ǣ� ��
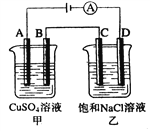
A. ���ձ���A������������ͭ0.64g
B. ���ձ��е����̪��Һ��D�������ȱ��
C. ���ձ���B���ϵ缫��Ӧʽ��4OH����4e����2H2O+O2��
D. �ձ���C���ϵ缫��ӦʽΪ��4H++4e����2H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ��Һ�м����Ȼ�����Һ�а�ɫ�������ټ�ϡ�����������ʧ���������ж���ȷ���ǣ� ��
A.һ����SO42-B.һ����CO32-
C.һ����Ag+D.һ����SO42-��Ag+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��0.2L1mol��L-1��KCl��Һ��0.5L1mol��L-1��FeCl3��Һ�У�Cl- �����ʵ���Ũ��֮��Ϊ �� ��
A.1��3B.3��1C.1��1D.2��15
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��д����صķ���ʽ��
��1��д����ⱥ��ʳ��ˮ�Ļ�ѧ����ʽ
��2���Ȼ����Һ��������Ե����ӷ���ʽ
��3���Ҵ���������KOHΪ����ʵ���Һ�γɵ�ȼ�ϵ�صĸ����缫��Ӧʽ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijЩ���ϱ�����NO��NO2������Na2O2��Ӧ��ijС��ѧ��������ɣ����Ǵ������Ϸ���Na2O2��NO2���������ԣ����ݻ��ϼ�����ԭ��������¼��裺
������. Na2O2����NO2�� ������. NO2����Na2O2��
��ش��������⣺
��1����ͬѧ�����ͼ1��ʾʵ��װ�ã�
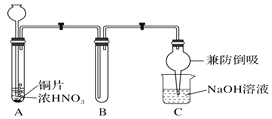
ͼ1
���Թ�A�з�Ӧ�����ӷ���ʽ��___________________________________________________��
�ڴ��Թ�B���ռ������壬���Թ�B�м�������Na2O2��ĩ���������ӣ��������Թ��ڷ�ĩ���۲쵽����ɫ����Ѹ����ʧ���ٽ������ǵ�ľ��Ѹ������Թ��ڣ�ľ����ȼ����ͬѧ�ݴ���Ϊ��������ȷ����ͬѧ��Ϊ��װ�ò��ܴﵽʵ��Ŀ�ģ�Ϊ�ﵽʵ��Ŀ�ģ�Ӧ��A��B֮������һ��װ�ã���װ�õ�������__________________________________________________________________��
����ͬѧ�øĽ����װ�ã��ظ��˼�ͬѧ��ʵ��������۲쵽����ɫ����Ѹ����ʧ�������ǵ�ľ��δ��ȼ���ó����ۣ���������ȷ��NO2��Na2O2��Ӧ�Ļ�ѧ����ʽ��_____________________��
��2����ͬѧ��ΪNO����O2������Ӧ��Ӧ���ױ�Na2O2��������������֪��
��) 2NO��Na2O2===2NaNO2��
��) 6NaNO2��3H2SO4===3Na2SO4��2HNO3��4NO����2H2O��
��)���������£�NO��NO![]() ������MnO
������MnO![]() ��Ӧ����NO
��Ӧ����NO![]() ��Mn2����
��Mn2����
��ͬѧ��ͼ2��ʾװ��(���ּг�װ����)̽��NO��Na2O2�ķ�Ӧ��
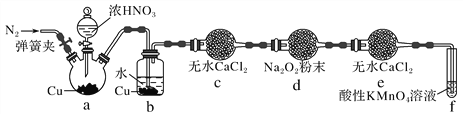
ͼ2
��bװ���й۲쵽����Ҫ������__________________________________________________��fװ�õ�������_________________________________________________________________��
���ڷ�Ӧǰ���ȴ��ɼУ�ͨ��һ��ʱ��N2����Ŀ����____________________________
�۳�ַ�Ӧ����dװ���з�����Ӧ��ʵ����___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ������ ��
A. ֱ������1 nm ~ 100 nm ֮�������Ϊ����
B. �������Ӻ�С����������Ĥ
C. ���ö����ЧӦ����������Һ�ͽ���
D. ��FeCl3��Һ�м���NaOH��Һ���Ƶ�Fe��OH��3����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com