
【题目】MnO2是一种重要的无机功能材料,工业上从锰结核中制取纯净的MnO2工艺流程如下图所示:

部分难溶的电解质溶度积常数(Ksp)如下表:
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10﹣17 | 10﹣17 | 10﹣39 |
已知:一定条件下,MnO4![]() 可与Mn2+反应生成MnO2
可与Mn2+反应生成MnO2
(1)步骤Ⅱ中消耗0. 5molMn2+时,用去1molL-1的NaClO3溶液200ml,该反应离子方程式为
(2)已知溶液B的溶质之一可循环用于上述生产,此物质的名称是_____________。
(3)MnO2是碱性锌锰电池的正极材料.放电过程产生MnOOH,该电池正极的电极反应式是 。如果维持电流强度为5A,电池工作五分钟,理论消耗锌 g.(已知F=96500C/mol)
(4)向废旧锌锰电池内的混合物(主要成分MnOOH、Zn(OH)2)中加入一定量的稀硫酸和稀草酸(H2C2O4),并不断搅拌至无CO2产生为止,写出MnOOH参与反应的离子方程式 。
。向所得溶液中滴加高锰酸钾溶液产生黑色沉淀,设计实验证明黑色沉淀成分为MnO2 。
(5)用废电池的锌皮制作ZnSO47H2O的过程中,需除去锌皮中的少量杂质铁,其方法是:加入稀H2SO4和H2O2,铁溶解变为Fe3+,加碱调节pH为 时,铁刚好沉淀完全(离子浓度小于1×10﹣5molL﹣1时,即可认为该离子沉淀完全)。继续加碱调节pH为 时,锌开始沉淀(假定Zn2+浓度为0.1molL﹣1)。
【答案】(1)5Mn2++ 2ClO3- +4H2O =5 MnO2+Cl2↑ +8H+ (2分)
(2)氯酸钠 (1分);
(3)MnO2+ H2O +e﹣=MnOOH +OH-(2分) 0.5g(2分);
(4)2MnOOH+ H2C2O4 +4H+ = 2Mn2++ 2CO2↑+4H2O(2分)
取少量黑色固体放入试管中,加入少量浓盐酸并加热, 产生黄绿色气体,说明黑色固体为MnO2(2分);
(5)2.7(1分) 6(1分)
【解析】
试题分析:工业上从锰结核中制取纯净的MnO2工艺流程中,先选矿富集,锰结核为锰的氧化物与其它金属氧化物的混合物,加入稀硫酸发生反应生成Mn2+,在溶液中加入NaClO3反应生成MnO2和A等,A和热氢氧化钠溶液反应生成溶液B;
(1)0.1mol/L的NaClO3溶液200ml的物质的量是0.02mol,当生成0.05molMnO2时,转移电子的物质的量是0.05mol×(4-2)=0.1mol,根据电子得失守恒可知0.02mol氯酸钠得到0.1mol电子,因此氯元素的化合价变化5价,即从+5价降低到0价,因此还原产物是氯气,所以该反应离子方程式为5Mn2++ 2ClO3- +4H2O =5 MnO2+Cl2↑ +8H+;
(2)氯气与热的氢氧化钠溶液反应生成氯酸钠、氯化钠和水,因此可以循环的物质B是氯酸钠;
(3)原电池中负极失去电子,正极得到电子,因此碱性锌锰电池放电时,正极是二氧化锰得到电子,则电极反应式为MnO2+ H2O +e﹣=MnOOH +OH-;5分钟转移电子的电量Q=It=5A×300s=1500C,转移电子的物质的量为Q/F=1500C/96500C/mol≈0.0155mol,则消耗的Zn的质量为0.0155mol×0.5×65g/mol=0.5g;
(4)因为反应物有稀草酸,产物有二氧化碳,则说明碳元素化合价升高发生氧化还原反应,所以锰化合价降低生成二价的MnSO4,方程式为2MnOOH+H2C2O4+2H2SO4=2CO2↑+2MnSO4+4H2O;根据实验室制氯气的反应原理,取少量黑色固体放入试管中,加入少量浓盐酸并加热,产生黄绿色气体,说明黑色固体为MnO2;
(5)铁加入稀H2SO4和H2O2,可被氧化生成Fe3+,铁刚好沉淀完全时离子浓度小于1×10-5molL-1,因Ksp=10-39,则c(OH-)=![]() ≈0.5×10-11mol/L,此时pH=2.7;如锌开始沉淀,则c(OH-)=
≈0.5×10-11mol/L,此时pH=2.7;如锌开始沉淀,则c(OH-)=![]() =10-8mol/L,此时pH=6。
=10-8mol/L,此时pH=6。


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
【题目】铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O![]() Fe(OH)2+2Ni(OH)2.下列有关该电池的说法不正确的是( )
Fe(OH)2+2Ni(OH)2.下列有关该电池的说法不正确的是( )
A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe
B.电池放电时,负极反应为Fe-2e-![]() Fe2+
Fe2+
C.电池充电过程中,阴极附近溶液的pH升高
D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-![]() Ni2O3+3H2O
Ni2O3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物能使澳的CC4溶液褪色,也能在一定条件下发生水解生成两种有机物,还能发生加聚反应生成高分子化合物,则此有机物中通常含有的基团的组合是
A. 卤素原子、碳碳双键 B. 羟基、羧基 C. 醛基、酯基 D. 碳碳双键、酯基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:在体积为1 L的密闭容器中,充入1 mol CO2和3 molH2,一定条件下发生反应:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1
T温度下,测得CO2和CH3OH(g)的浓度随时间变化如下图。请回答下列问题:

① 达平衡时,氢气的平衡浓度为C (H2)= 。
② 能够说明该反应已达到平衡的是 (填字母序号,下同)。
A.恒温、恒容时,容器内的压强不再变化
B.恒温、恒容时,容器内混合气体的密度不再变化
C.一定条件下,CO、H2和CH3OH的浓度保持不变
D.一定条件下,单位时间内消耗3 mol H2的同时生成1 mol CH3OH
③ 下列措施中能使平衡混合物中![]() 增大的是______________。
增大的是______________。
A.加入催化剂 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.降低温度
④ 求此温度(T)下该反应的平衡常数K = 。若开始时向该1 L密闭容器中充入1 mol CO2,2molH2,1.5mol CH3OH和1 mol H2O(g),则反应向 (填“正”或“逆”)反应方向进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,属于吸热反应的是( )
①液态水汽化; ②胆矾加热变为白色粉末;③浓硫酸稀释;
④氯酸钾分解制氧气;⑤碳与氧气反应生成一氧化碳。
A.①③⑤ B.②④ C.①② D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用粗盐(含Ca2+、Mg2+、SO42-等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如下图所示。下列有关说法正确的是


A. 对粗盐溶液除杂可依次加入NaOH、Na2CO3、BaCl2,再加入盐酸调节溶液pH
B. 饱和食盐水中先通入的气体为CO2
C. 流程图中的系列操作中一定需要玻璃棒
D. 如图所示装置可以比较Na2CO3和NaHCO3晶体热稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式: .若1g水蒸气转化成液态水放热2.5kJ,则氢气的燃烧热为△H= kJ/mol.
(2)近年来已经研制出甲烷(CH4)燃料电池,该电池的电解质溶液为H2SO4溶液,写出该电池负极的电极反应式: .该电池总反应式: .
(3)用惰性电极电解AgNO3溶液,写出该电解反应的化学方程式 ;若在阳极收集到 0.32g O2,中和电解生成的酸需0.4molL﹣1NaOH溶液 mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属及其化合物的说法正确的是
A. 地壳中含量最多的元素是铝元素
B. 在自然界中铝以化合态存在
C. NaCl的焰色反应呈紫色
D. 白色絮状沉淀Fe(OH)2置在空气中颜色不会发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。
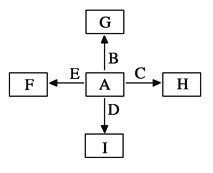
已知:①G为红棕色固体,能发生反应C+G![]() B+H,该反应会放出
B+H,该反应会放出
大量的热②I是一种常见的温室气体,它和E可以发生反应:
2E+I![]() 2F+D,F中E元素的质量分数为60%。回答问题:
2F+D,F中E元素的质量分数为60%。回答问题:
(1)①中反应的化学方程式为_____________________;
(2)化合物I的电子式为___________,它的空间构型是________________;
(3)8.0g G溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量____________g;
(4)C与过量NaOH溶液反应后溶液与过量化合物I反应的离子方程式为_____________;
(5)E在I中燃烧观察到的现象是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com