
【题目】下列叙述正确的是( )。
A.同温同压下,相同体积的物质,其物质的量一定相等
B.标准状况下,等物质的量的甲烷和一氧化碳所含的原子数一定相等
C.1 L一氧化碳气体一定比1 L氧气的质量小
D.相同条件下的一氧化碳气体和氮气,若体积相等,则质量一定相等
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列关于糖类的说法正确的是( )
A. 所有糖类物质都有甜味,但不一定都溶于水
B. 葡萄糖和果糖性质不同,但分子式相同
C. 摄入人体的纤维素在酶的作用下能水解为葡萄糖
D. 用浓硫酸与蛋白质的颜色反应鉴别部分蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物。n是元素Z的单质。通常为黄绿色气体,q的水溶液具有漂白性。0.01mol/Lr溶液的![]() 为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是
为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是

A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. ![]() 的氢化物常温常压下为液态
的氢化物常温常压下为液态
D. ![]() 的最高价氧化物的水化物为强酸
的最高价氧化物的水化物为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.纯碱和烧碱都属于碱
B.凡是能电离出H+的化合物都叫做酸
C.铝片在空气中能剧烈燃烧并放出大量的热
D.NH3的水溶液可以导电,但NH3属于非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】符合下列条件的有机物中,同分异构体(不考虑立体异构)数目最多的是( )
A.分子式为C5H10且能使溴的CCl4溶液褪色
B.分子式为C7H16且含有三个甲基
C.分子式为C4H8O2且能与NaOH溶液反应
D.分子式为C4H10O且能与钠反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示.下列判断正确的是( )
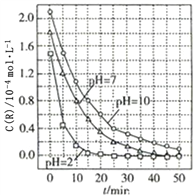
A. 在20~25min之间,pH=10时R的平均降解速率为0.04molL-1min-1
B. 溶液酸性越强,R的降解速率越小
C. R的起始浓度越小,降解速率越大
D. 50min时,pH=2和pH=7时R的降解百分率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是( )
A. 钠和冷水反应 2Na+2H2O=2Na++2OH-+H2↑
B. 石灰石与醋酸溶液反应 CaCO3+2H+=Ca2++H2O+CO2↑
C. 溴化亚铁溶液中通入少量氯气 2Br -+ Cl2=Br2+2C1-
D. NH4HCO3 溶液中加入足量的 NaOH 溶液:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资料显示“O2的氧化性随溶液pH的增大逐渐减弱”。某兴趣小组探究不同条件下KI与O2的反应.实验如下。
装置 | 烧杯中的液体 | 现象(5分钟后) |
| ①2 mL1 mol/LKI溶液+5滴淀粉 | 无明显变化 |
②2 mL1 mol/LKI溶液+5滴淀粉+2 mL0.2 mol/L HCl | 溶液变蓝 | |
③2 mL1 mol/LKI溶液+5滴淀粉+2 mL0.2 mol/L KCl | 无明显变化 | |
④2 mL1 mol/LKI溶液+5滴淀粉+2 mL0.2 mol/L CH3COOH | 溶液变蓝,颜色较②浅 |
(1)实验②中生成I2的离子方程式是___________。
(2)实验③的目的是_________________________________________________________________。
(3)实验④比②溶液颜色浅的原因是________。
(4)为进一步探究KI与O2的反应,用上表中的装置继续进行实验:
烧杯中的液体 | 现象(5小时后) |
⑤2 mLpH=8.5混有KOH的1mol/L KI溶液+5滴淀粉 | 溶液才略变蓝 |
⑥2 mLpH=10混有KOH的1mol/L KI溶液+5滴淀粉 | 无明显变化 |
I.对于实验⑥的现象.甲同学提出猜想“pH=10时O2不能氧化I-”,设计了下列装置进行实验,验证猜想。
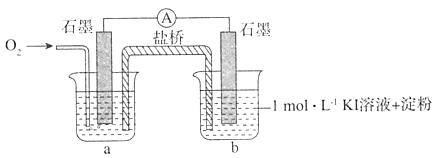
i.烧杯a中的溶液为____。
ii.实验结果表明,此猜想不成立。支持该结论的实验现象是:通入O2后,_______。
Ⅱ.乙同学向pH=10的KOH溶液(含淀粉)中滴加碘水,溶液先变蓝后迅速褪色.经检测褪色后的溶液中含有IO3-,褪色的原因是(用离子方程式表示)____________。
(5)该小组同学对实验过程进行了整体反思.推测实验①的现象产生的原因可能是______;实验⑥的现象产生的原因可能是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 以可逆反应为原理的原电池发生反应达平衡时,该电池仍有电流产生
B. 向AgCl、AgBr的饱和溶液中加入少量的AgNO3,溶液中氯离子和溴离子浓度的比值不变
C. 使用催化剂能够降低反应的△H
D. 金属发生吸氧腐蚀时,被腐蚀的速率和氧浓度无关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com