
����Ŀ����������������ѧ��FulvioCacace���˻���˼��������о������N4���ӡ�N4���ӽṹ��ͼ��ʾ����֪����1mol N��N����167 kJ����������1mol N��N�ų�942 kJ������������Ϣ�����ݣ�����˵����ȷ����
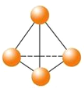
A��N4��N2��Ϊͬ���칹��
B��1mo1N4����ת��ΪN2������882kJ����
C��N4��g��=2N2��g�� ��H = - 882KJ
D��P4���������ķ��ӽṹ��N4���ƣ�1mol N4��1mol P4������6mol�Ǽ��Լ�
 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������һ�ֹ�ҵ��������Ҫ�ɷ�ΪMgCO3��Mg2SiO4������Fe��Al�������Ϊԭ���Ʊ�MgCO3��3H2O��ʵ��������£�

��1�����ܹ�������Ҫ��Ӧ���Ȼ�ѧ����ʽΪ
MgCO3(s)+2H+(aq)===Mg2+(aq)+CO2(g)+H2O(l) ��H=��50.4 kJ��mol�C1
Mg2SiO4(s)+4H+(aq)="==2" Mg2+(aq)+H2SiO3(s)+H2O(l) ��H=��225.4 kJ��mol�C1
��������ȵ�Ŀ����_____ _������H2SO4���˹���̫���ԭ����____ __��
��2������H2O2����ʱ������Ӧ�����ӷ���ʽΪ__________
��3������ͼ��ʾ��ʵ��װ�ý�����ȡ��Һ���Գ�ȥ��Һ�е�Fe3+��

��ʵ��װ��ͼ������A������Ϊ__________��
��ΪʹFe3+�����ܶ�ش�ˮ��ת�����л��࣬��ȡ�IJ�������װ��ˮ��Һ������A�м���һ�������л���ȡ���� �����á���Һ�����ظ���Ρ�
��4���벹����������ȡ��õ���ˮ��Һ�Ʊ�MgCO3��3H2O��ʵ�鷽�����߽��������Һ�еμӰ�ˮ�� �����ˡ���ˮϴ�ӹ���2��3�Σ���50���¸���õ�MgCO3��3H2O��
[��֪����Һ��pH=8.5ʱMg(OH)2��ʼ������pH=5.0ʱAl(OH)3������ȫ]��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ȷ�Ӧ2CO��g��= 2C��s����O2��g�����覤H �ͦ�S�����¶ȶ���������˵������ȷ����
A�����������Է����� B�����������Է�����
C���κ��¶��¶����Է����� D���κ��¶��¶������Է�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ӻ�ˮ����ȡ��Ĺ�ҵ������ͼ��
��1�����ϲ���I���ѻ������̬���壬����II�ֽ�֮ת��ɻ���̬���壬��Ŀ���� ��
��2��������ͨ���ȿ�����ˮ��������Br2,��������� ��
A.������ B.��ԭ�� C.�ӷ��� D.��ʴ��
��3���������������漰�����ӷ�Ӧ���£��������淽���������ʵ��Ļ�ѧ����������Ӧ���ʣ�
��Br2 + ��CO32-![]() ��BrO3��+ ��Br��+ ��
��BrO3��+ ��Br��+ ��
��4�����������д������������� Ҳ�����ö�������ˮ��Һ���գ�������������������д�������������ˮ��Һ��Ӧ�Ļ�ѧ����ʽ: ��
��5��ʵ���ҷ����廹�������ܼ���ȡ�������п������������ȡ������ ��
A.�Ҵ� B.���Ȼ�̼ C.�ռ���Һ D.��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͨ����н��еĹ����������ʵ�����ʵ�飺
���� 

��������Ϊ��Fe�������������ɫ���ݣ�Һ���Ϸ���Ϊ����ɫ
��Fe���������������ɫ���ݺ�Ѹ��ֹͣ
��Fe��Cu�Ӵ�����������������ɫ����
����˵���в���ȷ������ ��
A��������������ɫ�����ɫ�Ļ�ѧ����ʽΪ��2NO+O2�T2NO2
B�����е�����˵��Fe�����γ����ܵ������㣬��ֹFe��һ����Ӧ
C���Ա�������������˵��ϡHNO3��������ǿ��ŨHNO3
D���������������Fe��Cu֮�����ӵ����ƣ����ж�Fe�Ƿ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڽ��������������ȷ���ǣ� ��
A���ò��������β����ý��������۽���
B����̬������ʱ�������۵���1000�����ҵľ�������ǽ�������
C�������������ܶѻ���ʽֻ�����������ѻ���ʽ
D��������������ڵ���ʣ���������Һ�������ԭ��һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��黯�����У���ѧ��������ȫ��ͬ���ǣ� ��
A��NaOH��NaClO��Na2O
B��HCl �� HClO��MgCl2
C��NH3��CO2��Na2O2
D��C2H6��H2O2��C2H5OH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ���й�Ӧ�õ������У���ȷ����
A�������ȼ����Ϊ890��3kJ��mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��
CH4��g��+2O2��g��=CO2��g��+2H2O��g�� ��H= -890��3kJ��mol-1
B����֪ǿ����ǿ����ϡ��Һ�ﷴӦ���к���Ϊ57��3 kJ��mol-1�� ��1/2 H2SO4��aq��+1/2 Ba��OH��2��aq��= 1/2BaSO4��s��+H2O��l�� ��H= -57��3 kJ��mol-1
C�� 500�桢30MPa�£���0��5mol N2��1��5molH2�����ܱյ������г�ַ�Ӧ����NH3��g��������19��3kJ�� ���Ȼ�ѧ����ʽΪ��N2��g�� + 3H2��g��![]() 2NH3��g�� ��H= -38��6kJ��mol-1
2NH3��g�� ��H= -38��6kJ��mol-1
D����֪25�桢101KPa�����£�4Al��s����3O2��g����2A12O3��s�� ��H����2834��9 kJ��mol-1,
4Al��s����2O3��g����2A12O3��s�� ��H����3119��1 kJ��mol-1�� ��O2��O3�ȶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������MgCl2��Һֱ��������ʱ�������ֽ����Ϊ
A�� MgCl2 B��Mg(OH)2 C��MgO D�� Mg
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com