
ЁОЬтФПЁПЯТСаЪЕбщВйзїЛђЖдЪЕбщЪТЪЕЕФа№Ъіе§ШЗЕФгаМИИіЃЈ ЃЉ
ЂйгУХЈАБЫЎЧхЯДзіЙ§жЦБИAgClЗДгІКѓЕФЪдЙмЃЛЂкХфжЦвЛЖЈЮяжЪЕФСПХЈЖШЕФШмвКЪБЃЌЮДеёЕДвЁдШдђШмвКХЈЖШЦЋИпЃЛЂлгУЪЊШѓЕФpHЪджНВтЖЈЯЁбЮЫсЕФpHЃЛЂмгУМюЪНЕЮЖЈЙмСПШЁ20.00mL0.1mol/LKMnO4ШмвКЃЛЂнНЋNa2CO3ЙЬЬхдкДЩлсліжаМгШШШлШкЃЛЂоВЛЩїНЋБНЗгШмвКеДЕНЦЄЗєЩЯЃЌСЂМДгУNaOHЯЁШмвКЧхЯДЃЛЂпЯђЗаЬкЕФNaOHШмвКжаЕЮМгFeCl3ШмвКжЦБИFe(OH)3НКЬхЃЛЂрХфжЦFeSO4ШмвКЪБЃЌашМгШыЩйСПЬњЗлКЭЯЁбЮЫс
A.1B.2C.3D.4
ЁОД№АИЁПB
ЁОНтЮіЁП
![]() гЩгкАБЫЎКЭТШЛЏвјПЩвдЗДгІаЮГЩвјАБШмвКЃЌЙЪПЩгУХЈАБЫЎЧхЯДзіЙ§жЦБИAgClЗДгІКѓЕФЪдЙмЃЌЙЪ
гЩгкАБЫЎКЭТШЛЏвјПЩвдЗДгІаЮГЩвјАБШмвКЃЌЙЪПЩгУХЈАБЫЎЧхЯДзіЙ§жЦБИAgClЗДгІКѓЕФЪдЙмЃЌЙЪ![]() е§ШЗЃЛ
е§ШЗЃЛ
![]() ХфжЦвЛЖЈЮяжЪЕФСПХЈЖШЕФШмвКЪБЃЌЮДеёЕДвЁдШдђШмвКХЈЖШЦЋИпЃЌЙЪ
ХфжЦвЛЖЈЮяжЪЕФСПХЈЖШЕФШмвКЪБЃЌЮДеёЕДвЁдШдђШмвКХЈЖШЦЋИпЃЌЙЪ![]() е§ШЗЃЛ
е§ШЗЃЛ
![]() ЪджНВЛФмЪЊШѓЃЌгУЪЊШѓЕФpHЪджНВтЖЈЯЁбЮЫсЕФpHЃЌЛсЕМжТЯЁбЮЫсБЛЯЁЪЭЃЌВтЖЈНсЙћЦЋИпЃЌЙЪ
ЪджНВЛФмЪЊШѓЃЌгУЪЊШѓЕФpHЪджНВтЖЈЯЁбЮЫсЕФpHЃЌЛсЕМжТЯЁбЮЫсБЛЯЁЪЭЃЌВтЖЈНсЙћЦЋИпЃЌЙЪ![]() ДэЮѓЃЛ
ДэЮѓЃЛ
![]() гУМюЪНЕЮЖЈЙмСПШЁ
гУМюЪНЕЮЖЈЙмСПШЁ![]()
![]() ШмвКЃЌМюЪНЕЮЖЈЙмЕФЯ№НКЙмЛсБЛИпУЬЫсМиШмвКбѕЛЏЃЌгІИУЪЙгУЫсЪНЕЮЖЈЙмСПШЁЃЌЙЪ
ШмвКЃЌМюЪНЕЮЖЈЙмЕФЯ№НКЙмЛсБЛИпУЬЫсМиШмвКбѕЛЏЃЌгІИУЪЙгУЫсЪНЕЮЖЈЙмСПШЁЃЌЙЪ![]() ДэЮѓЃЛ
ДэЮѓЃЛ
![]() НЋNa2CO3ЙЬЬхдкДЩлсліжаМгШШШлШкЃЌЬМЫсФЦФмЙЛгылсліжаЕФЖўбѕЛЏЙшЗДгІЃЌгІИУЪЙгУЬњлсліЃЌЙЪ
НЋNa2CO3ЙЬЬхдкДЩлсліжаМгШШШлШкЃЌЬМЫсФЦФмЙЛгылсліжаЕФЖўбѕЛЏЙшЗДгІЃЌгІИУЪЙгУЬњлсліЃЌЙЪ![]() ДэЮѓЃЛ
ДэЮѓЃЛ
![]() ЧтбѕЛЏФЦОпгаЧПСвЕФИЏЪДадЃЌЫљвдВЛФмгУДѓСПЕФNaOHЯЁШмвКГхЯДЃЌПЩвдгУОЦОЋЯДШЅЃЌЙЪ
ЧтбѕЛЏФЦОпгаЧПСвЕФИЏЪДадЃЌЫљвдВЛФмгУДѓСПЕФNaOHЯЁШмвКГхЯДЃЌПЩвдгУОЦОЋЯДШЅЃЌЙЪ![]() ДэЮѓЃЛ
ДэЮѓЃЛ
![]() ЯђЗаЬкЕФNaOHШмвКжаЕЮМгFeCl3ШмвКЃЌЗДгІЩњГЩЕФЪЧЧтбѕЛЏЬњГСЕэЃЌжЦБИЧтбѕЛЏЬњНКЬхЕФЗНЗЈЮЊЃКНЋБЅКЭТШЛЏЬњШмвКМгШыЕНЗаЫЎжаЃЌМЬајМгШШжСвКЬхГЪКьКжЩЋЃЌЙЪ
ЯђЗаЬкЕФNaOHШмвКжаЕЮМгFeCl3ШмвКЃЌЗДгІЩњГЩЕФЪЧЧтбѕЛЏЬњГСЕэЃЌжЦБИЧтбѕЛЏЬњНКЬхЕФЗНЗЈЮЊЃКНЋБЅКЭТШЛЏЬњШмвКМгШыЕНЗаЫЎжаЃЌМЬајМгШШжСвКЬхГЪКьКжЩЋЃЌЙЪ![]() ДэЮѓЃЛ
ДэЮѓЃЛ
![]() ХфжЦFeSO4ШмвКЪБЃЌЮЊСЫЗРжЙбЧЬњРызгБЛбѕЛЏЃЌашвЊМгШыЩйСПЬњЗлЃЛЮЊСЫвжжЦбЧЬњРызгЕФЫЎНтЃЌЛЙашвЊМгШыЩйСПЯЁСђЫсЃЌЙЪДэЮѓЃЛ
ХфжЦFeSO4ШмвКЪБЃЌЮЊСЫЗРжЙбЧЬњРызгБЛбѕЛЏЃЌашвЊМгШыЩйСПЬњЗлЃЛЮЊСЫвжжЦбЧЬњРызгЕФЫЎНтЃЌЛЙашвЊМгШыЩйСПЯЁСђЫсЃЌЙЪДэЮѓЃЛ
ИљОнвдЩЯЗжЮіПЩжЊЃЌа№Ъіе§ШЗЕФга2ИіЃЌЙЪBе§ШЗЃЛ
ЙЪбЁBЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙЄвЕЩЯЁАЙЬЖЈЁБКЭРћгУCO2ФмгааЇЕиМѕЧсЁАЮТЪваЇгІЁБЁЃ
IЃЎЙЄвЕЩЯе§дкбаОПРћгУCO2РДЩњВњМзДМШМСЯЕФЗНЗЈЃЌИУЗНЗЈЕФЛЏбЇЗНГЬЪНЪЧЃКCO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ЁїH=-49.0kJmolЉ1ЃЌФГПЦбЇЪЕбщНЋ6molCO2КЭ8 molH2ГфШывЛШнЛ§ЮЊ2LЕФУмБеШнЦїжа(ЮТЖШБЃГжВЛБф)ЃЌВтЕУH2ЕФЮяжЪЕФСПЫцЪБМфБфЛЏШчЯТЭМжаЪЕЯпЫљЪОЃЈЭМжазжФИКѓЕФЪ§зжБэЪОЖдгІЕФзјБъЃЉЃК
CH3OH(g)+H2O(g) ЁїH=-49.0kJmolЉ1ЃЌФГПЦбЇЪЕбщНЋ6molCO2КЭ8 molH2ГфШывЛШнЛ§ЮЊ2LЕФУмБеШнЦїжа(ЮТЖШБЃГжВЛБф)ЃЌВтЕУH2ЕФЮяжЪЕФСПЫцЪБМфБфЛЏШчЯТЭМжаЪЕЯпЫљЪОЃЈЭМжазжФИКѓЕФЪ§зжБэЪОЖдгІЕФзјБъЃЉЃК
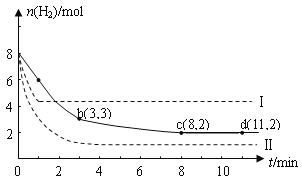
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉвдЯТЫЕЗЈВЛе§ШЗЕФЪЧЃЈ__________ЃЉ
AЃЎ0ЁЋ1minЕФЦНОљЗДгІЫйТЪДѓгк3ЁЋ4minЕФЦНОљЗДгІЫйТЪ
BЃЎДяЕНЦНКтЪБH2ЕФзЊЛЏТЪЮЊ75%
CЃЎ дкЦфЫќЬѕМўВЛБфЪБЃЌШєЬсИпЗДгІЕФЮТЖШе§ЗДгІЫйТЪдіДѓЃЌФцЗДгІЫйТЪМѕаЁ
ЃЈ2ЃЉИУЗДгІдк0 ЁЋ8 minФкCO2ЕФЦНОљЗДгІЫйТЪЪЧ_______ЁЃ
ЃЈ3ЃЉИУЗДгІЕФЦННжГЃЪ§K=______________ЁЃ
ЃЈ4ЃЉНіИФБфФГвЛЬѕМўдйНјааЪЕбщЃЌВтЕУH2ЕФЮяжЪЕФСПЫцЪБМфБфЛЏШчЭМжаащЯпЫљЪОЁЃгыЪЕЯпЯрБШЃЌащЯпIИФБфЕФЬѕМўПЩФмЪЧ_________ЁЃШєЪЕЯпЖдгІЬѕМўЯТЦНКтГЃЪ§ЮЊKЃЌащЯпIЖдгІЬѕМўЯТЦНКтГЃЪ§ЮЊK1ЃЌащЯпIIЖдгІЬѕМўЯТЦНКтГЃЪ§ЮЊK2ЃЌдђKЁЂK1КЭK2ЕФДѓаЁЙиЯЕЪЧ____ЁЃ
IIЃЎМКжЊ25ЁцЪБЃЌввЫсКЭЬМЫсЕФЕчРыЦНКтГЃЪ§ШчЯТБэЃК
ЮяжЪЕФЛЏбЇЪН | CH3COOH | H2CO3 | |
ЕчРыЦНКтГЃЪ§ | K=1.8ЁС10Ѓ5 | K1=4.3ЁС10Ѓ7 | K2=5.6ЁС10Ѓ11 |
ЃЈ1ЃЉгУБЅКЭАБЫЎЮќЪеCO2ПЩЕУЕНNH4HCO3ШмвКЃЌШєвбжЊCH3COONH4ШмвКpH=7ЃЌдђ(NH4)2CO3ШмвКЯд_____(ЬюЁАЫсадЁБЁЂЁАМюадЁБЛђЁАжаадЁБ)ЁЃ
ЃЈ2ЃЉ25ЁцЪБЃЌдк0ЃЎlmolLЉ1ввЫсШмвКжаМгШывЛЖЈСПЕФNaHCO3ЃЌБЃГжЮТЖШВЛБфЃЌЫљЕУЛьКЯвКЕФpH=6ЃЌФЧУДЛьКЯвКжа![]() =_______ЃЛИУЛьКЯШмвКжаЕФРызгХЈЖШгЩДѓЕНаЁЕФЫГађЮЊЃК________________ЁЃ
=_______ЃЛИУЛьКЯШмвКжаЕФРызгХЈЖШгЩДѓЕНаЁЕФЫГађЮЊЃК________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдкЦНКтЬхЯЕCa(OH)2(s) ![]() Ca2++2OH -жаЃЌФмЪЙc(Ca2+)МѕаЁЃЌЖјЪЙc(OH -)діДѓЕФЪЧЃКЃЈ ЃЉ
Ca2++2OH -жаЃЌФмЪЙc(Ca2+)МѕаЁЃЌЖјЪЙc(OH -)діДѓЕФЪЧЃКЃЈ ЃЉ
A.МгШыЩйСПMgCl2ЙЬЬхB.МгШыЩйСПNa2CO3ЙЬЬх
C.МгШыЩйСПKClЙЬЬхD.МгШыЩйСПCa(OH)2ЙЬЬх
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЃК![]() ЪБЃЌ
ЪБЃЌ![]() ЃЌ
ЃЌ![]() ЃЌ
ЃЌ![]() ЃЌ
ЃЌ![]() ЃЌ
ЃЌ![]() ЁЃ
ЁЃ
![]() ШмвККЭNaHAШмвКЗДгІЕФжївЊРызгЗНГЬЪНЮЊ________________________________
ШмвККЭNaHAШмвКЗДгІЕФжївЊРызгЗНГЬЪНЮЊ________________________________![]() ВЛПМТЧ
ВЛПМТЧ![]() гы
гы![]() ЗЂЩњбѕЛЏЛЙдЗДгІ
ЗЂЩњбѕЛЏЛЙдЗДгІ![]() ЁЃ
ЁЃ
![]() ШмвКжаРызгХЈЖШгЩДѓЕНаЁЕФЫГађЮЊ ____________________________ЁЃ
ШмвКжаРызгХЈЖШгЩДѓЕНаЁЕФЫГађЮЊ ____________________________ЁЃ
![]() ЪБЃЌНЋ
ЪБЃЌНЋ![]() ЕФHCOOHШмвККЭ
ЕФHCOOHШмвККЭ![]() ЕФ
ЕФ![]() ШмвКЗжБ№гы
ШмвКЗжБ№гы![]() ЕФ
ЕФ![]() ШмвКЛьКЯЃЌЪЕбщВтЕУВњЩњЕФЦјЬхЬхЛ§
ШмвКЛьКЯЃЌЪЕбщВтЕУВњЩњЕФЦјЬхЬхЛ§![]() ЫцЪБМф
ЫцЪБМф![]() БфЛЏЕФЪОвтЭМШчЭМЫљЪОЃК
БфЛЏЕФЪОвтЭМШчЭМЫљЪОЃК
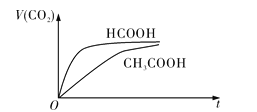
![]() ЕФЕчРыЦНКтГЃЪ§БэДяЪН
ЕФЕчРыЦНКтГЃЪ§БэДяЪН![]() __________________________ЁЃ
__________________________ЁЃ
![]() ЗДгІГѕЪМНзЖЮЃЌСНжжШмвКВњЩњ
ЗДгІГѕЪМНзЖЮЃЌСНжжШмвКВњЩњ![]() ЦјЬхЕФЫйТЪДцдкУїЯдВювьЕФдвђЪЧ__________________________________________________________________________________ЃЌЗДгІНсЪјКѓЫљЕУСНШмвКжаЃЌ
ЦјЬхЕФЫйТЪДцдкУїЯдВювьЕФдвђЪЧ__________________________________________________________________________________ЃЌЗДгІНсЪјКѓЫљЕУСНШмвКжаЃЌ![]() ____________
____________![]() ЬюЁА
ЬюЁА![]() ЁБЁА
ЁБЁА![]() ЁБЛђЁА
ЁБЛђЁА![]() ЁБ
ЁБ![]() ЁЃ
ЁЃ
![]() ЪБЃЌФГШмвКжаКЌга
ЪБЃЌФГШмвКжаКЌга![]() ЁЂ
ЁЂ![]() МгШыKOHЙЬЬхвдЕїНкШмвК
МгШыKOHЙЬЬхвдЕїНкШмвК![]() КіТдШмвКЬхЛ§ЕФБфЛЏЁЂКіТд
КіТдШмвКЬхЛ§ЕФБфЛЏЁЂКіТд ![]() ЕФЛгЗЂКЭЗжНт
ЕФЛгЗЂКЭЗжНт![]() ЁЃЕБpHЮЊ7ЪБЃЌФмЗёга
ЁЃЕБpHЮЊ7ЪБЃЌФмЗёга![]() ГСЕэЩњГЩЃП________
ГСЕэЩњГЩЃП________![]() ЬюЁАФмЁБЛђЁАЗёЁБ
ЬюЁАФмЁБЛђЁАЗёЁБ![]() ЁЃ
ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
A. ЬьШЛЦјЁЂЫЎУКЦјЁЂвКЛЏЪЏгЭЦјОљЪЧЩњЛюжаГЃгУЕФШМСЯЃЌЫќУЧЕФжївЊГЩЗжЖМЪЧЛЏКЯЮя
B. ЁАжаЙњЬьблЁБЕФЁАблПєЁБЪЧИжЬњНсГЩЕФШІСКЃЌЪєгкН№ЪєВФСЯ
C. жЦВЃСЇКЭЫЎФрЖМвЊгУЕНЪЏЛвЪЏдСЯ
D. 1996ФъШЫЙЄКЯГЩСЫЕк112КХдЊЫиц(Cn)ЃЌЪЂЗХцЕФШнЦїЩЯгІИУЬљЕФБъЧЉЪЧ![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдкУмБеШнЦїжагаЗДгІmA(g)+nB(g) ![]() pC(g) (е§ЗДгІЮќШШ)ДІгкЦНКтзДЬЌЃЌвбжЊm + n > pЃЌдђЯТСаЫЕЗЈе§ШЗЕФЪЧ ЃЈ ЃЉ
pC(g) (е§ЗДгІЮќШШ)ДІгкЦНКтзДЬЌЃЌвбжЊm + n > pЃЌдђЯТСаЫЕЗЈе§ШЗЕФЪЧ ЃЈ ЃЉ
ЂйЩ§ЮТЪБc(B)/ c(C)БШжЕМѕаЁ ЂкГфШыCЃЌдђAЁЂBЕФЮяжЪЕФСПдіДѓ ЂлГфШыBЃЌдђAЕФзЊЛЏТЪБфДѓЂмМгШыДпЛЏМСЃЌЦјЬхЕФзмЮяжЪЕФСПВЛБф
A.ЂйЂкB.ЂкЂлC.ЂлЂмD.ЂйЂкЂлЂм
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЪЕбщВйзїгыАВШЋЪТЙЪДІРэе§ШЗЕФЪЧ
A.Г§ШЅKClШмвКжаЕФЩйСПMgCl2ЃКМгШыЪЪСПNaOHШмвКЃЌЙ§ТЫ
B.АбВЃСЇЙмВхШыЯ№НКШћПзЪБЃЌгУКёВМЛЄЪжЃЌНєЮегУЫЎЪЊШѓЕФВЃСЇЙмВхШыЖЫЃЌЛКТ§а§НјШћПз
C.гУЪдЙмМаДгЪдЙмЕзгЩЯТЭљЩЯМазЁОрРыЙмПкдМ![]() ДІЃЌЪжГжЪдЙмМаГЄБњФЉЖЫЃЌНјааМгШШ
ДІЃЌЪжГжЪдЙмМаГЄБњФЉЖЫЃЌНјааМгШШ
D.гУЕуШМЕФЛ№ВёдквКЛЏЦјИжЦППкМьбщЪЧЗёТЉЦј
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСажааФдзгЕФдгЛЏЙьЕРРраЭКЭЗжзгМИКЮЙЙаЭВЛе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
A.PCl3жа Pдзгsp3дгЛЏЃЌЮЊШ§НЧзЖаЮ
B.BCl3жаBдзгsp2дгЛЏЃЌЮЊЦНУцШ§НЧаЮ
C.CS2жаCдзгspдгЛЏЃЌЮЊжБЯпаЮ
D.H2SжаSдзгspдгЛЏЃЌЮЊжБЯпаЮ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com