
【题目】综合利用CO2、CO对构建低碳社会有重要意义。
⑴ Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是_______。
a.可在碱性氧化物中寻找
b.可在ⅠA、ⅡA族元素形成的氧化物中寻找
c.可在具有强氧化性的物质中寻找
⑵ Li4SiO4可用于吸收、释放CO2,原理是:在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生。写出CO2与Li4SiO4反应的化学方程式 ;该反应为_______(填“吸”或者“放”)热反应,原因是 _____________。
⑶ CO与H2在催化剂作用下发生如下反应:CO(g)+2H2(g)![]() CH3OH(g)。对此反应进行如下研究:某温度下在某2 L恒容密闭容器中分别充入1.2 mol CO和1 mol H2,达到平衡测得有0.4 mol CH3OH(g),则该反应平衡常数值为_______。
CH3OH(g)。对此反应进行如下研究:某温度下在某2 L恒容密闭容器中分别充入1.2 mol CO和1 mol H2,达到平衡测得有0.4 mol CH3OH(g),则该反应平衡常数值为_______。
⑷ 在200℃并用钴做催化剂的条件下,CO与H2可合成C5H12(汽油的一种成分),可减少碳排放。反应中能量变化如下图所示,写出该反应的热化学方程式______________。

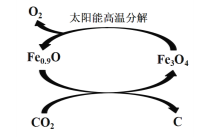
⑸ 如下图所示,利用缺铁氧化物[如Fe0.9O]可实现CO2的综合利用、构建低碳环保社会。请说明该转化的优点_____________________。
【答案】(14分,每空2分)(1)a b
(2)2CO2+Li4SiO4![]() 2Li2CO3+SiO2;放,
2Li2CO3+SiO2;放,
升高温度,平衡向逆向进行,说明逆反应为吸热反应,所以正反应为放热反应。(3)50
(4)5CO(g)+11H2(g)=C5H12(g)+5H2O(g) H= +(b-a) kJ/mol
(5)将CO2转化为C和O2;利用了太阳能;Fe3O4可循环使用(写出一条给1分)。
【解析】
试题分析:(1)a.Li2O、Na2O、MgO均属于碱性氧化物,均能吸收酸性氧化物CO2,可在碱性氧化物中寻找吸收CO2的其他物质,故a正确;b.Li2O、Na2O、MgO均能吸收CO2,钠、镁为ⅠA、ⅡA族元素,所以可在ⅠA、ⅡA族元素形成的氧化物中寻找吸收CO2的其他物质,故b正确;
c.Li2O、Na2O、MgO均能吸收CO2,但它们都没有强氧化性,且吸收二氧化碳与氧化还原无关,故c错误;故答案为ab;
(2)在500℃,CO2与Li4SiO4接触后生成Li2CO3,反应物为CO2与Li4SiO4,生成物有Li2CO3,根据质量守恒可知产物还有Li2SiO3,所以化学方程式为:CO2+Li4SiO4![]() Li2CO3+Li2SiO3;由于升高温度平衡左移,故正反应为放热反应;
Li2CO3+Li2SiO3;由于升高温度平衡左移,故正反应为放热反应;
(3)CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
起始:1.2mol 1mol 0
转化:0.4mol 0.8mol 0.4mol
平衡:0.8mol 0.2mol 0.4mol
所以:k=![]() =50(mol/L)-2;
=50(mol/L)-2;
(4)根据图1可知,反应物为5molCO气体和11mol氢气,产物为1mol戊烷气体和5mol水蒸汽,由于反应物的能量低于产物的能量,故此反应为吸热反应,且吸收(b-a)kJ,故热化学方程式为:5CO(g)+11H2(g)═C5H12(g)+5H2O(g) △H=+(b-a)kJ/mol;
(5)根据图示可知,Fe0.9O可以将CO2转化为Fe3O4和C,而Fe3O4又在太阳能高温作用下分解为Fe0.9O和氧气,在此循环过程中,利用了太阳能,Fe3O4可循环使用,且能将CO2转化为C和O2,减少了空气污染。


科目:高中化学 来源: 题型:
【题目】钛矿工业中的酸性废水富含Ti、Fe等元素,其综合利用如下:

已知:TiO2+易水解,只能存在于强酸性溶液中。
(1)TiO2+钛的化合价为
(2)步骤I中检验钛矿废水中加入铁屑是否足量的试剂是 。
(3)操作a是蒸发浓缩、冷却结晶、 。
(4)步骤Ⅲ中发生反应的化学方程式为____________;反应温度一般需控制在35℃以下,其目的是 。
(5)已知![]() s。步骤Ⅲ中,FeCO3达到溶解平衡时,若室温下测得溶液的pH为8.5,c(Fe2+)=1×10-6 mol/L。试判断所得的FeCO3中________(填“有”或“没有”)Fe(OH)2;步骤Ⅳ中,为了得到较为纯净的Fe2O3,除了适当的温度外,还需要采取的措施是 。
s。步骤Ⅲ中,FeCO3达到溶解平衡时,若室温下测得溶液的pH为8.5,c(Fe2+)=1×10-6 mol/L。试判断所得的FeCO3中________(填“有”或“没有”)Fe(OH)2;步骤Ⅳ中,为了得到较为纯净的Fe2O3,除了适当的温度外,还需要采取的措施是 。
(6)向“富含TiO2+溶液”中加入Na2CO3粉末得到固体TiO2·nH2O。请结合原理和化学用语解释其原因 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式,正确的是( )
A.澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2===CaCO3↓+H2O
B.碳酸钠溶液中加入二氧化硅:CO32-+SiO2===SiO32-+CO2↑
C.二氧化硅与烧碱溶液反应:SiO2+2OH-===SiO32-+H2↑
D.硅酸与烧碱溶液中和:H2SiO3+2OH-===SiO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室拟用浓盐酸与二氧化锰反应制取纯净的氯气。并验证氯气的性质。
(Ⅰ)制取氯气:
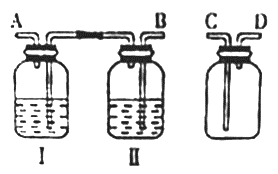
(1)按气体从左到右流动的方向将下列装置进行连接(填字母〉,H→_____、_______→ _______。广口瓶Ⅱ中的试剂为________。
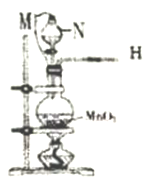
(2)仪器N的名称是_______;M是连通上下玻璃仪器的橡胶管,其目的是__________________;写出圆底烧瓶中发生反应的离子方程式_________________。
(3)连接好仪器后,上述装置存在一个明显的缺陷,你的改进方法是_______________。
(Ⅱ)验证氯气的性质:将从上述发生装置H处导出的气体依次经过下列装置验证氯气的性质(其他相关装置已略去)
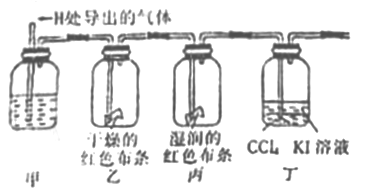
(4)丁中出现的现象是__________________,该反应证明了氯气的____________性。
(5)证明HClO具有漂白性的实验现象是__________________,甲中的试剂是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校课外探究小组欲在实验室条件下制取少量纯净的无水氯化铝。查阅到以下资料:无水氯化铝是白色晶体,易吸收水分,常压下在177.8 ℃升华,遇潮湿空气即产生大量白雾。用于有机合成和石油工业的催化剂,以及用于处理润滑油等。他们设计了以下装置,请结合题意回答问题:

(1)A装置中发生反应的化学方程式为:_________________________
(2)装置B的作用是__________________________
(3)请给标记为F的实线方框选择合适的装置_______

(4)AlCl3遇潮湿空气即产生大量白雾的原因是_________________(结合化学方程式说明)。
(5)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,该小组同学提出酸碱中和滴定法测定方案。方案如下:首先准确量取残余清液稀释一定的倍数后作为试样,平行做了4次滴定。实验中所用NaOH溶液浓度为0.2000 mol·L-1,以下是实验记录与数据处理(不考虑NaOH与残液中其他成分的反应)。
①若本实验需要NaOH标准溶液80mL,则配制该标准溶液需要用到玻璃仪器有玻璃棒,烧杯_______
②经计算,该次滴定测的试样中盐酸浓度为_______________mol·L-1。
③在本实验的滴定过程中,下列操作会使实验结果偏小的是___________(填写序号)。
A.开始滴定时滴定管尖嘴处留有气泡,滴定结束气泡消失
B.未用标准NaOH溶液润洗滴定管
C.锥形瓶中加入待测盐酸后,再加少量水
D.锥形瓶在滴定时剧烈摇动,有少量液体溅出
e.滴定前锥形瓶用待测盐酸润洗
f.观察读数时,滴定前仰视,滴定后俯视
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于SO2的叙述中,正确的是
A.SO2的摩尔质量是64g
B.1molSO2中所含分子数约为6.02×1023
C.1molSO2的质量是64g/mol
D.常温常压下,1molSO2的体积为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应①X(g)+2Y(g)![]() 2Z(g)、②2M(g)
2Z(g)、②2M(g)![]() N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦,可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦,可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:

下列判断正确的是:
A 反应①的正反应是吸热反应
B 达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15
C 达平衡(I)时,X的转化率为5/11
D 在平衡(I)和平衡(II)中,M的体积分数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20mL0.5mol·L-1的醋酸溶液中逐渐加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如所示。下列关于混合溶液的相关说法错误的是

A.醋酸的电离平衡常数:B点>A点
B.由水电离出的c(OH-):B点>C点
C.从A点到B点,混合溶液中可能存在:c(CH3COO-)=c(Na+)
D.从B点到C点,混合溶液中一直存在:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com