
����Ŀ��Ca(NO2)2�����ڵ��ӡ��DZ���ұ��ҵ��ij�������������з����Ʊ�Ca(NO2)2������ȥ�������������Ⱦ�������������ͼ��
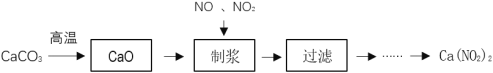
��NO2��NO��Ca(OH)2�TCa(NO2)2��H2O��4NO2��2Ca(OH)2�TCa(NO2)2��Ca(NO3)2��2H2O
��������������2![]() +4H++2I-=2NO��+I2+2H2O��2
+4H++2I-=2NO��+I2+2H2O��2![]() +I2=
+I2=![]() +2I-
+2I-
(1)Ϊ�ӿ�CaCO3�ķֽ����ʣ����Բ�ȡ�Ĵ�ʩ��___����дһ�֣���
(2) ���ƽ�������������Ca(OH)2�Ļ�ѧ����ʽ��___��
(3)�ù��������������NO��NO2���ʵ���֮�Ƚӽ�1��1����n(NO2)��n(NO)��1��1����ᵼ��___��
(4)Ca(NO2)2��Ʒ���ȵIJⶨ
��ȷ��ȡ1.50gCa(NO2)2��Ʒ���250ml����Һ��ȡ25mL����ƿ�У����������KI��Һ��������Һ���μ�ϡ���ᣬ��Һ������
����0.1mol��L-1Na2S2O3��Һ�ζ���Һ����ɫ������Na2S2O3��Һ�����Ϊ20.00mL���ݴ˼�����Ʒ��Ca(NO2)2�Ĵ��ȣ�д���������___��
���𰸡���߷�Ӧ�¶ȣ���CaCO3ĥ��� CaO+H2O=Ca(OH)2 ��ƷCa(NO2)2��Ca(NO3)2�������� 88%
��������
CaCO3�ڸ��������·ֽ⣬����CaO��CO2���壻���ɵ�CaO����ˮ����Ca(OH)2��ͨ��NO��NO2�Ļ�����壬������ӦNO2��NO��Ca(OH)2�TCa(NO2)2��H2O����NO2��������ᷢ����Ӧ4NO2��2Ca(OH)2�TCa(NO2)2��Ca(NO3)2��2H2O���Ӷ�ʹCa(NO2)2�л���Ca(NO3)2��
(1)Ϊ�ӿ�CaCO3�ķֽ����ʣ�����ͨ��������Ӧ�¶Ȼ�����Ӵ�����ķ��������Բ�ȡ�Ĵ�ʩ����߷�Ӧ�¶ȣ���CaCO3ĥ��ȡ���Ϊ����߷�Ӧ�¶ȣ���CaCO3ĥ��ȣ�
(2) ���ƽ��������У�CaO��H2O��Ӧ����Ca(OH)2����Ӧ�Ļ�ѧ����ʽ��CaO+H2O=Ca(OH)2����Ϊ��CaO+H2O=Ca(OH)2��
(3)�ù��������������NO��NO2���ʵ���֮�Ƚӽ�1��1����n(NO2)��n(NO)��1��1��������ӦNO2��NO��Ca(OH)2�TCa(NO2)2��H2O֮���ֻᷢ����Ӧ4NO2��2Ca(OH)2�TCa(NO2)2��Ca(NO3)2��2H2O���Ӷ����²�ƷCa(NO2)2��Ca(NO3)2�������ߡ���Ϊ����ƷCa(NO2)2��Ca(NO3)2�������ߣ�
(4)�ɷ�Ӧ����ʽ��2![]() +4H++2I-=2NO��+I2+2H2O��2
+4H++2I-=2NO��+I2+2H2O��2![]() +I2=
+I2=![]() +2I-���ɽ������¹�ϵʽ��Ca(NO2)2����2 Na2S2O3��25mL ���Ƶ���Һ������Na2S2O3�����ʵ���n(Na2S2O3)= 0.1mol��L-1��0.02000L=0.002mol����ԭ��Ʒ������Ca(NO2)2������Ϊ��m[Ca(NO2)2]=
+2I-���ɽ������¹�ϵʽ��Ca(NO2)2����2 Na2S2O3��25mL ���Ƶ���Һ������Na2S2O3�����ʵ���n(Na2S2O3)= 0.1mol��L-1��0.02000L=0.002mol����ԭ��Ʒ������Ca(NO2)2������Ϊ��m[Ca(NO2)2]=![]() =1.32g����Ʒ��Ca(NO2)2�Ĵ���Ϊ
=1.32g����Ʒ��Ca(NO2)2�Ĵ���Ϊ![]() =88%����Ϊ��88%��
=88%������88%��


 ǧ�������������ĩ�����Ծ�����ϵ�д�
ǧ�������������ĩ�����Ծ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
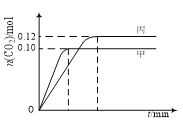
����Ŀ��һ���¶��£��������ݻ���Ϊ2.0 L�ĺ����ܱ������з�����Ӧ��2NO(g)��2CO(g)![]() N2(g)��2CO2(g)������������ʼ���ʵ����뷴Ӧ�¶����±���ʾ����Ӧ�����мס���������CO2�����ʵ�����ʱ��仯��ϵ����ͼ��ʾ������˵����ȷ����
N2(g)��2CO2(g)������������ʼ���ʵ����뷴Ӧ�¶����±���ʾ����Ӧ�����мס���������CO2�����ʵ�����ʱ��仯��ϵ����ͼ��ʾ������˵����ȷ����
���� | �¶�/�� | ��ʼ���ʵ���/mol | |
NO (g) | CO (g) | ||
�� | T1 | 0.20 | 0.20 |
�� | T1 | 0.30 | 0.30 |
�� | T2 | 0.20 | 0.20 |
A. �÷�Ӧ������ӦΪ���ȷ�Ӧ
B. �ﵽƽ��ʱ������CO2����������ȼ��еĴ�
C. T1��ʱ������ʼʱ����г���0.40 mol NO��0.40mol CO��0.40mol N2��0.40mol CO2����Ӧ�ﵽ��ƽ��ǰv(��)��v(��)
D. T2��ʱ������ʼʱ����г���0.06mol N2��0.12 mol CO2�����ƽ��ʱN2��ת���ʴ���40%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƣ�NaClO2����һ�ָ�Ч��Ư�����������������ڸ�����ά��ijЩʳƷ��Ư�ס�����ѷ��Mathieson�����Ʊ��������Ƶ��������£�
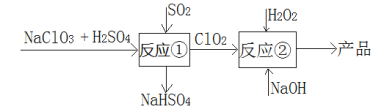
����˵��������ǣ� ��
A.��Ӧ�ٽΣ��μӷ�Ӧ��NaClO3��SO2�����ʵ���֮��Ϊ2��1
B.����Ӧ��ͨ��ԭ�����ʵ�֣���ClO2����������
C.��Ӧ���е�H2O2����NaClO4����
D.��Ӧ�������£�ClO2�������Դ���H2O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼��������������������Ĵ�������������������о����ȵ����⡣����β���к��к���һ����̼��һ��������������(Pd)�Ƚ�������������Ѹ�ٽ�����ת��Ϊ���Ķ�����̼�͵�����
��1��������λ��ͬ�У�����������һ���ڣ�����Ԫ�����ڱ���λ����__����̬��ԭ�ӵļ۵��ӵĵ����Ų�ͼΪ__��
��2��C��N��O�ĵ�һ�������ɴ�С��˳��Ϊ__��
��3��SO2���ӵ�VSEPR����Ϊ__��SO3��������ԭ�ӵ��ӻ���ʽΪ__��N2O��CO2��Ϊ�ȵ����壬��N2O������Oֻ��һ��N������N2O�Ŀռ乹��Ϊ_�������е�������������Ŀ֮����__��
��4����������3����3������ԭ�ӱ˴�ƽ�е�p����Ӳ�����ص��γɵ�������һ�����������У�������֮���γ�һ��������һ��2����������һ��3������������3��������__(������������������)��������һ����������Fe2+������ɫ[Fe(H2O)5NO]2+���ӣ�Ϊ�����������ӵķ�Ӧ֮һ��[Fe(H2O)5NO]2+��������λ����__��
��5��CO���γ��۵�Ϊ-20�棬�е�Ϊ103��������Fe(CO)5��Fe(CO)5��������Ԫ�صĻ��ϼ�Ϊ___������__���塣
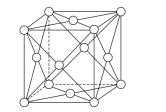
��6���پ���ľ�����ͼ�������ı߳�Ϊapm��NA��ʾ�����ӵ�������ֵ�����ٵ��ʵ��ܶ�Ϊ___g/cm3(�г�����ʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ķ����в��Ϻش���Ӧ���⣺һ������50kg�Ľ����˵����ں���2g����2g���������ڲ����Ե��ʵ���ʽ���ڵģ�������Fe2+��Fe3+����ʽ���ڡ�Fe2+�ױ����գ���ƶѪ�߲�����ʱ��Ӧ���躬Fe2+�������Σ�����������(FeSO4)������ά����C����ʹʳ���е�Fe3+ת��ΪFe2+���������������ա�
�������о�������![]() ��ת����Aת����Fe2+����________������������������ԭ������ͬ����Ӧ��Bת����Fe3+��________����
��ת����Aת����Fe2+����________������������������ԭ������ͬ����Ӧ��Bת����Fe3+��________����
��������ά����C����ʹʳ���е�Fe3+ת��ΪFe2+������仰ָ��ά����C����һ��Ӧ����________��������________�ԡ�
��ij�������ų��ķ�Һ�к���Ag+��Ba2+��Cu2+���ֽ��������ӣ�������CO32����OH����Cl�����ֲ�ͬ�������ӷֱ�����������������һ�γɳ�����ȥ�����������ӵ���ȷ˳����_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������廯����A(����R��δ֪����)��һ�������¿�ת��Ϊ����ϵ�����ʡ�
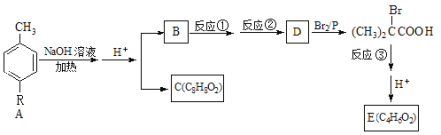
��֪��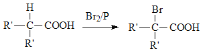 (R��Ϊ���)
(R�����)
�ش��������⣺
(1)A�Ľṹ��ʽ___________________________��B�Ľṹ��ʽ____________________��
(2)д����������������C��һ��ͬ���칹��Ľṹ��ʽ_______________________��
(I)�������ࣻ(II)������ֻ��һ��ȡ������(III)�ܷ���������Ӧ��
(3)���鷴Ӧ���Ƿ���ȫ�ķ�����_______________________________________________��
(4)��Ӧ�ٷ�Ӧ������______________________________��
(5)д����Ӧ�۵Ļ�ѧ����ʽ___________________________________________________��
(6) E���Ժϳɸ߾��д���ø߾���Ľṹ��ʽ__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ 4NH3+5O2 = 4NO+6H2O(g)������Ӧ���ʷֱ��� v(NH3)��v(O2)��v(NO)��v(H2O)��ʾ������ȷ�Ĺ�ϵ��( )
A.v(O2)=![]() v(NH3)B.v(H2O)=
v(NH3)B.v(H2O)= ![]() v(O2)C.v(H2O)=
v(O2)C.v(H2O)=![]() v(NH3)D.v(NO)=
v(NH3)D.v(NO)= ![]() v(O2)
v(O2)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������X������Ԫ����ɣ�ijѧϰС�����������ʵ�飺
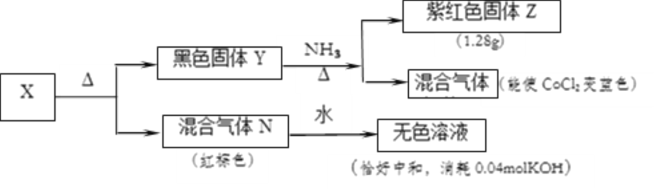
(1)������X�Ļ�ѧʽΪ___________
(2)�������Nͨ��������NaOH��Һ�У�ǡ����ȫ��Ӧ����һ���Σ������ӷ�Ӧ����ʽΪ______________��
(3)��ɫ����Y��NH3�Ļ�ѧ����ʽΪ____________
(4)����X 3H2O����ʵ�飬��170��ʱ��������һ���м����W�� 0.1mol������W����0.6molHCl�պ���ȫ��Ӧ����0.1mol������W�ټ����������ɺ�ɫ����Y������Ϊ32.0g������W�Ļ�ѧʽΪ______________��
(5)�������N�ж���Ϊ���������������ñ��շۣ�Na2S2O4�����ա���˵���������N���ñ��շ����յ�����___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״̬�£�������̬�����������ܶ���1.16g��L��1���û������������̬����������Ȳ����ܵ���(����)
A.2��5B.1��5C.9��5D.16��5
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com