
【题目】下列指定反应的离子方程式正确的是( )
A.向AlCl3溶液中加入过量的氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH![]()
B.向![]() 溶液中通入少量CO2:2
溶液中通入少量CO2:2![]() +CO2+H2O→2
+CO2+H2O→2![]() +CO
+CO![]()
C.向[Ag(NH3)2]OH溶液中加入盐酸:Ag++Cl-=AgCl↓
D.向稀硝酸中滴加Na2SO3溶液:SO![]() +2H+=SO2↑+H2O
+2H+=SO2↑+H2O
【答案】A
【解析】
A.NH3·H2O属于弱碱,Al(OH)3不能溶解在弱碱溶液中,因此向AlCl3溶液中加入过量的氨水的离子方程式为:Al3++3NH3·H2O=Al(OH)3↓+3NH4+,故A正确;
B.因苯酚的酸性强于HCO3-,因此向苯酚钠溶液中通入少量CO2所发生的离子方程式为:![]() +CO2+H2O→
+CO2+H2O→![]() ↓+HCO3-,故B错误;
↓+HCO3-,故B错误;
C.[Ag(NH3)2]OH溶液中加入盐酸,[Ag(NH3)2]OH属于强电解质,能够完全电离出[Ag(NH3)2]+、OH-,其与盐酸反应的离子方程式为:[Ag(NH3)2]++OH-+3H++Cl-=AgCl↓+2NH4++H2O,故C错误;
D.稀硝酸具有强氧化性,能够氧化SO32-,因此向稀硝酸中滴加Na2SO3溶液时,发生离子反应为:2NO3-+2H++3SO32-=3SO42-+2NO↑+H2O,故D错误;
故答案为:A。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】硼酸(H3BO3)是一种片层状结构白色晶体,受热易分解。层内的 H3BO3分子通过氢键相连(如图所示),则下列有关说法中正确的是

A.正硼酸晶体属于原子晶体B.H3BO3分子的稳定性与氢键有关
C.1 mol H3BO3晶体中含有3 mol氢键D.分子中硼原子最外层为8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应![]() 经2min后,B的浓度减少了0.6mol·L-1。下列说法正确的是( )
经2min后,B的浓度减少了0.6mol·L-1。下列说法正确的是( )
A.用A表示的化学反应速率是0.4mol·L-1·min-1
B.分别用B、C、D表示化学反应速率,其比是3:2:1
C.在2min末的反应速率用B表示是0.3mol·L-1·min-1
D.在这2min内B和C两物质的浓度都减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家通过测量SiO2中26Al和10Be两种元素的比例来确定“北京人”年龄,这种测量方法叫铝铍测年法。关于26Al和10Be的说法不正确的是
A.10Be和9Be是中子数不同质子数相同的不同原子
B.10Be的原子核内中子数比质子数多
C.5.2 g26Al3+中所含的电子数约为1.2×1024
D.26Al和26Mg的质子数、中子数和核外电子数都不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达700900℃时,O2可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。下列说法正确的是( )
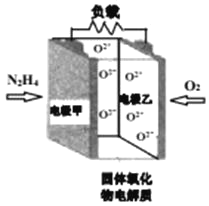
A.电池内的O2由电极乙移向电极甲
B.电池总反应为N2H4+2O2=2NO+2H2O
C.当甲电极上有lmolN2H4消耗时,乙电极上有22.4LO2参与反应
D.电池外电路的电子由电极乙移向电极甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1,下列说法正确的是( )
A.CO的燃烧热为-283 kJ·mol-1
B.CO的燃烧热为566 kJ·mol-1
C.CO的燃烧热ΔH=-283 kJ·mol-1
D.如图可表示由CO生成CO2的反应过程和能量关系
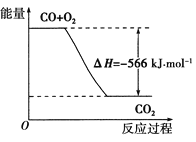
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,将乙针筒内的物质压到甲针筒内,进行下表所列实验,对实验现象的描述错误的是
(气体在同温同压下测定)
![]()
选项 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
A | 20mLH2S | 10mLSO2 | 生成黄色固体,活塞自动向内压缩 |
B | 1g薄铜片 | 10mL12mol/L浓硝酸 | 生成棕色气体、溶液呈绿色,活塞自动外移,Cu有剩余 |
C | 30mLNO2 | 10mL水(液态) | 剩有无色气体,活塞自动向内压缩 |
D | 10mLFeSO4溶液 | 10mLNH3 | 生成白色沉淀,最终沉淀转变为红褐色 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液分别滴加到两种一元弱酸HA和HB中,两种混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是
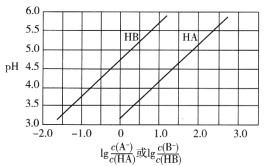
A. Ka(HA)的数量级为10-5
B. 当NaOH溶液与HB混合至中性时:c(B-)<c(HB)
C. 等浓度的NaA、NaB溶液中,水的电离程度:NaA<NaB
D. 等浓度的HB和NaA的混合溶液中:c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的有效回收利用,既能缓解能源危机,又可减少温室效应的影响,具有解决能源问题及环保问题的双重意义。Zn/ZnO热化学循环还原CO2制CO的原理如图所示,回答下列问题:
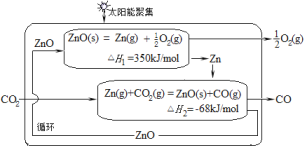
(1)①Zn/ZnO在反应中循环使用,其作用是___。
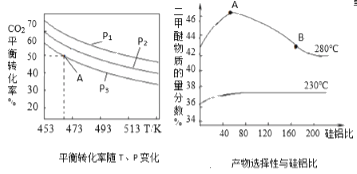
(2)二甲醚是主要的有机物中间体,在一定条件下利用CO2与H2可直接合成二甲醚:2CO2(g) +6H2(g)![]() CH3OCH3(g)+3H2O(g),
CH3OCH3(g)+3H2O(g),![]() =3时,实验测得CO2的平衡转化率随温度及压强变化如图所示。
=3时,实验测得CO2的平衡转化率随温度及压强变化如图所示。
合成二甲醚过程中往往会生成一氧化碳,合成时选用硅铝化合物做催化剂,硅铝比不同时,生成二甲醚或一氧化碳的物质的量分数不同。硅铝比与产物选择性如图所示。图中A点和B点的化学平衡常数比较:KA___KB(填“>、<、=”)。根据以上两条曲线,写出其中一条变化规律:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com