
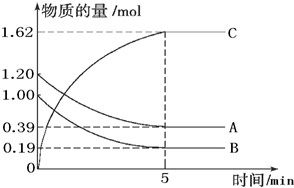
| △c |
| △T |
| 转化量 |
| 起始量 |
| △c |
| △T |
| ||
| 5min |
| 转化量 |
| 起始量 |
| (1-0.19)mol |
| 1mol |
| c18(C) |
| c9(A)×c(B) |
| c18(C) |
| c9(A)×c(B) |


科目:高中化学 来源: 题型:
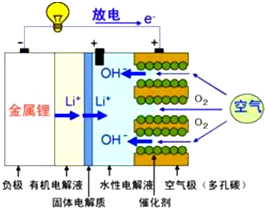 美国IBM公司设计出了一款新型锂空气电池,其原理就是通过吸入空气与设备内的锂离子发生反应,进行能量的提供.因其独特的放电方式,也称呼吸式电池.负极采用金属锂条,负极的电解液采用含有锂盐的有机电解液.中间设有用于隔开正极和负极的锂离子固体电解质.正极的水性电解液使用碱性水溶性凝胶,与由微细化碳和廉价氧化物催化剂形成的正极组合.如图所示.下列说法不正确的是( )
美国IBM公司设计出了一款新型锂空气电池,其原理就是通过吸入空气与设备内的锂离子发生反应,进行能量的提供.因其独特的放电方式,也称呼吸式电池.负极采用金属锂条,负极的电解液采用含有锂盐的有机电解液.中间设有用于隔开正极和负极的锂离子固体电解质.正极的水性电解液使用碱性水溶性凝胶,与由微细化碳和廉价氧化物催化剂形成的正极组合.如图所示.下列说法不正确的是( )| A、负极反应:Li-e-=Li+,金属锂以锂离子(Li+)的形式溶于有机电解液,电子供应给导线.溶解的锂离子(Li+)穿过固体电解质移到正极的水性电解液中 |
| B、正极反应:O2+2H2O+4e-=4OH-,在正极的水性电解液中与锂离子(Li+)结合生成水溶性氢氧化锂(LiOH),并能实现锂元素的循环 |
| C、在负极的有机电解液和空气极的水性电解液之间,用只能通过锂离子的固体电解质隔开,以防止两电解液发生混合,而且能促进电池发生反应 |
| D、锂-空气电池至今都未普及,原因是它存在致命缺陷,即固体反应生成物氧化锂(Li2O)在正极堆积,使电解液与空气的接触被阻断,从而导致放电停止 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图铅蓄电池是一种典型的可充电电池,电池总反应式为
如图铅蓄电池是一种典型的可充电电池,电池总反应式为| 放电 |
| 充电 |
| A、放电时,电流方向由B过M到A |
| B、充电时,铅蓄电池的正极应与充电器电源的负极相连 |
| C、放电时,正极反应是Pb-2e-+SO42-═PbSO4 |
| D、充电时,阳极反应是PbSO4-2e-+2H2O═PbO2+SO42-+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MgF2 |
| B、MgCl2 |
| C、CaCl2 |
| D、CaBr2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室制取乙烯的装置如图所示,请回答:
实验室制取乙烯的装置如图所示,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 实 验 用 品 | 溶 液 温 度 | 中和热 △H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol?L-1NaOH | 50mL.0.5mol?L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol?L-1NaOH | 50mL.0.5mol?L-1HCl | 20℃ | 23.5℃ | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com