
【题目】已知Ca3(PO4)2与SiO2、C高温共热可以反应得到CaSiO3、P4蒸气和CO.反应如下: Ca3(PO4)2+SiO2+C ![]() CaSiO3+P4↑+CO↑
CaSiO3+P4↑+CO↑
(1)配平该反应方程式,并标出电子转移方向和数目. Ca3(PO4)2+SiO2+C ![]() CaSiO3+P4↑+CO↑
CaSiO3+P4↑+CO↑
(2)该反应中被还原的元素是 , 氧化产物是 .
(3)每消耗24.0g碳时,有个电子发生转移,生成P4g.
(4)反应所得混合气体,折算成标况下,其气体密度为g/L(保留两位小数).与该反应中涉及到的磷元素相同主族的氮元素,是造成水体富营养化的主要原因.若某污水中NH4Cl含量为180mg/L.
(5)写出NH4Cl的电子式 .
(6)为除去废水中的NH4+ , 向103L该污水中加入0.1mol/LNaOH溶液,发生如下反应:NH4++OH﹣→NH3+H2O.则理论上需要NaOH溶液的体积为L(计算结果保留两位小数)
【答案】
(1)2;6;10;6;1;10; 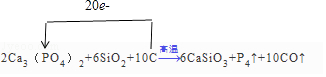
(2)p; CO
(3)4NA;24.8
(4)1.64
(5)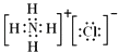
(6)33.64
【解析】解:(1)在此反应中Ca3(PO4)2中P元素价态从+5降低到0价的P4,化合价降低了20,C从0价升高到+2价的CO,化合价升高了+2价,最小公倍数为20,故P4前系数为1,CO前系数为10,并根据原子守恒配平,故方程式2Ca3(PO4)2+6SiO2+10C ![]() 6CaSiO3+P4↑+10CO↑故方程式前面的系数为:2;6;10;6;1;10;单线桥表示
6CaSiO3+P4↑+10CO↑故方程式前面的系数为:2;6;10;6;1;10;单线桥表示 
所以答案是:2;6;10;6;1;10; 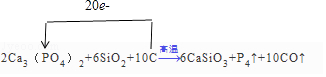
;(2)据Ca3(PO4)2中P元素的化合价由+5价降低为0,化合价降低,故作氧化剂,又因为氧化剂具有氧化性被还原,故P元素被还原;C元素由0价升高到+2价的
CO,化合价升高,做还原剂,得到的CO是氧化产物,
所以答案是:P;CO;(3)(3)每消耗24.0g碳时,转移电子为 ![]() ×(2﹣0)=4mol,N=nNA=4NA,由反应可知,消耗10molC生成1molP4,其质量为0.2mol×124g/mol=24.8g
×(2﹣0)=4mol,N=nNA=4NA,由反应可知,消耗10molC生成1molP4,其质量为0.2mol×124g/mol=24.8g
所以答案是:4NA;24.8;(4)(4)由反应可知,混合气体的质量为24.8g+2mol×28g/mol=80.8g,标况下体积为2.2mol×22.4L/mol=49.28L,所以密度为 ![]() =1.64g/L
=1.64g/L
所以答案是:1.64(5)氯化铵是离子化合物,由氨根离子与氯离子构成,电子式为: 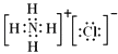 ,
,
所以答案是: 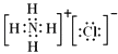 ;(6)
;(6)
由NH4Cl~~~~ | NaOH |
53.3g | 1mol |
180mg/L×103 L×103 g/mg | 0.1mol/L×V |
![]() =
= ![]() 解之得:V=33.64L
解之得:V=33.64L
所以答案是:33.64.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】在20℃时,在一刚性容器内部有一个不漏气且可滑动的活塞将容器分隔成左右两室.左室充入氮气,右室充入氢气与氧气的混合气体,活塞恰好停留在离左端的 ![]() 处(如图左所示),然后引燃氢、氧混合气体,反应完毕后恢复至原来温度,活塞恰好停在中间(如图所示),如果忽略水蒸气体积,则反应前氢气与氧气的体积比可能是( )
处(如图左所示),然后引燃氢、氧混合气体,反应完毕后恢复至原来温度,活塞恰好停在中间(如图所示),如果忽略水蒸气体积,则反应前氢气与氧气的体积比可能是( ) 
A.3:4
B.4:5
C.6:2
D.2:7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X,Y,Z是三种短周期的主族元素,在周期表的位置如图,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( ) 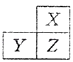
A.原子半径:Y>Z>X
B.气态氢化物的热稳定性:X<Z
C.y和z的最高价氧化物对应水化物均为强酸
D.若z的最高正价为+m,则X的最高正价也一定为+m
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是( ) 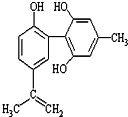
A.该物质与苯酚属于同系物,遇FeCl3溶液呈紫色
B.滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
C.该分子中的所有碳原子不可能共平面
D.1mol此物质分别与浓溴水和H2反应时最多消耗Br2和H2为4mol和7mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.NH4HCO3溶于过量的浓KOH溶液中并加热:NH4++HCO3﹣+2OH﹣=CO32﹣+NH3↑+2H2O
B.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42﹣沉淀完全:2Al3++3SO42﹣+3Ba2++6OH ﹣=2 Al(OH)3↓+3BaSO4↓
C.向FeI2溶液中通入少量氯气:2Fe2++Cl2=2Fe3++2Cl﹣
D.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3﹣═3Fe3++NO↑+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).下列物质中与该产品互为同分异构体的是( ) 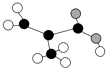
A.CH2═C(CH3)COOH
B.CH2═CHCOOCH3
C.CH3CH2CH═CHCOOH
D.CH3CH(CH3)COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将装有50mL NO2、NO混合气体的量筒倒立于水槽中,反应后气体体积缩小为30mL,则原混合气体中NO2和NO的体积比是( )
A.5:3
B.3:5
C.3:2
D.2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.5mol的Fe和一定量稀硝酸恰好完全反应生成Fe(NO3)2、Fe(NO3)3和NO,经测定其中Fe(NO3)2与Fe(NO3)3的物质的量之比为3:2,请计算:
(1)生成NO的物质的量;
(2)原稀硝酸中含HNO3的物质的量.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp(AgCl)=1.56×10﹣10 , Ksp(AgBr)=7.7×10﹣13 , Ksp(Ag2CrO4)=9.0×10﹣12 . 某溶液中含有Cl﹣、Br﹣和CrO42﹣浓度均为0.010molL﹣1 , 向该溶液中逐滴加入0.010molL﹣1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为( )
A.Cl﹣、Br﹣、CrO42﹣
B.CrO42﹣、Br﹣、Cl﹣
C.Br﹣、Cl﹣、CrO42﹣
D.Br﹣、CrO42﹣、Cl﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com