
【题目】氨在化肥生产、储氢及环境治理等领域发挥着重要作用。
(1)中科院固体研究所的赵惠军和张海民研究团队以MoS2为催化剂,通过调节催化剂/电解质的表界面相互作用,在不同电解质溶液中实现常温电催化合成氨,其反应历程与相对能量模拟计算结果如图1。将Na2SO4溶液换成Li2SO4溶液后,反应速率明显加快的主要原因是加快了下列__转化的反应速率(填标号)。
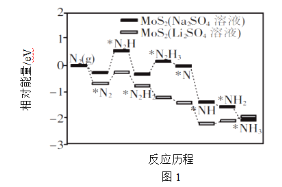
A.N2→*N2 B.*N2→*N2H C.*N2H3→*N D.*NH→*NH2
(2)2017年Dr.KatsutoshiNagaoka等带领的研究团队开发了一种可以“快速启动的氨制氢工艺”。
已知:NH3(g)=![]() H2(g)+
H2(g)+![]() N2(g) ΔH1=+45.9kJ·mol-1
N2(g) ΔH1=+45.9kJ·mol-1
NH3(g)+![]() O2(g)=
O2(g)=![]() H2O(g)+
H2O(g)+![]() N2(g) ΔH2=-318kJ·mol-1
N2(g) ΔH2=-318kJ·mol-1
则快速制氢反应NH3(g)+![]() O2(g)=H2(g)+
O2(g)=H2(g)+![]() H2O(g)+
H2O(g)+![]() N2(g)的ΔH=___kJ·mol-1。
N2(g)的ΔH=___kJ·mol-1。
(3)氨在高温下分解可以产生氢气和氮气。1100℃时,在钨丝表面NH3分解的半衰期(浓度减小一半所需时间)如下表所示:

表中的t5的值为___。c(NH3)的值从2.28×10-3变化至1.14×10-3的过程中,平均反应速率v(H2)=___ mol·L-1·s-1(保留三位有效数字)。
(4)氨催化氧化时会发生两个竞争反应:
Ⅰ:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH=-905.0kJ·mol-1
4NO(g)+6H2O(g) ΔH=-905.0kJ·mol-1
Ⅱ:4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) ΔH=-1266.6kJ·mol-1
2N2(g)+6H2O(g) ΔH=-1266.6kJ·mol-1
为分析某催化剂对反应的选择性,在1L密闭容器中存入1mol氨气和2mol的氧气,测得有关物质的物质的量随温度变化的关系如图2。
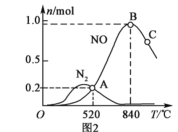
①该催化剂在低温时,选择反应___(填“Ⅰ”或“Ⅱ”)。
②520℃时,4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)的平衡常数K=___(只需列出数字计算式,无需计算结果)。
4NO(g)+6H2O(g)的平衡常数K=___(只需列出数字计算式,无需计算结果)。
(5)华南理工大学提出利用电解法制H2O2并用产生的H2O2处理废氨水,装置如图3所示。
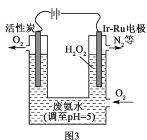
①IrRu惰性电极有吸附O2的作用,该电极上的反应为__。
②理论上电路中每转移3mol电子,最多可以处理NH3·H2O的物质的量为__。
【答案】B ﹣75.4 825 7.77×10﹣6 II ![]() O2+2e﹣+2H+=H2O2 1mol
O2+2e﹣+2H+=H2O2 1mol
【解析】
(1)化学反应速率快慢取决于慢反应的速率;
(2)①NH3(g)═![]() H2(g)+
H2(g)+![]() N2(g)△H1=+45.9kJmol﹣1,②NH3(g)+
N2(g)△H1=+45.9kJmol﹣1,②NH3(g)+![]() O2(g)═
O2(g)═![]() H2O(g)+
H2O(g)+![]() N2(g)△H2=﹣318kJmol﹣1,根据盖斯定律可知方程式①×
N2(g)△H2=﹣318kJmol﹣1,根据盖斯定律可知方程式①×![]() +②×
+②×![]() 得方程式NH3(g)+
得方程式NH3(g)+![]() O2(g)═
O2(g)═![]() H2O(g)+
H2O(g)+![]() N2(g)+H2(g)的△H进行相应改变;
N2(g)+H2(g)的△H进行相应改变;
(3)表中NH3分解的半衰期规律:440s、220s、110s、55s、27.5s、…,c(NH3)的值从2.28×10﹣3变化至1.14×10﹣3的过程中,平均反应速率(NH3)=![]() =
=![]() mol/(L·s)=5.18×10﹣6 mol/(L·s),相同时间内v(H2)=
mol/(L·s)=5.18×10﹣6 mol/(L·s),相同时间内v(H2)=![]() v(NH3);
v(NH3);
(4)①根据图象分析,在温度较低时,产生较多的是氮气;
②可逆反应:
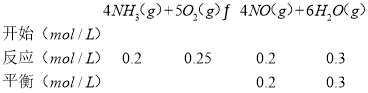
可逆反应:
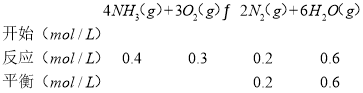
则平衡时c(NH3)=(1﹣0.2﹣0.4)mol/L=0.4mol/L、c(O2)=(2﹣0.25﹣0.3)mol/L=1.45mol/L,c(NO)=c(N2)=0.2mol/L、c(H2O)=(0.3+0.6)mol=0.9mol,反应4NH3(g)+5O2(g)4NO(g)+6H2O(g)的K=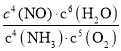 ;
;
(5)①IrRu惰性电极有吸附
②双氧水具有强氧化性,能氧化一水合氨生成氮气,则消耗1mol一水合氨转移3mol电子。
(1)化学反应速率快慢取决于慢反应的速率,能量越高反应速率越慢,根据图知,反应速率取决于*N2→*N2H,*N2→*N2H中能量变低,所以化学反应速率变化明显,故答案为:B;
(2)①NH3(g)═![]() H2(g)+
H2(g)+![]() N2(g)△H1=+45.9kJmol﹣1,②NH3(g)+
N2(g)△H1=+45.9kJmol﹣1,②NH3(g)+![]() O2(g)═
O2(g)═![]() H2O(g)+
H2O(g)+![]() N2(g)△H2=﹣318kJmol﹣1,根据盖斯定律可知方程式①×
N2(g)△H2=﹣318kJmol﹣1,根据盖斯定律可知方程式①×![]() +②×
+②×![]() 得方程式NH3(g)+
得方程式NH3(g)+![]() O2(g)═
O2(g)═![]() H2O(g)+
H2O(g)+![]() N2(g)+H2(g)的△H=(+45.9kJmol﹣1)×
N2(g)+H2(g)的△H=(+45.9kJmol﹣1)×![]() +(﹣318kJmol﹣1)×
+(﹣318kJmol﹣1)×![]() =﹣75.4kJ/mol;
=﹣75.4kJ/mol;
(3)表中NH3分解的半衰期规律:440s、220s、110s、55s、27.5s、…,所以t5=770s+55s=825s;c(NH3)的值从2.28×10﹣3变化至1.14×10﹣3的过程中,平均反应速率(NH3)=![]() =
=![]() mol/(L·s)=5.18×10﹣6 mol/(L·s),相同时间内v(H2)=
mol/(L·s)=5.18×10﹣6 mol/(L·s),相同时间内v(H2)=![]() v(NH3)=
v(NH3)=![]() ×5.18×10﹣6 mol/(L·s)=7.77×10﹣6 mol/(L·s);
×5.18×10﹣6 mol/(L·s)=7.77×10﹣6 mol/(L·s);
(4)①由图可知,该催化剂在高温时,生成的NO物质的量远大于氮气的,故该催化剂在高温下选择反应I,低温时选择反应II,故答案为:II;
②可逆反应:
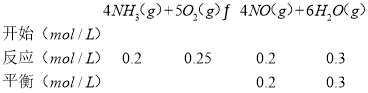
可逆反应:
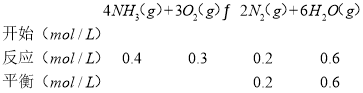
则平衡时c(NH3)=(1﹣0.2﹣0.4)mol/L=0.4mol/Lc(O2)=(2﹣0.25﹣0.3)mol/L=1.45mol/L,c(NO)=c(N2)=0.2mol/L、c(H2O)=(0.3+0.6)mol=0.9mol,此时4NH3(g)+5O2(g)4NO(g)+6H2O(g)的K=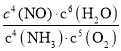 =
=![]() ;
;
(5)①IrRu惰性电极有吸附O2 的作用,该电极上氧气得电子和氢离子反应生成双氧水,电极反应式为O2+2e﹣+2H+=H2O2;
②双氧水具有强氧化性,能氧化一水合氨生成氮气,则消耗1mol一水合氨转移3mol电子,则电路中每转移3 mol 电子,最多可以处理NH3H2O 的物质的量为1mol。


科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应
X(g)+Y(g) ![]() 2Z(g) △H < 0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H < 0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A.反应前2min的平均速率ν(Z)=2.0×10-3mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前ν(逆)> ν(正)
C.该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
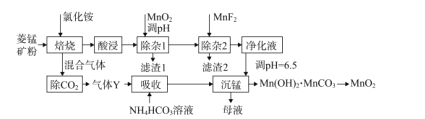
【题目】利用菱锰矿(主要成分是MnCO3,含少量A12O3、Fe2O3、FeO、CaO、MgO等)为原料制备MnO2的工艺流程如下:
已知:①25℃时,![]()
②相关金属离子![]() 形成氢氧化物沉淀pH范围如下:
形成氢氧化物沉淀pH范围如下:
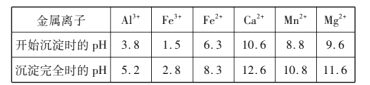
(1)“除杂1”中加入适量MnO2的作用是____,应调节溶液pH不小于____。
(2)“除杂2”的主要目的将Ca2+、Mg2+转化为相应的氟化物沉淀而除去,除去Ca2+的离子方程式为____,该反应的平衡常数为____。
(3)“沉锰”中生成Mn(OH)2'MnCO3沉淀的离子方程式为____,“母液”经加热等系列操作后可返回“____”工序循环使用。
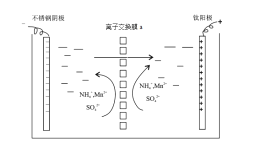
(4)以MnSO4-(NH4)2SO4为电解质溶液,利用下图装置可同时制备金属锰和MnO2。离子交换膜a为____,阳极电极反应式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是一种二元弱酸。常温下向H2C2O4溶液中滴加NaOH溶液,混合溶液里lgX[X表示![]() 或
或![]() ]随pH的变化关系如图所示。下列说法不正确的是
]随pH的变化关系如图所示。下列说法不正确的是

A. 直线I中X表示的是![]()
B. 直线I、Ⅱ的斜率均为1
C. c(HC2O4-)>c(C2O42-)>c(H2C2O4)对应1.22<pH<4.19
D. c(Na+)=c(HC2O4-)+2c(C2O42-)对应pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是

A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化铜(II)甲基咪唑配合物是一种制备有机玻璃的催化剂,其合成方法如下:
(1)铜元素位于周期表中第_____族,写出基态Cu2+的电子排布式_______。
(2)与![]() 互为等电子体的阴离子为_______。
互为等电子体的阴离子为_______。
(3)![]() 中心原子的杂化方式为_________。
中心原子的杂化方式为_________。
(4)MIm中含σ键与π数目之比为__________。
(5)一种铜的溴化物晶胞结构如图所示。
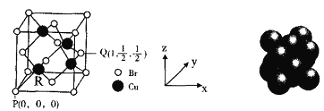
由图中P点和Q点的原子坐标参数,可确定R点的原子坐标参数为______。
(6)Cu晶体的堆积方式为面心立方最密堆积,设Cu原子半径为a,晶体中Cu原子的配位数为________,晶体的空间利用率为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置,以NH3作氢源,可实现电化学氢化反应。下列说法错误的是

A.a为阴极
B.b电极反应为:2NH3-6e-=N2+6H+
C.电解一段时间后,装置内H+数目增多
D.理论上每消耗1 mol NH3,可生成1.5mol![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中美科学家在银表面首次获得了二维结构的硼烯,该科研成果发表在顶级刊物《Science》上,并获重点推荐,二维结构的硼烯如图所示。下列说法中错误的是( )
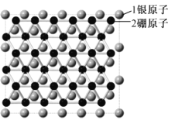
A.1.5mol硼原子核外电子数目为7.5NA
B.1个硼原子与其他原子最多只能形成3对共用电子对
C.硼的氧化物的水化物与NaOH溶液反应可生成BO2-
D.硼烯有望代替石墨烯作“硼烯-钠基”电池的负极材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钨是熔点最高的金属,是重要的战略物资。自然界中钨主要存在于黑钨矿中,其主要成分是铁和锰的钨酸盐(FeWO4、MnWO4),还含有少量Si、As的化合物。由黑钨矿冶炼钨的工艺流程如下:
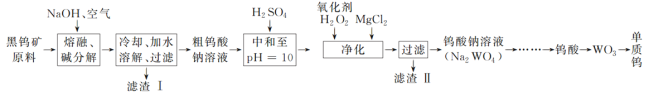
已知:①滤渣Ⅰ的主要成分是Fe2O3、MnO2;②上述流程中,钨的化合价只有在最后一步发生改变;③常温下钨酸溶于水。
(1)钨酸盐(FeWO4、MnWO4)中钨元素的化合价为______,请写出FeWO4在熔融条件下发生碱分解生成Fe2O3的化学方程式:_____________。
(2)上述流程中向粗钨酸钠溶液中加硫酸中和至pH=10后,溶液中的杂质阴离子含有SiO32—、HAsO32—、HAsO42—等,则“净化”过程中,加入H2O2时发生反应的离子方程式为HAsO32—+H2O2===HAsO42—+H2O,滤渣Ⅱ的主要成分是________。
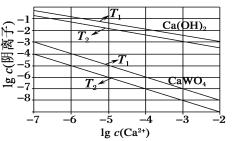
(3)已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度的升高而减小。如图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线。则:
①T1_____T2(填“>”或“<”);T1℃时Ksp(CaWO4)=______。
②向钨酸钠溶液中加入石灰乳会得到大量钨酸钙,发生反应的离子方程式为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com