
(11分)某化学兴趣小组用如图所示装置电解CuSO4溶液,测定铜的相对原子质量。
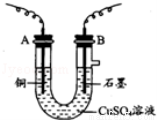
(1)若实验中测定在标准状况下放出的氧气的体积VL,B连接直流电源的_________(填“正极”或“负极”);
(2)电解开始一段时间后,在U形管中可观察到的现象有__________________,电解的离子方程式为___________________________________。
(3)实验中还需测定的数据是_______________(填写序号)
①B极的质量增重m g
②A极的质量增重m g
(4)下列实验操作中必要的是________(填字母)
A.称量电解前电极的质量
B.电解后,取出电极直接烘干称重
C.刮下电解过程中电极上析出的铜,并清洗、称重
D.在有空气存在的情况下,烘干电极必须采用低温烘干的方法
(5)铜的相对原子质量为:___________(用含有m、V的计算式表示)
(6)如果用碱性(KOH为电解质)甲醇燃料电池作为电源进行实验,放电时负极电极反应式为___________。
(11分,除标注外每空2分)
(1)正极 ;
(2)铜电极上有红色固体析出,石墨电极上有无色气体产生,溶液蓝色变浅;2Cu2++2H2O 2Cu+O2↑+4H+;
2Cu+O2↑+4H+;
(3)② ;(4)AD ;(5) ;(6)CH3OH﹣6e﹣+8OH﹣=CO32﹣+6H2O
;(6)CH3OH﹣6e﹣+8OH﹣=CO32﹣+6H2O
【解析】
试题分析:(1)铜作电极是活性电极,在溶液中OH-放电生成氧气,说明铜作阴极,与电源的负极相连,所以B连接直流电源的正极。
(2)惰性电极电解硫酸铜溶液,阴极:2Cu2++4e-=2Cu,阳极:4OH--4e-=2H2O+O2↑,所以电解开始一段时间后,在U形管中可观察到的现象有铜电极上有红色固体析出,石墨电极上有无色气体产生,溶液蓝色变浅;阴极阳极电极反应相加即得电解的总反应,电解的离子方程式为2Cu2++2H2O 2Cu+O2↑+4H+;
2Cu+O2↑+4H+;
(3)该实验测定铜的相对原子质量,需要知道铜的质量,铜在A极析出,所以选②
(4)该实验需测定析出铜的质量,阴极析出铜,而阴极用铜作电极,只需要测定反应前后阴极的质量差,在有空气存在的条件下,2Cu+O2  2CuO,所以在有空气存在的情况下,烘干电极必须采用低温烘干的方法,选AD。
2CuO,所以在有空气存在的情况下,烘干电极必须采用低温烘干的方法,选AD。
(5)根据2Cu2++2H2O 2Cu+O2↑+4H+
2Cu+O2↑+4H+
2M 22.4
m V 列方程解得M= ;
;
(6)用KOH溶液作电解液的甲醇燃料电池,甲醇在负极是电子生成CO2 ,CO2与KOH溶液反应生成碳酸钾,所以负极电极反应为CH3OH﹣6e﹣+8OH﹣=CO32﹣+6H2O。
考点:考查电解的工作原理。


科目:高中化学 来源:2014-2015山东省聊城市茌平等三县高二上学期期末联考化学试卷(解析版) 题型:选择题
反应 在四种不同情况下的反应速率分别为
在四种不同情况下的反应速率分别为 
 该反应进行的快慢顺序为
该反应进行的快慢顺序为
A.④>③=②>① B.④<③=②<①
C.①>②>③>④ D.④>③>②>①
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省德州市高二2月期末统考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.明矾水解形成的Al(0H)3胶体能杀菌消毒,可用于水的净化
B.镀锡的铁制品比镀锌的铁制品耐用
C.乙醇和乙酸都能溶于水,都是电解质
D.分别与等物质的量的HC1和CH3COOH恰好中和时,消耗NaOH的物质的量相同
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高一上学期期末化学试卷(解析版) 题型:选择题
下列有关实验操作、现象和解释或结论都正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 过量的Fe粉中加入HNO3 ,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀 |
B | CO2通入BaCl2溶液中 | 有白色沉淀出现 | 生成了BaCO3沉淀 |
C | Al箔插入稀 | 无现象 | Al箔表面被 |
D | 用玻璃棒蘸取浓硝酸点到蓝色石蕊试纸上 | 试纸先变红色后褪色 | 浓硝酸有酸性和氧化性 |
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高一上学期期末化学试卷(解析版) 题型:选择题
在25℃、1×105Pa时,等质量的H2、Cl2、CO2、C2H2四种气体中
A.H2分子数最大 B.C2H2原子数最大
C.CO2密度最大 D.Cl2分子间平均距离最大
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高二上学期期末化学试卷(解析版) 题型:选择题
下列有关电解质溶液的叙述正确的是
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7
B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大
C.含1 mol KOH的溶液与1 mol CO2完全反应后,溶液中c(K+)=c(HCO3-)
D.在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高二上学期期末化学试卷(解析版) 题型:选择题
常温下,0.2 mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是

A.HA为强酸
B.图中X表示HA,Y表示OH-,Z表示H+
C.该混合液pH=7
D.该混合溶液中:c(A-)+c(HA)=c (Na+)
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列有关化学键与晶体说法中,不正确的是
A.离子晶体的晶格能越大,离子晶体的密度就越大
B.共价键的键能越大,分子晶体的熔、沸点越高
C.成键原子的原子轨道重叠越多,共价键越牢固
D.共用电子对不发生偏移的化学键是非极性共价键
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省大冶市高三上学期期末联考理综化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,常温下,抽去下图所示装置中的玻璃片,使两种气体充分反应。下列说法正确的是
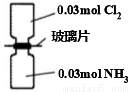
A.反应前气体的总体积为1.344L
B.装置中产生大量的白色烟雾
C.反应前后分子总数不变,均为0.06 NA个
D.生成物充分溶于水后所得溶液含有0.01 NA个NH4+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com