
ЁОЬтФПЁПЕЊЛЏХ№(BN)ОЇЬхгаЖржжНсЙЙЁЃЛиД№ЯТСаЮЪЬтЃК
(1)СљЗНЕЊЛЏХ№ЕФНсЙЙгыЪЏФЋЯрЫЦ(ШчЭМЫљЪО)ЃЌОпгаВузДНсЙЙЃЌПЩзїИпЮТШѓЛЌМСЃЌЕЋВЛЕМЕчЁЃИУОЇЬхжаДцдкЕФзїгУСІРраЭга___________ЃЌСљЗНЕЊЛЏХ№ОЇЬхВуФквЛИіХ№дзггыЯрСкЕЊдзгЙЙГЩЕФПеМфЙЙаЭЮЊ______________ЃЌСљЗНЕЊЛЏХ№ВЛЕМЕчЕФдвђЪЧ__________ЁЃ

![]()
(2)СљЗНЕЊЛЏХ№дкИпЮТИпбЙЯТЃЌПЩвдзЊЛЏЮЊСЂЗНЕЊЛЏХ№(ШчЭМЫљЪО)ЃЌИУОЇАћБпГЄЮЊa pmЃЌcдзгЕФзјБъВЮЪ§ЮЊ(0ЃЌ0ЃЌ0)ЃЌeЮЊ(![]() ЃЌ
ЃЌ![]() ЃЌ0)ЃЌfЮЊ(
ЃЌ0)ЃЌfЮЊ(![]() ЃЌ0ЃЌ
ЃЌ0ЃЌ![]() )ЁЃ
)ЁЃ
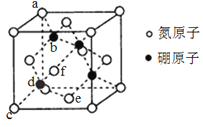
ЂйгЩЬтИЩЫљИјЕФзјБъВЮЪ§жЊЃЌdдзгЕФзјБъВЮЪ§ЮЊ_________ЁЃ
ЂкBдзгЬюГфдкNдзгЕФЫФУцЬхПеЯЖЃЌЧвеМОнДЫРрПеЯЖЕФБШР§ЮЊ_________ЁЃ
ЂлaЮЛжУNдзггыbЮЛжУBдзгЕФОрРыЮЊ________pmЁЃ
ЁОД№АИЁПЙВМлМќЁЂЗжзгМфзїгУСІ ЦНУцШ§НЧаЮ ИУОЇЬхжаУЛгаздгЩвЦЖЏЕФЮДГЩМќЕЅЕчзгЃЌвђДЫВЛЕМЕч (![]() ЃЌ
ЃЌ![]() ЃЌ
ЃЌ![]() ) 50%
) 50% ![]()
ЁОНтЮіЁП
(1)BКЭNЖМЪЧЗЧН№ЪєдЊЫиЃЌвдЙВМлМќНсКЯЃЌВуКЭВужЎМфДцдкЗжзгМфзїгУСІЃЌгЩЭМПЩжЊЃЌвЛИіBдзггы3ИіNдзгЯрСЌЃЌBдзгЙТЖдЕчзгЖдЪ§=![]() =0ЃЌ
=0ЃЌ![]() МќЕчзгЖдЪ§=
МќЕчзгЖдЪ§=![]() =3ЃЌМлВуЕчзгЖдЪ§=3+0=3ЃЌBдзгвдsp2дгЛЏЃЌЧвУЛгаЙТЖдЕчзгЃЌЫљвдЙЙаЭЮЊЦНУцШ§НЧаЮЃЌИУОЇЬхжаУЛгаздгЩвЦЖЏЕФЮДГЩМќЕЅЕчзгЃЌЫљвдВЛЕМЕчЃЌЙЪД№АИЮЊЃКЙВМлМќЁЂЗжзгМфзїгУСІЃЛЦНУцШ§НЧаЮЃЛИУОЇЬхжаУЛгаздгЩвЦЖЏЕФЮДГЩМќЕЅЕчзгЃЌвђДЫВЛЕМЕчЃЛ
=3ЃЌМлВуЕчзгЖдЪ§=3+0=3ЃЌBдзгвдsp2дгЛЏЃЌЧвУЛгаЙТЖдЕчзгЃЌЫљвдЙЙаЭЮЊЦНУцШ§НЧаЮЃЌИУОЇЬхжаУЛгаздгЩвЦЖЏЕФЮДГЩМќЕЅЕчзгЃЌЫљвдВЛЕМЕчЃЌЙЪД№АИЮЊЃКЙВМлМќЁЂЗжзгМфзїгУСІЃЛЦНУцШ§НЧаЮЃЛИУОЇЬхжаУЛгаздгЩвЦЖЏЕФЮДГЩМќЕЅЕчзгЃЌвђДЫВЛЕМЕчЃЛ
(2) ЂйcДІNЕФдзгзјБъВЮЪ§ЮЊ(0,0,0)ЃЌОрРыИУNдзгзюНќЕФdдзгСЌЯпДІгкОЇАћЬхЖдНЧЯпЩЯЃЌЧвЖўепОрРыЮЊЬхЖдНЧЯпЕФ![]() ЃЌдђИУNдзгЕНИїзјБъЦНУцОрРыОљЕШгкОЇАћРтГЄЕФ
ЃЌдђИУNдзгЕНИїзјБъЦНУцОрРыОљЕШгкОЇАћРтГЄЕФ![]() ЃЌЫљвдdдзгЕФзјБъВЮЪ§ЮЊ(
ЃЌЫљвдdдзгЕФзјБъВЮЪ§ЮЊ(![]() ЃЌ
ЃЌ![]() ЃЌ
ЃЌ![]() )ЃЌЙЪД№АИЮЊЃК(
)ЃЌЙЪД№АИЮЊЃК(![]() ЃЌ
ЃЌ![]() ЃЌ
ЃЌ![]() )ЃЛ
)ЃЛ
ЂкBдзгжмЮЇ4ИіNдзгаЮГЩе§ЫФУцЬхНсЙЙЃЌУПИіОЇАћжага8ИіетбљЕФе§ЫФУцЬхНсЙЙЃЌжЛга4ИіЬюГфСЫBдзгЃЌЫљвдBдзгеМОнДЫРрПеЯЖЕФБШР§ЮЊ50%ЃЌЙЪД№АИЮЊЃК50%ЃЛ
ЂлaЕНbЮЛжУЕФОрРы=cЕНdЕФОрРыЃЌcЕНdЕФСЌЯпДІгкОЇАћЬхЖдНЧЯпЩЯЃЌЧвИУОрРыЮЊЬхЖдНЧЯпЕФ![]() ЃЌЖјОЇАћЕФЬхЖдНЧЯп=
ЃЌЖјОЇАћЕФЬхЖдНЧЯп=![]() =
=![]() ЃЌЫљвдaЕНbЮЛжУЕФОрРы=cЕНdЕФОрРы=
ЃЌЫљвдaЕНbЮЛжУЕФОрРы=cЕНdЕФОрРы=![]() ЃЌЙЪД№АИЮЊЃК
ЃЌЙЪД№АИЮЊЃК![]() ЁЃ
ЁЃ


 ЯАЬтОЋбЁЯЕСаД№АИ
ЯАЬтОЋбЁЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛжжРызгОЇЬхЕФОЇАћШчЭМЫљЪОЁЃЦфжабєРызгAвд![]() БэЪОЃЌвѕРызгBвд
БэЪОЃЌвѕРызгBвд![]() БэЪОЁЃЙигкИУРызгОЇЬхЕФЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ)
БэЪОЁЃЙигкИУРызгОЇЬхЕФЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ)
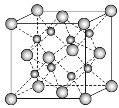
A. бєРызгЕФХфЮЛЪ§ЮЊ8ЃЌЛЏбЇЪНЮЊAB
B. вѕРызгЕФХфЮЛЪ§ЮЊ4ЃЌЛЏбЇЪНЮЊA2B
C. УПИіОЇАћжаКЌ4ИіA
D. УПИіAжмЮЇга4ИігыЫќЕШОрЧвзюНќЕФA
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаУшЪіжае§ШЗЕФЪЧ( )
A. ЕЊдзгЕФМлЕчзгХХВМЭМЃК![]()
B. 2pКЭ3pЙьЕРаЮзДОљЮЊбЦСхаЮЃЌФмСПвВЯрЕШ
C. МлЕчзгХХВМЮЊ4s24p3ЕФдЊЫиЮЛгкЕкЫФжмЦкЕкЂѕAзхЃЌЪЧpЧјдЊЫи
D. ФЦдзггЩ1s22s22p63s1Ёњ1s22s22p63p1ЪБЃЌдзгЪЭЗХФмСПЃЌгЩЛљЬЌзЊЛЏГЩМЄЗЂЬЌ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПHЁЂCЁЂNЁЂOЁЂV(ЗА)ЮхжждЊЫиаЮГЩЕФФГЗжзгНсЙЙШчЭМЫљЪОЃЌЯТСаЫЕЗЈДэЮѓЪЧ
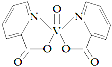
A.NдзгКЫЭтДцдк3жжВЛЭЌФмСПЕФЕчзг
B.ЛљЬЌVдзгЕФМлЕчзгЙьЕРБэЪОЪНЮЊ![]()
C.ЛљЬЌOдзгЃЌЕчзгеМОнЕФзюИпФмМЖЗћКХЮЊ2p
D.ЛљЬЌCЁЂNСНжждзгжаЃЌКЫЭтДцдкЯрЭЌЖдЪ§зда§ЗНЯђЯрЗДЕФЕчзг
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈОље§ШЗЕФзщКЯЮЊ
ЂйsЃs ІвМќгыsЃp ІвМќЕФЕчзгдЦаЮзДЯрЭЌ
ЂкЕкЫФжмЦкЕФдЊЫиЛљЬЌдзгжаЃЌ4sФмМЖжЛга1ИіЕчзгЕФдЊЫиЙВга3жж
ЂлЮйЕФХфКЯЮяРызг[W(CO)5OH]ЃФмДпЛЏЙЬЖЈCO2ЃЌИУХфРызгжаЮйЯд0Мл
ЂмжааФдзгВЩШЁsp3дгЛЏЕФЗжзгЃЌЦфСЂЬхЙЙаЭвЛЖЈЪЧе§ЫФУцЬх
Ђн2ЃЖЁДМжаДцдкЪжадЬМдзг
ЂоЯрЖдЗжзгжЪСПЃКCH3CH2OHЃОCH3CHOЃЌЫљвдЗаЕуЃКCH3CH2OHЃОCH3CHO
A.ЂкЂлЂнB.ЂлЂнC.ЂйЂкЂмD.ЂмЂо
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЗДгІЕФРызгЗНГЬЪНВЛе§ШЗЕФЪЧ( )
A.NaOHШмвКИЏЪДВЃСЇЦПШћЃКSiO2 +2OHЃ=SiO32- + 2H2O
B.ЪЕбщЪвжЦCl2ЃКMnO2ЃЋ4HCl(ХЈ) ![]() Mn2+ЃЋ2ClЃЃЋ2H2OЃЋCl2Ёќ
Mn2+ЃЋ2ClЃЃЋ2H2OЃЋCl2Ёќ
C.ЯђMg(OH) 2аќзЧвКжаМгШыFeCl3ШмвКЃК2Fe3ЃЋЃЋ3Mg(OH)2 ==2 Fe(OH)3ЃЋ3Mg2+
D.ЯђBa(OH)2ШмвКжаМгШыЩйСПNaHSO3ШмвКЃК HSO3Ѓ+Ba2ЃЋ+OHЃ=BaSO3Ё§+H2O
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПюЦБЕЭбѕЪЧвЛжжаТаЭНкФмИпЮТГЌЕМЬхЃЌЦфОЇАћНсЙЙШчЭМЫљЪОЁЃбаОПЗЂЯжЃЌДЫИпЮТГЌЕМЬхжаЕФCuдЊЫигаСНжжМлЬЌЃЌЗжБ№ЮЊ+2КЭ+3ЃЌYдЊЫиЕФЛЏКЯМлЮЊ+3ЃЌBaдЊЫиЕФЛЏКЯМлЮЊ+2ЁЃ

(1)ИУЮяжЪЕФЛЏбЇЪНЮЊ________ЁЃ
(2)ИУЮяжЪжаCu2+гыCu3+ЕФИіЪ§БШЮЊ__________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПДЋЭГжаВнвЉН№вјЛЈЖджЮСЦЁАаТЙкЗЮбзЁБгааЇЃЌЦфгааЇГЩЗжЁАТЬдЫсЁБЕФвЛжжШЫЙЄКЯГЩТЗЯпШчЯТЃК
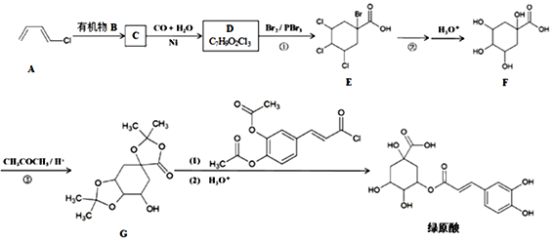
вбжЊЃКi. ![]()
ii. ![]()
ЛиД№ЯТСаЮЪЬтЃК
(1)гаЛњЮяBЕФУћГЦЪЧ__________ЁЃ
(2)CЁњDЗДгІЩњГЩЕФЙйФмЭХЪЧ__________ЁЃ
(3)ЗДгІЂйЕФЗДгІРраЭЪЧ__________ЁЃ
(4)ЗДгІЂкЕФЛЏбЇЗНГЬЪНЪЧ__________ЁЃ
(5)ЗДгІЂлЕФФПЕФЪЧ__________ЁЃ
(6)GЁњТЬдЫсЗДгІжаЃЌШєЫЎНтЪБМфЙ§ГЄЛсНЕЕЭТЬдЫсВњТЪЃЌЩњГЩИБВњЮяFКЭ(аДНсЙЙМђЪН)_______________ЁЃ
(7)ВЮееЩЯЪіКЯГЩЗНЗЈЃЌЩшМЦШ§ВНЗДгІЭъГЩвдБћЫсЮЊдСЯжЦБИИпЮќЫЎадЪїжЌОлБћЯЉЫсФЦ (ЮоЛњЪдМСШЮбЁ) ЃЌаДГіКЯГЩТЗЯп__________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЧтбѕЛЏяЎЃЈLiOHЃЉЪЧживЊЕФГѕМгTяЎВњЦЗжЎвЛЃЌПЩгУгкМЬајЩњВњЗњЛЏяЎЁЂУЬЫсяЎЕШЃЌгУЬьШЛяЎЛдЪЏЃЈжївЊГЩЗжLiAISi2O3ЃЌКЌгаFe ЃЈIIIЃЉЕШдгжЪЃЉЩњВњLiOHЕФвЛжжЙЄвеСїГЬШчЭМЫљЪОЃК

вбжЊШмвК1жаКЌгаLi+ЁЂK+ЁЂA13+ЁЂNa+ЁЂFe3+ЁЂSO42-ЕШРызгЃЌЧыЛиД№ЯрЙиЮЪЬтЁЃ
ЃЈlЃЉНЋLiAlSi2O6ИФаДЮЊбѕЛЏЮяЕФаЮЪНЃК____ЁЃ
ЃЈ2ЃЉИпЮТЩеНсЕФФПЕФЪЧ____ЁЃВйзї1ЪЧ __ ЁЃ
ЃЈ3ЃЉОЛЛЏЙ§ТЫЙ§ГЬжаШмвКЕФpHВЛФмЙ§ЕЭвВВЛФмЙ§ИпЃЌдвђЪЧ____ЁЃ
ЃЈ4ЃЉСїГЬжаЕФФГжжЮяжЪПЩбЛЗРћгУЃЌИУЮяжЪЕФЛЏбЇЪНЪЧ____ЁЃ
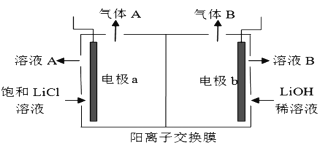
ЃЈ5ЃЉЙЄвЕЩњВњжаЭЈЙ§ЕчНтLiCIШмвКЕФЗНЗЈвВПЩжЦЕУLiOHЃЌЦфдРэШчЭМЫљЪОЃЌЕчМЋaгІСЌНгЕчдДЕФ____ЃЈбЁЬюЁАе§МЋЁБЛђЁАИКМЋЁБЃЉЃЌЕчМЋbЗЂЩњЕФЗДгІЪЧ ___ЃЌбєРызгНЛЛЛФЄЕФзїгУЪЧ___
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com