
某无色溶液X,由K+、NH4+、Ba2+、Al3+、Fe3+、CO32—、SO42—
中的若干种离子组成,取该溶液进行如下实验:
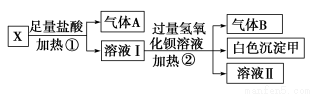
(1)白色沉淀甲是________。
(2)试写出实验过程中生成气体A、B的离子方程式
__________________________、_______________________________
(3)通过上述实验,可确定X溶液中一定存在的离子是
________,尚未确定是否存在的离子是________。
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练3-4练习卷(解析版) 题型:选择题
已知常温下D、E、F、H、L、N均为气体;A的焰色反应呈黄色;向B的溶液中滴加KSCN溶液,无明显现象;1 mol B隔绝空气分解得到F、G、H三种氧化物,其物质的量均为1 mol;F是易与血红蛋白结合的物质;J是现代社会中应用最广泛的金属单质。
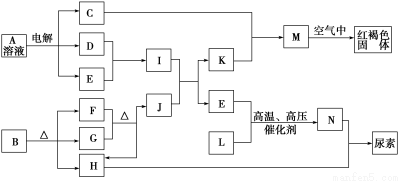
请回答下列题:
(1)B的化学式为________;H的结构式为________
(2)电解A溶液的离子方程式为______________________________________
(3)D与E反应可制得一种重要的化工原料,其反应的现象是____________________________
(4)F与G反应的化学方程式为________________________________
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练3-1练习卷(解析版) 题型:填空题
向100 mL NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M。通入二氧化碳的体积V(标准状况下)与M的质量W的关系如图
所示。请回答下列问题:

(1)b点时M的组成成分为______________________。
(2)若要使b点生成的盐的质量变为8.4 g,则应继续向溶液中通入二氧化碳________L(标准状况下)。
(3)若向生成的7.16 g盐的溶液中加入一定量的某物质,充分反应后,减压低温蒸发得到纯净的碳酸钠固体(无结晶水)8.4 g。
①若只加入0.03 mol某物质,则加入的物质可以是________或________;
②若只加入0.06 mol某物质,则加入的物质可以是________、________或________。
(4)常温下,同浓度的碳酸钠溶液和碳酸氢钠溶液的pH
都大于7,二者中________的pH更大,理由是________________________;0.1 mol·L-1碳酸钠溶液中离子浓度的大小关系是________;向碳酸氢钠溶液中逐滴滴入氢氧化钡溶液,发生反应的离子方程式为________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-3练习卷(解析版) 题型:填空题
氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)水是人体的重要组成成分,是人体中含量最多的一种物质。而“四种基本反应类型
与氧化还原反应的关系”也可用如图表达。
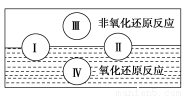
试写出有水参加的符合反应类型Ⅳ的一个化学方程式:________________________,其中水为________剂。
(2)氯化铵常用作焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:
CuO+____NH4Cl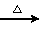 Cu+____CuCl2+N2↑+____H2O。
Cu+____CuCl2+N2↑+____H2O。
①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是________(填元素名称),氧化剂是________(填化学式)。
(3)(2011·福建高考卷节选)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2=6CaSiO3+P4O10,10C+P4O10=P4+10CO。
每生成1 mol P4时,就有________mol电子发生转移。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-3练习卷(解析版) 题型:选择题
铬是人体必需的微量元素,但铬过量会引起污染,危害人体健康。不同
价态的铬毒性不一样,六价铬的毒性最大。下列叙述错误的是( )
A.K2Cr2O7可以氧化乙醇,可用来鉴别司机是否酒后驾驶
B.污水中铬一般以Cr3+存在,与水中的溶解氧作用可被还原为六价铬
C.人体内六价铬超标,服用维生素C缓解毒性,说明维生素C具有还原性
D.1 mol Cr2O72—得到6 mol电子时,还原产物是Cr3+
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-2练习卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是( )
A.将Al条投入NaOH溶液中:Al+OH-+H2O=AlO2—+H2↑
B.铜溶于稀硝酸中:Cu+4H++2NO3—=Cu2++2NO2↑+2H2O
C.碳酸氢钙溶液中加入过量的氢氧化钠溶液:HCO3—+OH-=CO32—+H2O
D.向碳酸钠溶液中逐滴加入与之等体积等物质的量浓度的稀醋酸:CO32—+CH3COOH=CH3COO-+HCO3—
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-2练习卷(解析版) 题型:选择题
下列固体混合物与过量的稀H2SO4反应,能产生气泡并有沉淀生成的
是( )
A.NaHCO3和Al(OH)3 B.BaCl2和NaCl
C.KClO3和K2SO4 D.Na2SO3和BaCO3
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-3练习卷(解析版) 题型:填空题
近几年地球发生地震灾害较多,抢救地震后被困在废墟下的伤员,首要的措施是给伤员补充能量。下图是医院给伤员输液时用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液标签,请认真观察标签上所列的内容后填写:

(1)葡萄糖的摩尔质量为________;
(2)该溶液中含水________g;
(3)该溶液的密度约为________g/mL;
(4)该溶液的物质的量浓度为________mol/L(精确到小数点后面两位)。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习2-3-2氧化还原反应方程式配平及计算练习卷(解析版) 题型:填空题
在热的稀硫酸中溶解了11.4 g FeSO4固体,当加入50 mL 0.5 mol·L-1 KNO3溶液时,其中的Fe2+全部转化成Fe3+,KNO3也完全反应并放出NxOy气体。
(1)推算出x= ;y= 。
(2)配平该反应的方程式:
FeSO4+ KNO3+ H2SO4= K2SO4+ Fe2(SO4)3+  (NxOy)+ H2O(配平时x、y用具体数值表示,物质填在
(NxOy)+ H2O(配平时x、y用具体数值表示,物质填在 中)。
中)。
(3)反应中氧化产物是 。
(4)用双线桥法表示该反应中的电子转移方向和数目: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com