
氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)水是人体的重要组成成分,是人体中含量最多的一种物质。而“四种基本反应类型
与氧化还原反应的关系”也可用如图表达。
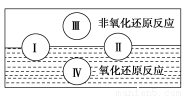
试写出有水参加的符合反应类型Ⅳ的一个化学方程式:________________________,其中水为________剂。
(2)氯化铵常用作焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:
CuO+____NH4Cl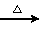 Cu+____CuCl2+N2↑+____H2O。
Cu+____CuCl2+N2↑+____H2O。
①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是________(填元素名称),氧化剂是________(填化学式)。
(3)(2011·福建高考卷节选)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2=6CaSiO3+P4O10,10C+P4O10=P4+10CO。
每生成1 mol P4时,就有________mol电子发生转移。
(1)C+H2O(g)  CO+H2(合理即可) 氧化
CO+H2(合理即可) 氧化
(2)①4CuO+2NH4Cl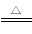 3Cu+CuCl2+N2↑+4H2O
3Cu+CuCl2+N2↑+4H2O
②氮 CuO (3)20
【解析】(1)由图可知,反应类型Ⅳ全部属于氧化还原反应,应该是置换反应,有水参加的置换反应有许多,如C+H2O(g)  CO+H2、2Na+2H2O=2NaOH+H2↑等上述两个反应中水均作氧化剂。
CO+H2、2Na+2H2O=2NaOH+H2↑等上述两个反应中水均作氧化剂。
(2)①用化合价升降法配平化学方程式为4CuO+2NH4Cl 3Cu+CuCl2+N2↑+4H2O。
3Cu+CuCl2+N2↑+4H2O。
②在该反应中,氮元素化合价升高,被氧化,NH4Cl为还原剂,铜元素化合价降低,被还原,CuO为氧化剂。
(3)反应过程中磷酸钙最终变成了白磷,磷的化合价由+5价变成0价,由此可以得到如下关系式:
2Ca3(PO4)2~P4~20e-,所以每生成1 mol P4,转移20 mol电子。


科目:高中化学 来源:2014年高考化学一轮复习课后规范训练4-1练习卷(解析版) 题型:填空题
在下列物质的转化关系中,A是一种固体单质,且常作半导体材料,E是一种白色沉淀,F是最轻的气体单质。
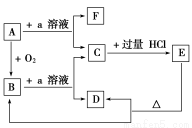
据此填写:(1)B的化学式是 ,目前在现代通讯方面B已被用作 的主要原料。
(2)B和a溶液反应的离子方程式是 。
(3)A和a溶液反应的离子方程式是 。
(4)C和过量盐酸反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练3-2练习卷(解析版) 题型:填空题
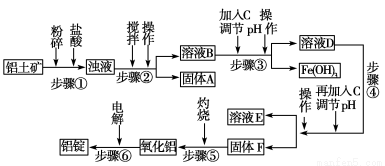
日常生活中使用的铝合金中的铝来自于电解氧化铝。工业上电解氧化铝要求其纯度不得低于98.2%,而天然铝土矿的氧化铝含量为50%~70%,杂质主要为SiO2、Fe2O3、CaO、MgO、Na2O等。工业生产铝锭的工艺流程示意图如下。
一些氢氧化物沉淀的pH如下表。
沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 |
开始沉淀pH(离子初始浓度0.01 mol/L) | 4 | 2.3 | 10.4 |
完全沉淀pH(离子浓度<10-5mol/L) | 5.2 | 4.1 | 12.4 |
请回答下列问题。
(1)实验室进行步骤④的操作名称为________。
(2)固体A的化学式为________,物质C的化学式为________。
(3)步骤④调节pH的范围为________。
(4)步骤⑥反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练3-1练习卷(解析版) 题型:选择题
把2.1 g CO与H2组成的混合气体与足量的O2充分燃烧后,立即通入足
量的Na2O2固体中,固体的质量增加( )
A.2.1 g B.3.6 g
C.7.2 g D.无法确定
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练3-1练习卷(解析版) 题型:选择题
下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液中 ②过量NaOH溶液和明矾溶液混合 ③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中
A.只有①④ B.只有③C.只有②③ D.只有①③④
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-3练习卷(解析版) 题型:选择题
有下列三个反应:
①Cl2+FeI2=FeCl2+I2
②2Fe2++Br2=2Fe3++2Br-
③Co2O3+6HCl=2CoCl2+Cl2↑+3H2O
下列说法正确的是( )
A.反应①②③中的氧化产物分别是I2、Fe3+、CoCl2
B.根据以上方程式可以得到氧化性:Cl2>Fe3+>Co2O3
C.在反应③中当1 mol Co2O3参加反应时,2 mol HCl被氧化
D.可以推理得到Cl2+FeBr2=FeCl3+Br2
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-2练习卷(解析版) 题型:填空题
某无色溶液X,由K+、NH4+、Ba2+、Al3+、Fe3+、CO32—、SO42—
中的若干种离子组成,取该溶液进行如下实验:
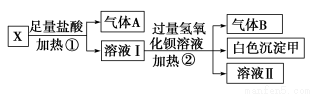
(1)白色沉淀甲是________。
(2)试写出实验过程中生成气体A、B的离子方程式
__________________________、_______________________________
(3)通过上述实验,可确定X溶液中一定存在的离子是
________,尚未确定是否存在的离子是________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-1练习卷(解析版) 题型:选择题
下表各组物质中,满足如图物质一步转化关系的选项是( )
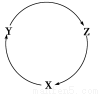
选项XYZ
ANaNaOHNaHCO3
BCuCuSO4Cu(OH)2
CCCOCO2
DSiSiO2H2SiO3
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-1练习卷(解析版) 题型:填空题
某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO2—、MnO4—、CO32—、SO42—、SiO32—中的若
干种组成(不考虑水的电离)。取该溶液进行如下实验:
Ⅰ.取适量溶液,加入过量的盐酸,有气体生成,并得到无色溶液;
Ⅱ.在Ⅰ所得溶液中加入过量的NH4HCO3溶液,有气体生成,同时析出白色沉淀甲;
Ⅲ.在Ⅱ所得溶液中加入过量的Ba(OH)2溶液,加热,也有气体生成,同时析出白色沉淀乙。
请回答下列问题:
(1)由实验Ⅰ可知原溶液中一定不含有的离子是________;一定含有的离子是________________。
(2)由实验Ⅱ可知原溶液中还一定含有的离子是________;生成甲的离子方程式为________________。
(3)实验Ⅲ中生成白色沉淀乙的离子方程式为________________。
(4)原溶液中还可能存在的离子是________;检验该离子的方法是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com