
| A. | 8.48 g | B. | 7.48 g | C. | 5.72 g | D. | 5.22g |
分析 盐与气体的质量相比,生成正盐比生成酸式盐质量增重多,
若生成正盐,假设全为Na2CO3,生成的盐的质量最重,NaOH可能有剩余,故最大值可能大于盐的极大值;
若生成酸式盐,假设全是NaHSO3,生成的盐的质量最小,由于混有CO2,故固体的质量大于该值,据此计算判断.
解答 解:若生成正盐,则生成的盐的质量最重,假设全为Na2CO3,生成的盐的质量最重,盐的最大质量为$\frac{3.52g}{44g/mol}$×106g/mol=8.48g,NaOH可能有剩余,故固体的最大值可能大于盐的极大值8.48g;
若生成酸式盐,盐的质量最小,假设全是NaHSO3,生成的盐的质量最小,盐的极小值为$\frac{3.52g}{64g/mol}$×104g/mol=5.72g,
故固体的质量最小值大于5.72g,最大值可以为8.48 g,
故选:AB.
点评 本题考查混合物的有关计算,难度较大,关键是利用极值法进行解答,注意氢氧化钠可能会剩余,侧重于考查学生的分析能力和计算能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. 、
、 、
、 (其中三种).
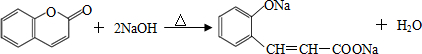
(其中三种). 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
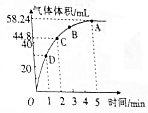 取等物质的量浓度、等体积的H2O2溶液分别进行H2O2的分解实验,实验报告如下表所示(现象和结论略)
取等物质的量浓度、等体积的H2O2溶液分别进行H2O2的分解实验,实验报告如下表所示(现象和结论略) | 序号 | 条件 | 现象和结论 | |
| 温度/℃ | 催化剂 | ||
| 1 | 40 | FeCl3溶液 | |
| 2 | 20 | FeCl3溶液 | |
| 3 | 20 | MnO2 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ② | B. | ②③ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
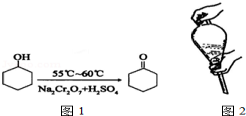 环己酮是一种重要的有机化工原料.实验室合成环己酮的反应如图1;环己醇和环己酮的部分物理性质见表:
环己酮是一种重要的有机化工原料.实验室合成环己酮的反应如图1;环己醇和环己酮的部分物理性质见表:| 物质 | 相对分子质量 | 沸点(℃) | 密度(g•cm-3、20℃) | 溶解性 |
| 环乙醇 | 100 | 161.1 | 0.9624 | 能溶于水和醚 |
| 环己酮 | 98 | 155.6 | 0.9478 | 微溶于水,能溶于醚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石、碳化硅、晶体硅的熔点依次升高 | |
| B. | CO2和SiO2 化学式相似,物理性质也相似 | |
| C. | CH3CH(CH2OH)CH2OOCCH3是一种手性分子,水解后手性消失 | |
| D. | 水加热到很高的温度都难以分解是因为水分子间存在氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molFeBr2与1molCl2反应时转移的电子数为1NA | |
| B. | 10g H218O与D216O的混合物中所含中子、电子数目均为5NA | |
| C. | 标况下,22.4L甲烷中含有C-H键数为1NA | |
| D. | pH=2的H2SO4溶液1L,含H+的数目为0.02NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com